-
某废水处理厂处理废水中NH+的过程如下:
①NH4+ (aq)+ O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH=-b KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH=-b KJ/mol
②2HNO2(aq)+O2(g)=2NO3- (aq)+2H+ ΔH=-aKJ/mol
下列叙述正确的是( )
A.将NH4+转化为NO3-的热化学方程式可表示为:
NH4+ (aq)+2O2(g)=NO3- (aq)+2H+(aq)+H2O(1) ΔH=-(b+ )KJ/mol
)KJ/mol
B.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
C.常温下,若HNO3溶液中c(H+)=0.1 mol·L-1,则该溶液的pH>1
D.若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)=c(NO3-)+c(H+)
-
某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H =-273kL/mol
②NO2-(aq)+l/2O2(g)=NO3-(aq) △H =-73kL/mol
下列叙述不正确的是
A. lmol的NH3和1mol的NH4+都有10×6.02×1023个电子
B. 室温下,0.1mol/LHNO2(aq) pH>l,则NaNO2溶液显碱性
C. NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) △H =-346kL/mol
D. 在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH4+在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) △H=-273kJ·mol-1
②NO2-(aq)+1/2O2(g)=NO3-(aq) △H=-73kJ·mol-1
下列说法正确的是( )
A.1mol的NH3和1mol的NH4+都有10×6.02 ×1023个质子
B.室温下,NH4NO2溶液呈酸性,则说明Ka(HNO2)< Kb(NH3·H2O)
C.NH4+(aq)+2O2(g) NO3—(aq)+2H+(aq)+H2O(l);△H= - 346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确的是
A.1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子
B.室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性
C.NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol
D.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
某废水中含有的NH 在一定条件下可被O2氧化,反应过程如下:
在一定条件下可被O2氧化,反应过程如下:
①NH4+(aq)+3/2O2(g)=NO2-(aq)+2H+(aq)+H2O(l) ΔH = -273kJ/mol
②NO2-(aq)+1/2O2(g)=NO3-(aq) ΔH = -73kJ/mol
下列叙述不正确的是
A. 1mol的NH3和1mol 的NH4+都有10×6.02×1023个电子
B. 室温下,0.1 mol/L HNO2溶液pH>1,则NaNO2溶液显碱性
C. NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH= -346kJ/mol
D. 在上述两次转化过程中,废水的酸性先增大然后逐渐减弱
-
氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
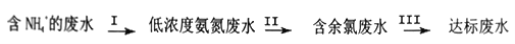
(1)过程Ⅰ:加NaOH溶液,调节pH至11后,并鼓入大量空气。用离子方程式表示加NaOH溶液的作用是______________;用化学平衡理论解释鼓入大置空气的目的__________________。
(2) II中加入适量NaClO溶液,控制pH在3~4,将NH4+转化为无毒物质。则反应的离子方程式是__________________。
(3)分别称取2.39 g (NH4)2SO4和NH4Cl固体混合物两份。
①将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为__________。
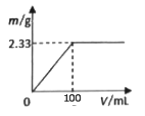
②另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_______ (溶液体积变化忽略不计)。
-
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3· H2O的形式存在,该废水的处理流程如下:
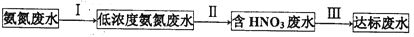
(1)过程I:加NaOH溶液,升温至60 ℃,调节pH至9后,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:_____________________。
②用化学平衡原理解释通空气的目的:_____________________。
③回收的氨气经净化处理后可进行催化氧化,已知催化剂为Cr2O3。
i.氨催化氧化的化学方程式为____________________。
ii.预先将催化剂加热到红热状态,停止加热后催化剂仍保持红热,该反应是______反应。
(填“吸热”或“放热”)
(2)过程II:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。请完成第一步反应的离子方程式:__________________________________________
(3)过程III:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 gCH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是_______。
-
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在,该废水的处理流程如下:
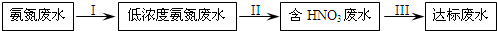
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收.
①用离子方程式表示加NaOH溶液的作用:________.
②用化学平衡原理解释通空气的目的:________.
(2)过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化示意图如下:

①第一步反应是________反应(选题“放热”或“吸热”),判断依据是________.
②1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是:________.
-
某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,该废水的处理流程如下:

(1)过程Ⅰ:加NaOH溶液,其作用用离子方程式表示为____________,调节pH至9后,升温至30℃,通空气将氨赶出并回收;
(2)过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

①第一步反应的热化学方程式是____________;
②1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是____________;
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32gCH3OH转移6mol电子,则该反应的化学方程式是____________。
-
资料显示,可用次氯酸钠处理废水中的氨氮(NH3),使其转化为氮气除去,其主要反应如下:
① NH3(aq)+ HClO(aq)═ NH2Cl(aq)+ H2O(l)
② 2NH2Cl(aq)+ HClO(aq)═ N2(g)+ H2O(l)+ 3HCl(aq)
(1)在其他条件不变的情况下,向一定量废水中逐滴滴加次氯酸钠溶液,氨氮去除率随n(NaClO)/n(NH3)的变化曲线如下:
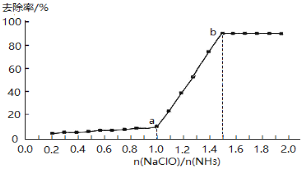
Ⅰ.物质NH2Cl中氮元素的化合价是____________。
Ⅱ.a-b点间,溶液中氨氮去除率迅速提高的原因是__________。
(2)Ⅰ.反应①②中HClO 的来源用化学用语解释是__________。
Ⅱ.实验测得,废水中pH与氨氮去除率如图所示:
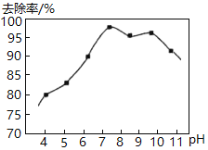
pH较高时,氨氮去除率下降的原因是__________。
pH较低时,氨氮去除率也下降,可能的原因是__________。
(3)运用上述原理去除废水中的氨氮,可结合下图所示的电解法。
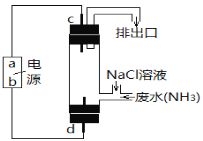
Ⅰ. a极为__________。
Ⅱ. d极反应式为__________。
O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH=-b KJ/mol
)KJ/mol