-
.LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g) 2LiH(s) △H=-182kJ·mol-1;
2LiH(s) △H=-182kJ·mol-1;
②2H2(g)+O2(g) 2H2O(1) △H=-572kJ·mol-1;
2H2O(1) △H=-572kJ·mol-1;
③4Li(s)+O2(g) 2Li2O(s) △H=-1196kJ·mol-1。
2Li2O(s) △H=-1196kJ·mol-1。
则LiH在O2中燃烧的热化学方程式为( )
A. 2LiH(s)+O2(g) Li2O(s)+H2O(1) △H=-702kJ·mol-1
Li2O(s)+H2O(1) △H=-702kJ·mol-1
B. 2LiH(s)+O2(g) Li2O(s)+H2O(1) △H=-1950kJ·mol-1
Li2O(s)+H2O(1) △H=-1950kJ·mol-1
C. 2LiH(s)+O2(g) Li2O(s)+H2O(1) △H=-1586kJ·mol-1
Li2O(s)+H2O(1) △H=-1586kJ·mol-1
D. 2LiH(s)+O2(g) Li2O(s)+H2O(g) △H=-988kJ·mol-1
Li2O(s)+H2O(g) △H=-988kJ·mol-1
-
H2的燃烧热为286 kJ/mol,Li的燃烧热为299 kJ/mol。LiH可做飞船燃料,合成LiH的热化学方程式是2Li(s)+H2(g)=2LiH(s)△H=-182kJ/mol,则LiH的燃烧热为( )
A. 702 kJ/mol B. 442 kJ/mol C. 585 kJ/mol D. 351 kJ/mol
-
LiH(氢化锂)常用作干燥剂、氢气发生剂等,可利用下列反应制备:2Li(熔融)+H2 =2LiH。下列说法正确的是
A. H2作还原剂
B. 生成1 mol LiH,转移电子的物质的量为2 mol
C. 4 g LiH与足量水反应最多可生成1 g氢气
D. 22. 4 L H2与足量Li反应最多可制取2 mol LiH
-
(1) 0.5 mol C2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出683.4 kJ热量,写出该反应的热化学方程式___________________。
(2)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)= 2LiH(s) ΔH=-182 kJ·mol-1
②2H2(g)+O2(g)= 2H2O(l) ΔH=-572 kJ·mol-1
③4Li(s)+O2(g)= 2Li2O(s) ΔH=-1 196 kJ·mol-1
试写出LiH在O2中燃烧的热化学方程式__________________。
(3) “长征三号甲”三子级使用的燃料是液氢和液氧,下面是298 K时,氢气(H2)、氧气(O2)有关变化的反应热:
①H2(g)+O2(g)= H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)= H2(l) ΔH=-0.92 kJ·mol-1
③O2(g)= O2(l) ΔH=-6.84 kJ·mol-1
④H2O(g)= H2O(l) ΔH=-44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:____________。
-
肼(N2H4)又称联氨,常用作火箭推进器的燃料。已知:
①N2(g)+O2(g)=2NO(g) ΔH1=+182kJ·mol-1;
②2NO(g) +O2(g)=2NO2(g) ΔH2=-114.3kJ·mol-1;
③2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH2=-1135.7kJ·mol-1。
下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-1068kJ·mol-1
B.用铂作电极,以KOH溶液为电解液的肼 空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O
空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O
C.肼与氨类似,溶于水显碱性,可表示为N2H4+H2O=N2H5++OH-
D.某密闭容器中存在:2NO2(g) N2O4(g),加压
N2O4(g),加压 缩小体积
缩小体积 后颜色先变深后变浅,不能用勒夏特列原理解释
后颜色先变深后变浅,不能用勒夏特列原理解释
-
下列变化中一定为放热反应的是( )
A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
B.N2(g)+O2(g)===2NO(g) ΔH=+182.6 kJ·mol-1
C.形成化学键过程中放出862 kJ热量的化学反应
D.能量变化如图所示的化学反应

-
下列变化中一定为放热的化学反应的是

A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
B.N2(g)+O2(g)===2NO(g) ΔH=+182.6 kJ·mol-1
C.形成化学键过程中放出862 kJ热量的化学反应
D.能量变化如上图所示的化学反应
-
已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJ·mol−1
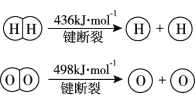
下列说法不正确的是
A.该反应可作为氢氧燃料电池的反应原理
B.破坏1 mol H-O键需要的能量是463.4 kJ
C.H2的燃烧热ΔH<-241.8 kJ·mol−1
D.H2(g)中的H-H键比H2O(g)中的H-O键牢固
-
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
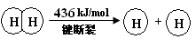

下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
-
液氨气化后,分解产生的氢气可作为氢氧燃料电池的燃料。氨气分解反应的热化学方程式如下:
2NH3(g)  N2 (g) + 3H2(g) H = + a kJ·mol-1
N2 (g) + 3H2(g) H = + a kJ·mol-1
请回答下列问题:
(1)已知:2H2 (g) + O2 (g) =2H2O(l) H = - b kJ·mol-1
NH3 (g)  NH3(l) H = - c kJ·mol-1
NH3(l) H = - c kJ·mol-1
则4NH3(l) + 3O2 (g) = 2N2 (g) + 6H2O(l) 的H = kJ·mol-1。
(2)水能发生电离:2H2O(l)  H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式 。
H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式 。
(3)实验室用Pt电极对液氨进行电解可以得到H2和N2 ,若电解过程中阳极收集得到4.48L气体(标况),则转移的电子的数目是 ,标准状况下阴极得到的气体的质量为 g。
2LiH(s) △H=-182kJ·mol-1;
2H2O(1) △H=-572kJ·mol-1;
2Li2O(s) △H=-1196kJ·mol-1。
Li2O(s)+H2O(1) △H=-702kJ·mol-1
Li2O(s)+H2O(1) △H=-1950kJ·mol-1
Li2O(s)+H2O(1) △H=-1586kJ·mol-1
Li2O(s)+H2O(g) △H=-988kJ·mol-1




