-
热化学方程式C(s)+H2O(g)
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1 表示的
为( )
A.碳与水反应吸收131.3 kJ的热量
B.1 mol碳和1 mol水反应吸收131.3 kJ的热量
C.1 mol固态碳与1 mol水蒸气反应产生一氧化碳气体和氢气,吸收131.3 kJ的热量
D.固态碳和气态水各1 mol反应,放出131.3 kJ的热量
高三化学选择题中等难度题查看答案及解析
-
C(s) + H2O(g) ="=" CO(g) + H2(g);△H =" +131.3" KJ/mol。它表示
A.碳与水反应吸收131.3 KJ的热量
B.1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量
C.1mol碳和1mol水反应吸收131.3 KJ的热量
D.固态碳和气态水各1mol反应,放出131.3 KJ的热量
高三化学选择题中等难度题查看答案及解析
-
热化学方程式C(s)+H2O(g)
CO(g)+H2(g) △H=+131.3 kJ·mol-1表示 ( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸收131.3KJ 热量
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
高三化学选择题简单题查看答案及解析
-
红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量。能表示该反应热化学方程式的是
A. C+H2O→H2+CO-131.3kJ
B. C(s)+H2O(l)→H2(g)+CO(g)+131.3kJ
C. C(s)+H2O(g)→H2(g)+CO(g)-131.3kJ
D. C(s)+H2O(g)→H2(g)+CO(g)+131.3kJ
高三化学单选题中等难度题查看答案及解析
-
炭和水蒸气反应生成1 mol H2和 1 mol CO,吸收 131.3kJ 热量,该反应的热化学方程式是
A. C(s) + H2O(l) → H2(g) + CO(g)-131.3kJ
B. C(s) + H2O(g) → H2(g) + CO(g)-131.3kJ
C. C(s) + H2O(g) → H2(g) + CO(g) + 131.3kJ
D. C(s) + H2O(l) → H2(g) + CO(g) + 131.3kJ
高三化学单选题简单题查看答案及解析
-
(1)已知: C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
C(s)+H2O(g)=CO(g)+H2(g) ΔH2=+131.3 kJ/mol
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= ____ ___kJ/mol。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)
CH3OH(g) ΔH
①下列情形不能说明该反应已达到平衡状态的是_______(填序号)。
A.每消耗1 mol CO的同时生成2molH2
B.混合气体总物质的量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
②CO的平衡转化率(α)与温度、压强的关系如图所示。A、B两点的平衡常数K(A)_______K(B)(填“>”、“=”或“<”,下同);由图判断ΔH _____0。

③某温度下,将2.0 mol CO和6.0 molH2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25 mol/L,则CO的转化率= ,此温度下的平衡常数K= (保留二位有效数字)。
(3)工作温度650℃的熔融盐燃料电池,用煤炭气(CO、H2)作负极反应物,空气与CO2的混合气体为正极反应物,催化剂镍作电极,用一定比例的Li2CO3和Na2CO3低熔点混合物作电解质。负极的电极反应式为:CO+H2-4e-+2CO32-=3CO2+H2O;则该电池的正极反应式为 。
高三化学填空题极难题查看答案及解析
-
(1)煤气化制合成气(CO和H2)
已知:C(s)+H2O(g)===CO(g)+H2(g)ΔH2=131.3kJ·mol−1
C(s)+2H2O(g)===CO2(g)+2H2(g)ΔH2=90kJ·mol−1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是_____
(2)由合成气制甲醇
合成气CO和H2在一定条件下能发生反应:CO(g)+2H2(g)
CH3OH(g)ΔH<0。
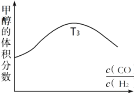
①在容积均为VL的甲、乙、丙、丁四个密闭容器中分别充入amolCO和2amolH2,四个容器的反应温度分别为T1、T2、T3、T4且恒定不变。在其他条件相同的情况下,实验测得反应进行到tmin时H2的体积分数如图所示,则T3温度下的化学平衡常数为_____(用a、V表示)

②图反映的是在T3温度下,反应进行tmin后甲醇的体积分数与反应物初始投料比
的关系,请画出T4温度下的变化趋势曲线。______________
③在实际工业生产中,为测定恒温恒压条件下反应是否达到平衡状态,可作为判断依据的是_____
A.容器内气体密度保持不变 B.CO 的体积分数保持不变
C.气体的平均相对分子质量保持不变 D.c(H2)=2c(CH3OH)
(3)由甲醇制烯烃
主反应:2CH3OH
C2H4+2H2O i;
3CH3OH
C3H6+3H2O ii
副反应:2CH3OH
CH3OCH3+H2O iii
某实验室控制反应温度为400℃,在相同的反应体系中分别填装等量的两种催化剂(Cat.1和Cat.2),以恒定的流速通入CH3OH,在相同的压强下进行甲醇制烯烃的对比研究,得到如下实验数据(选择性:转化的甲醇中生成乙烯和丙烯的百分比)
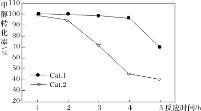
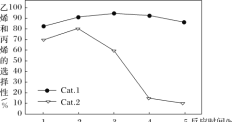
由图像可知,使用Cat.2反应2h后甲醇的转化率与乙烯和丙烯的选择性均明显下降,可能的原因是(结合碰撞理论解释)_____
高三化学综合题中等难度题查看答案及解析
-
通过以下反应均可获取H2。
① C(s) + H2O (g) =CO(g)+H2(g) ΔH1 = + 131.3 kJ·mol-1
② CH4 (g)+H2O(g) = CO(g)+3H2 (g) ΔH2 = + 206.1 kJ·mol-1
③ CO(g)+H2O(g) = CO2(g)+H2(g) ΔH3
下列说法正确的是( )
A.①中反应物的总能量大于生成物的总能量
B.②中使用适当催化剂,可以使ΔH2减小
C.由①、②计算反应CH4 (g) = C (s) + 2H2 (g) 的ΔH =-74.8 kJ·mol-1
D.若知反应C (s) + CO2 (g) = 2CO (g) 的ΔH,结合ΔH1可计算出ΔH3
高三化学单选题中等难度题查看答案及解析
-
煤化工中两个重要反应为①C(s)+H2O(g)
H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g)
 CO2(g)+ H2(g)。
CO2(g)+ H2(g)。(1)下列说法正确的是 。
A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度
B.反应②的熵变△S>0
C.反应①中增加C固体的量能增大反应速率
D.在反应中②及时分离出产生的H2对正反应速率无影响
(2)若工业上要增加反应①的速率,最经济的措施为 。
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达到平衡所
需时间/ min
CO
H2O
H2
CO2
I
650
4
2
1.6
1.6
5
Ⅱ
900
2
1
0.5
0.5
3
Ⅲ
900
a
b
c
d
t
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为___。
②CO(g)和H2O(g)反应的△H 0(填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______,与实验Ⅱ相比,化学平衡常数 (填“增大”、“减小”或“不变”)。
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1 mol CO、0.5 mol H2O、0.2 mol CO2、0.5 mol H2,平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)。
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g)
CH3OH(g)ΔH= -mkJ·mol-1
反应②: 2CO(g)+4 H2(g)
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
反应③:2CH3OH(g)
CH3OCH3(g)+ H2O(g)△H<0
则m与n的关系为 。
高三化学填空题极难题查看答案及解析
-
(7 分 )水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g)≒CO (g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
容器编号
c(H2O)/mol·L-1
c(CO)/mol·L-1
c(H2)/mol·L-1
V正、V逆比较
I
0.06
0.60
0.10
V正=V逆
II
0.06
0.50
0.40
?
III
0.12
0.40
0.80
V正<V逆
IV
0.12
0.30
?
V正=V逆
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为________;向该容器中补充 a mol 炭,水蒸气的转化率将________(填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为________。
(3)己知:C (s) +
O2(g)=CO (g);△H = -110.5kJ·mo1-1
CO(g) +
O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
H2 (g) +
O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H =________kJ·mo1-1
高三化学填空题中等难度题查看答案及解析