-
周期表前四周期元素R、X、Y、Z原子序效依次增大,RO2是红棕色气体:X位于元素周期表ⅣB族:同周期元素的基态原子中,Y的未成对电子最多;基态Z+最外层有18个电子。请回答下列问题:
(l)基态Y原子的价层电子轨道示意图为__________。
(2) RO3-的立体构型是______________,写出两个与RO3- 其有相同空间构型和键合形式的分子或离子____________。
(3) R及与R相邻的同周期元素中,第一电离能最大的是____(填元素符号), 原因是_____。
(4)若过渡金属离子具有未成对d电子,容易吸收可见光而发生d-d跃迁,因而它们的水合离子常常具有颜色;若过渡金属离子无未成对d电子,则其水合离子是无色的。下列水合离子为无色的是_____
A. X2+ B.X4+ C. Y3+ D. Z2+
(5)右图是Z与金的一种合金晶体的立方晶胞:
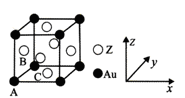
① 该晶体中,Z与Au的原子个数比为_________;
② 原子坐标参数可表示晶胞内各原子的相对位置。图示晶胞中,原子坐标参数A为(0, 0,0 );
B为(0,1/2,1/2)则C原子(底心)的坐标参数为__________。
③ 已知该立方晶胞的密度为dg/cm3 ,NA为阿伏伽德罗常数的值,则晶胞参数(描述晶胞的大小和形状)a=_______nm。(列出表达式即可)
-
有位于周期表前四周期的A、B、C、D、E、F六种元素,其原子序数依次增大。已知A原子核外有三个未成对电子;A与B形成的一种化合物常温下是红棕色气体;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;F原子核外最外层电子数与C相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D四种原子的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)C的氯化物的熔点比D的氯化物的熔点________(填“高”或“低”),理由是________。
(3)E的最高价氧化物分子的空间构型是________。
(4)基态F+离子的核外电子排布式是________,F的高价离子与A的最常见氢化物形成的配离子的化学式为________。
(5)Q分子是A2B的等电子体,Q的结构式为________,Q分子的中心原子的杂化类型是________。
(6)下图是B、F两元素组成的一种化合物的晶胞,其化学式为________。
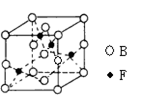
-
W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为 。下列叙述正确的是( )
。下列叙述正确的是( )
A.X与W、Y及Z均能组合成多种化合物 B.简单离子半径:Y>Z>X>W
C.W的氧化物的水化物一定为强酸 D.化合物Y2Z2中Y不满足8电子稳定结构
-
W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为 。下列叙述正确的是( )
。下列叙述正确的是( )
A.X与W、Y及Z均能组合成多种化合物 B.简单离子半径:Y>Z>X>W
C.W的氧化物的水化物一定为强酸 D.化合物Y2Z2中Y不满足8电子稳定结构
-
周期表前四周期的元素 、
、 、
、 、
、 ,原子序数依次增大,X原子基态时
,原子序数依次增大,X原子基态时 层中
层中 轨道电子数与s轨道电子数相同;
轨道电子数与s轨道电子数相同; 原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;
原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料; 位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
(1)X位于周期表的第_______周期,第______族。
(2)元素的第一电离能:X______Y(填“>”或“<”,下同);原子半径:X______Y。
(3) 的最高价氧化物对应水化物中酸根离子的空间构型是_______(用文字描述)。
的最高价氧化物对应水化物中酸根离子的空间构型是_______(用文字描述)。
(4) 基态核外电子排布式为_________,用铁氰化钾溶液检验
基态核外电子排布式为_________,用铁氰化钾溶液检验 的离子方程式为___________。
的离子方程式为___________。
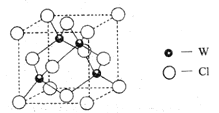
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是_______,它可与浓盐酸发生非氧化还原反应,生成配合物 ,反应的化学方程式:_________。
,反应的化学方程式:_________。
-
【选修3:物质结构与性质】X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是___________;Z所在周期中第一电离能最大的主族元素是___________(元素名称)。
(2)XY2¯离子的立体构型是___________;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是___________(元素符号)。
(3)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是______________________。
(4)Y与R所形成的化合物晶体晶胞如下图所示,该晶体的化学式:___________;晶胞参数如下图所示,则该晶胞密度是___________g·cm-3(列式并计算结果,保留小数点儿后一位)。
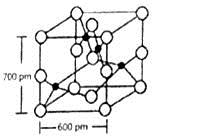
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________(填标号)。
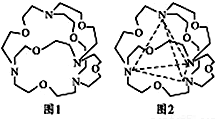
a.CF4b.CH4c.NH4+d.H2O
-
X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是______;Z所在周期中第一电离能最大的主族元素是_______(元素名称)
(2)XY2¯ 离子的立体构型是________;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是________(元素符号)。
(3) 已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是_______________
(4)Y与R所形成的化合物晶体晶胞如右图所示,该晶体的化学式:_____________;晶胞参数如图所示,则该晶胞密度是_______________g·cm-3(列式并计算结果,保留小数点儿后一位)。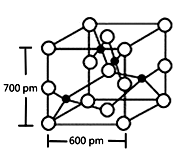

(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是________(填标号)。
A.CF4 B.CH4 C.NH4+ D.H2O
-
X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是______;Z所在周期中第一电离能最大的主族元素是_______(元素名称)
(2)XY2¯ 离子的立体构型是________;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是________(元素符号)。
(3)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是_______________。
(4)Y与R所形成的化合物晶体晶胞如图所示,该晶体的化学式:_____________;晶胞参数如图所示,则该晶胞密度是___________g‧cm-3(列式并计算结果,保留小数点儿后一位)。
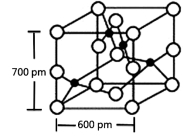
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是________(填标号)。
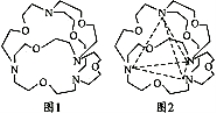
a.CF4 b.CH4 c.NH4+ d.H2O
-
短周期主族元素W、X、Y和Z的原子序数依次增大,W的气态氢化物的水溶液可使酚酞变红,W与X可形成一种红棕色有刺激性气味的气体,Y的原子半径是所有短周期主族元素中最大的,Z原子最外层电子数与W原子的电子总数相同。下列说法中正确的是
A. W的氧化物对应水化物均为强酸
B. 简单离子半径:W<X<Y
C. 简单氢化物沸点:Z<W
D. Y与Z形成的化合物的水溶液呈碱性
-
短周期元素X、Y、Z、W原子序数依次增大,XY2是红棕色气体,Z的周期数等于族序数,W的最外层电子数比次外层电子数少1,下列说法正确的是( )
A.原子半径:X<Y<Z B.气态氢化物的稳定性:Y<X<W
C.最高正价:Z<X<Y<W D.Y、W均可与Na形成离子化合物


 。下列叙述正确的是( )
。下列叙述正确的是( ) 。下列叙述正确的是( )
。下列叙述正确的是( )





