-
已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol。下列关于中和热的说法中正确的是
A.在稀溶液中所有酸和碱反应的中和热数值都相等
B.在稀溶液中1mol酸和1mol碱反应放出的热量都相等
C.在稀溶液中HCl和NaOH反应、HNO3和KOH的反应的中和热相等
D.将浓硫酸滴入稍过量的氢氧化钠溶液中刚好生成1mol水时,产生的热量即中和热
高二化学选择题简单题查看答案及解析
-
下列说法中正确的是
A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应、稀醋酸与稀NaOH溶液反应所测得的中和热都为ΔH=-57.3kJ/mol
B.由C(石墨,s)= C(金刚石,s)ΔH=+1.9kJ/mol,可知金刚石比石墨稳定
C.在用标准盐酸滴定未知浓度氢氧化钠溶液的实验中,若用待测液润洗锥形瓶,则测定结果偏低(其他操作正确)
D.向存在着FeCl3 (黄色)+3KSCN
Fe(SCN) 3(血红色) +3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化
高二化学选择题中等难度题查看答案及解析
-
下列有关中和热概念、中和热测定实验(如图)的说法正确的是
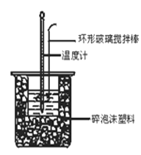
A.已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有
H2SO4(aq)+
Ba(OH)2(aq)=
BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
B.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ·mol-1,则该反应的中和热为114.6 kJ·mol-1。
C.中和热测定实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.酸碱混合时,量筒中的NaOH溶液应分多次倒入已装有盐酸的小烧杯中,并不断用环形玻璃搅拌棒搅拌。
高二化学单选题简单题查看答案及解析
-
下列说法正确的是
A. 已知NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) ΔH = - 57.3 kJ/mol ,则含有40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量。
B. 已知2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+2O2(g)=2CO (g) ΔH =b kJ/mol,则a>b。
C. 取50mL 0.55mol/LNaOH(aq)和50mL 0.50mol/L HCl(aq)进行中和热的测定实验,用温度计测定HCl(aq)起始温度后,直接测定NaOH(aq)的温度,会使中和热ΔH偏小
D. 已知P(白磷,s)=P(红磷,s) ΔH<0,则白磷比红磷稳定。
高二化学单选题中等难度题查看答案及解析
-
下列热化学方程式,正确的是
A.已知中和热为57.3 kJ/mol:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.3 kJ/mol
B.1 mol SO2与2 mol O2在某密闭容器中反应放出88 kJ热量,则反应的热化学方程式为:2SO2(g)+O2(g)
2SO3(g) △H=-176 kJ/mol
C.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
D.8 g 固体硫完全燃烧生成SO2,放出74kJ热量:S(s)+O2(g)=SO2(g) ΔH=-296 kJ/mol
高二化学单选题中等难度题查看答案及解析
-
下列有关H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ·mol-1的离子反应说法正确的是( )
A.代表所有的酸碱中和反应
B.反应物一定是强酸与强碱
C.强酸与强碱的中和反应都可以这样表示
D.代表稀的强酸与稀的强碱反应生成1mol液态水时,放出热量57.3kJ
高二化学单选题困难题查看答案及解析
-
下列依据热化学方程式得出的结论正确的是( )
A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ·mol-1,则含20.0gNaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.65kJ
B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ·mol-1,则标况下1mol氢气完全燃烧放出241.8kJ的热量
C.已知2C(s)+2O2(g)=2CO2(g)△H=akJ·mol-1,
2C(s)+O2(g)=2CO(g)△H=bkJ·mol-1,则a>b
D.已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定
高二化学选择题中等难度题查看答案及解析
-
已知中和热的热化学方程式为H + (aq)+OH - (aq)=H2O(l)△H=-57.3kJ·mol-1。下列反应均在稀溶液中进行,其中△H=-57.3kJ·mol-1的是
A. NaOH(aq)+ HNO3 (aq)= NaNO3(aq) + H2O(l) △H
B. NH3·H2O(aq)+ HCl(aq)= NH4Cl(aq)+ H2O(l) △H
C. HF(aq)+ KOH(aq)= KF(aq)+ H2O(l) △H
D. ½H2SO4(aq)+ ½Ba(OH)2(aq)= ½BaSO4(s)+ H2O(l) △H
高二化学单选题困难题查看答案及解析
-
下列说法正确的是( )
A.反应N2(g)+3H2(g)⇌2NH3(g)的△H<0,△S>0
B.在稀溶液中,H+(aq)+OH-(aq)═H2O(l) 中和热△H=-57.3 kJ•mol-1
C.燃烧热就是物质燃烧时所放出的热量
D.升高温度或加入催化剂,可以改变化学反应的反应热
高二化学单选题简单题查看答案及解析
-
下列与化学反应能量变化相关的叙述正确的是( )
A. 放热反应的反应速率总是大于吸热反应的反应速率
B. 已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,则中和热的热效应为57.3 kJ
C. 应用盖斯定律,可计算某些难以直接测量的反应焓变
D. 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
高二化学单选题中等难度题查看答案及解析