-
(共13分)
(1)混合物分离的方法在生产、生活和科学实验中有着广泛的应用。请指出下列做法中分别应用了哪些分离方法?
A、分液 B、过滤
C、萃取 D、蒸馏
E、蒸发结晶 F、加热分解
①除去Ca(OH)2 溶液中悬浮的 CaCO3 ;②从碘水中提取碘 ;
③用自来水制取蒸馏水 ;④分离植物油和水 ;
⑤海水淡化 ;⑥除去 KCl 中少量 KClO3 ;
⑦熬煮中药 ;⑧用海水晒盐 。
(2)某同学要配制100mL 1mol·L-1NaCl溶液,配制时需选用的仪器主要有
, , , , 和试剂瓶。
高一化学填空题困难题查看答案及解析
-
混合物分离的方法在生产、生活和科学实验中有着广泛的应用。请指出下列做法中分别应用了哪些分离方法?(请把答案填写在横线上)
(1)除去豆浆中的颗粒物杂质_______________ (2)用海水晒盐________________
(3)除去豆油中的水_____________________ (4)从碘水中提取碘__________________
高一化学实验题中等难度题查看答案及解析
-
混合物分离的方法在生产、生活和科学实验中有着广泛的应用,请指出下列做法中分别应用了哪些分离方法。
(1)除去豆浆中的颗粒物杂质______________
(2)用海水晒盐___________________
(3)除去豆油中的水____________________
(4)从碘水中提取碘_______________
高一化学实验题中等难度题查看答案及解析
-
萃取在生产和科学实验中有着广泛应用。下列混合物的分离中,需要应用萃取这种分离方法的是
A. 海水淡化 B. 分离豆浆和豆渣
C. 用海水晒盐 D. 从碘水中提取碘
高一化学单选题简单题查看答案及解析
-
氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
(1) 实验室制备NH3,下列方法中可以选用的是_______________。
A.固态氯化铵与熟石灰混合加热 B.固态氯化铵加热分解
C.碱石灰中滴加浓氨水 D.氯化铵溶液与氢氧化钠溶液共热
(2) “氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收所得气体制取硝酸(固定装置略去):
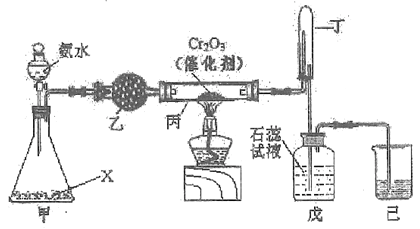
①盛装氨水仪器的名称是________。甲装置不需要加热即能同时产生氨气和氧气,则锥形瓶内固体X的化学式为____________。
②乙装置中药品的名称是_________。写出受热时丙装置发生反应的化学方程式________。
③当戊中观察到______现象,则说明戊中制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,并没有观察到此现象,请分析实验失败的可能原因________,如何改进装置_________。
(3) 若将氨气和氯气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出该反应的化学方程式_____________。
高一化学实验题中等难度题查看答案及解析
-
(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏、萃取、结晶)
a、熬煮中药______ b、分离豆浆和豆渣______c、用海水晒盐______ d、海水淡化______
(2 )今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、H+、Mg2+、Ba2+、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量NaHCO3溶液后,收集到气体0.03mol.
②第二份加足量Ba(NO3)2溶液充分反应后过滤干燥,得干燥沉淀4.66g.
根据上述实验回答:
(a)原溶液中一定不存在的离子是______.
(b)原溶液中可能存在的离子是______.
(c)请计算出原溶液中一定存在的阴离子的物质的量浓度______.高一化学解答题中等难度题查看答案及解析
-
(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏、萃取、结晶)
a、熬煮中药________ b、分离豆浆和豆渣________
c、用海水晒盐________ d、海水淡化________
(2)写出离子反应方程式H++OH-=H2O所对应的两个不同类型化学方程式
①________
②________
(3).在下列反应中:
A.2F2+2H2O=4HF+O2 B.2Na+2H2O=2NaOH+H2↑
C.CaO+H2O=Ca(OH)2 D.2H2O=2H2↑+O2↑
水只作氧化剂的是________,水只作还原剂的是________,水既作氧化剂又作还原剂的是________,水既不作氧化剂又不作还原剂的是________.请用线桥表示B反应的电子转移方向和数目.
2Na+2H2O=2NaOH+H2↑高一化学填空题中等难度题查看答案及解析
-
(10分)(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏 、萃取、结晶)
a、熬煮中药__________________ b、分离豆浆和豆渣__________________
c、用海水晒盐_________________ d、海水淡化__________________
(2 )今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、H+、Mg2+、Ba2+、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量NaHCO3溶液后,收集到气体0.03mol。
②第二份加足量Ba(NO3)2溶液充分反应后过滤干燥,得干燥沉淀4.66g。
根据上述实验回答:
(a)原溶液中一定不存在的离子是_______________________。
(b)原溶液中可能存在的离子是_______________________。
(c)请计算出原溶液中一定存在的阴离子的物质的量浓度________________。
高一化学填空题简单题查看答案及解析
-
(1)请指出下列做法中分别应用了哪些分离方法?(过滤、蒸发、蒸馏 、萃取、结晶)
a、熬煮中药__________________ b、分离豆浆和豆渣__________________
c、用海水晒盐____________________ d、海水淡化__________________
(2)写出离子反应方程式H+ + OH- =H2O所对应的两个不同类型化学方程式
①________
②________
(3).在下列反应中:
A. 2F2+2H2O=4HF+O2 B. 2Na+2H2O=2NaOH+H2↑
C. CaO+H2O=Ca(OH)2 D. 2H2O=2H2↑+O2↑
水只作氧化剂的是________ ,水只作还原剂的是________,水既作氧化剂又作还原剂的是________,水既不作氧化剂又不作还原剂的是________ 。请用线桥表示B反应的电子转移方向和数目。
2Na+2H2O=2NaOH+H2↑
高一化学填空题简单题查看答案及解析
-
铁、铝等金属单质及其化合物在生产和生活中有着广泛的应用。
(1)金属冶炼与处理常涉及氧化还原反应,由下列物质冶炼相应金属单质时采用电解法的是_________。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_______(填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______________________________________________。
(3)利用甲醇(CH3OH)、氧气组成燃料电池,电解质溶液为碱性,电池工作时负极反应式为_____________。
(4)氨气也可作为燃料电池的燃料源制成高效率无污染的燃料电池系统,总反应式为:
(未配平),写出此碱性燃料电池的负极反应式:_______。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为_________________________。
(6)科学家制造出一种使用固体电解质的燃料电池,其效率高无污染,多用于航天航空。如图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-),d电极上的电极反应式为_____________________。
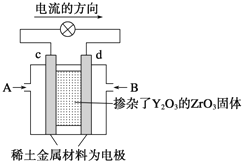
高一化学综合题中等难度题查看答案及解析