-
(物质结构与性质)
Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素D的基态原子电子排布式___________________。
(2)元素A、B形成的单质中,______对应的单质熔点更高,原因是_________________。
(3)写出C的最高价氧化物的水化物与B的最高价氧化物的水化物反应的化学方程式_______________。
(4)元素D可以形成化学式为D(NH3)5BrSO4,配位数均为6的两种配合物。若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为____________。
Ⅱ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。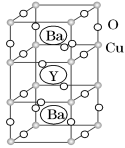
(5)根据图示晶胞结构,推算晶体中Y,Ba,Cu和O原子个数比,确定其化学式为________。
Ⅲ.BF3与一定量的水形成晶体Q [(H2O)2·BF3],Q在一定条件下可转化为R: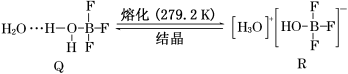
(6)晶体Q中各种微粒间的作用力不涉及________(填字母)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
(7)R中阳离子的空间构型为________,阴离子的中心原子轨道采用_____杂化。
-
(7分)元素周期表是学习物质结构和性质的重要工具,下面是元素周期表的一部分,表中所列字母A、D、E、G、Q、M、R、T分别代表某一化学元素。请用所给元素回答下列问题。
(1)某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为________。
 (2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)________。
(2)某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)________。
(3)M、D两种元素形成的化合物含有的化学键类型是 ________ ,其分子是(填“极性”或“非极性”)________分子;
A分别与D、E、R形成的分子中,分子间存在氢键的是(填分子式)________。
A与D形成分子的空间结构可能是(填序号)________。(2分)
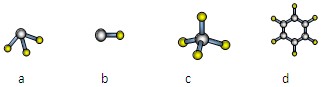
-
元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、m、n、o、r分别代表某一种元素。请回答下列问题。
(1)g元素的原子序数为 ;上述所给11种元素中非金属元素共有 种。
(2)m元素在元素周期表中的位置 ;e、n二元素形成的稳定化合物的化学式为 。
(3)o元素离子的电子式为 ;化合物ba3的结构式为 。
(4)用电子式表示化合物d2n的形成过程 ;
(5)d的最高价氧化物的水化物与e的最高价氧化物反应的离子方程式 。
(6)单质r与b的最高价氧化物的水化物的稀溶液反应的离子方程式 。
-
【化学-选修物质结构与性质】(共12分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| A | | |
| B | C | | D | E | F | G | H | I |
| J | K | | | | M | N | |
| | | | | | | Fe | | | | | | | | | | |
| | | | | | | | | | | | | | | | | |
试依据信息回答下列问题:
(1)上表所示元素中能形成氢化物且氢化物分子间存在氢键最强的是(填氢化物的分子式)________。
(2)Fe元素位于周期表的________区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____价;与CO分子互为等电子体的分子和离子分别为 和 (填化学式)。
(3)在CH4、CO2、CH3OH中,碳原子采取sp3杂化的分子有 。CH3OH的熔、沸点比CH4的熔、沸点高,其主要原因是 ______。
(4)根据VSEPR理论预测NG4- 离子的空间构型为__________型。E、F、G、N原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子的电子式为:__________(任意一种)。
-
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
| a | | |
| b | | | | c | d | e | f | |
| g | h | i | j | | k | l | m |
| n | | | | | | | o | | | | | | | | | | |
试回答下列问题:
(1)请写出字母O代表的元素符号______,该元素在周期表中的位置______.
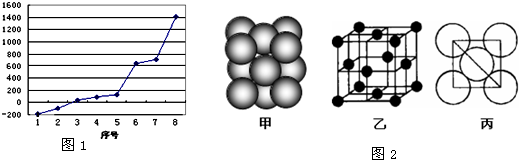
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表______(填元素符号);其中电负性最大的是______(填如图1中的序号).
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是______(填化学式),试从结构角度加以解释:______.
(4)k与l形成的化合物kl2的电子式是______,它在常温下呈液态,形成晶体时,属于______晶体.
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为______,该晶体的密度_______
-
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.

试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为___, 在周期表中位于______区。
(2)写出基态时J元素基态原子原子的价电子排布式_______________,J在周期表中的位置是______。
(3)ABGH的原子半径由大到小顺序是________________;ABCD的第一电离能由大到小顺序是_______;ABCD的电负性由大到小顺序是_____________。
-
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
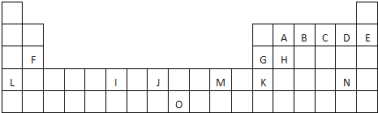
试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为___, 在周期表中位于______区。
(2)写出A原子的核外电子排布的电子排布图 _____________________ ,写出基态时J元素基态原子原子的价电子排布式_______________,J在周期表中的位置是__________;
(3)ABGH的原子半径大小顺序是________________;ABCD的第一电离能大小顺序是_______;ABCD的电负性大小顺序是____________。
-
(16分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| a | | |
| b | | | | c | d | e | f | |
| g | h | i | j | | k | l | m |
| n | | | | | | | o | | | | | | | | | | |
| | | | | | | | | | | | | | | | | |
试回答下列问题:
(1)请写出字母O代表的元素符号________,该元素在周期表中的位置________ 。
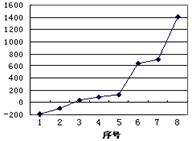
(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________(填元素符号);其中电负性最大的是________(填右图中的序号)。
(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释:________。
(4)k与l形成的化合物kl2的电子式是________,它在常温下呈液态,形成晶体时,属于
________晶体。
(5)i单质晶体中原子的堆积方式如下图(甲)所示,其晶胞特征如下图(乙)所示,原子之间相互位置关系的平面图如下图(丙)所示。

若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
晶胞中i原子的配位数为,一个晶胞中i原子的数目为________, 该晶体的密度为__________________(用M、NA、d表示)。
-
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
| a | | | | | | | | | | | | | | | | | |
| b | | | | | | | | | | | | | c | d | e | f | |
| g | h | | | | | | | | | | | i | j | | k | l | m |
| n | | | | | o | | p | | | | | | | | | | |
(1)在周期表中,与元素b的化学性质最相似的邻族元素是________(填写以上表中字母对应的元素符号),该元素基态原子核外M层电子的自旋状态________(填“相同”或“相反”)。
(2)元素As与________同族(填写以上表中字母对应的元素符号),其简单气态氢化物的稳定性由大到小的顺序是________。
(3)基态ρ原子成为阳离子时首先失去________轨道电子,基态 的最外层电子排布式________。
的最外层电子排布式________。
(4)i的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式为________________。
(5)下列关于上图表中元素说法正确的是________(填序号)。
①未成对电子数最多的元素是O
②元素的电负性强弱;
③元素的第一电离能:
④简单离子半径:
-
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
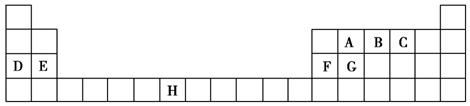
试回答下列问题:
(1)B、D、F、G的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)请写出元素H的基态原子电子排布式_____________________。
(3)A的最简单氢化物分子里中心原子采取________形式杂化,A的最高价氧化物分子的空间构型是________。
(4)D的氯化物的熔点比G的氯化物的熔点________(填“高”或“低”),理由是__________________________。
(5)元素C与元素G形成的晶体所属的晶体类型为________晶体,在该晶体中原子间形成的共价键属于________(从下列选项中选出正确类型)。
A.σ键 B.π键 C.既有σ键,又有π键
(6)F单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。晶胞中F原子的配位数为________,一个晶胞中F原子的数目为________。