-
某化学研究性学习小组对硫酸铜分解气体产物的成分进行如下探究:
【查阅资料】
硫酸铜受热分解生成氧化铜和气体,温度不同时,气体可能为SO3,SO2和O2中的一种、两种或三种。
【提出假设】
假设1:气体产物只有一种;
假设2:气体产物只有两种;
假设3:气体产物有三种。
(1)若假设1成立,则产物气体的成分是 ;若假设2成立,则产物气体的成分是 。
【实验及结果讨论】
(2)甲同学将分解生成的气体依次通过盛浓硫酸和KMnO4酸性溶液的洗气瓶,能说明产物气体中含SO2的现象是 ,该现象说明SO2具有的性质是 ,实验中还发现盛浓硫酸的洗气瓶质量明显增加,原因是 。
(3)乙同学将分解生成的气体通过碱石灰后,再收集测定剩余气体的体积,在不同温度下进行3组实验。请完成下表(实验中硫酸铜均完全分解):
实验
序号
称取CuSO4
的质量/g
碱石灰的
增加质量/g
剩余气体的体积(折算
成标准状况下)/mL
结论
Ⅰ
6.4
假设1成立
Ⅱ
6.4
2.88
224
Ⅲ
6.4
2.56
448
高三化学实验题困难题查看答案及解析
-
某课外研究性化学兴趣小组查阅资料:硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同,气体成分可能含
、
和
中的一种、两种或三种。下列叙述中错误的是( )
A.所得气体成分只有一种,则气体为
B.所得气体成分有两种,则气体为
、
C.所得气体成分有三种,则气体为
、
和
D.若发现气体成分中有
,则该气体中一定含有
高三化学选择题简单题查看答案及解析
-
某学习小组查阅资料加。大多数硝酸盐不稳定。受热易分解,分解产物与金属活动顺序有关)了探究硝酸铁分解产物。他们进行如下探究:
(一)探究气体产物
[提出假设]
他们对气体产物提出如下猜想:
猜想1:气体为NO2
猜想2:气体为NO和O2
猜想3:气体为NO和NO2
清想4:气体为NO2和O2
猜想5:气体为NO
(1)他们经过讨论,认为猜想2不成立。理由是_______;根据氧化还原反应原理,不成立的猜想还有__________
[查阅资料]
①几种气体熔点。沸点如下:
气体
NO
NO2
O2
熔点/℃
-163.6
-11.2
沸点/℃
-151
21.1
-183
②2NO2(g)
N2O4(g)(无色) ΔH<0
[设计实验]
加热装置省略(冰盐冷却剂温度约为-5℃)
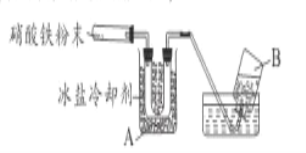
取一定量无水硝酸铁粉术进行实验,实验结果: A中U型管收集到少量液体物质;B中排水法收集一部分气体
(2)本实验的橡胶寨、导管接口处都用锡箔纸包裹,其目的是___________
(3)实验完毕,取出U型管,打开塞子。观察到有棕色气体产生,则U型管内的气体是_____
向U型管加入_____能吸收该物质。避免污染环境。
(4)检验B瓶收集气体为氧气的操作方法是__________
(二)探究固体成分
分析固体中铁元素价态,可能有种情况:①+2价②+3价③+2价和+3价。
为了探究固体中铁元素价态。甲、乙同学设计如下方案:
步骤
现象
甲
取少量样品于试管,加入适量稀硫酸使固体完全溶解,再滴加酸性高锰酸钾溶液
溶液无明显颜色变化
乙
取少量样品于试管,加入稀盐酸使固体完全溶解,滴加KSCN溶液
溶液变红色
(5)上述实验,不能确定固体成分的实验是______(填“甲”或“乙”);根据上迷实验结论。写出硝酸铁分解反应的化学方程式______________
高三化学填空题中等难度题查看答案及解析
-
师大附中某化学研究性学习小组为探究Cu(OH)2受热分解产物及产物性质,设计如下实验过程:
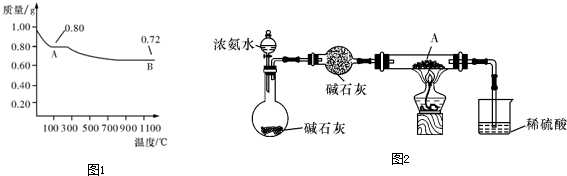
(1)取0.98gCu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示.产物A、B的化学式分别为______
和Cu2O;通过该实验可知,主温时______更稳定(用A或B的化学式表示)
(2)为探究产物A能否被NH3还原,设计如图2实验装置(夹持及尾气处理装置未画出),实验中观察到A变成红色物质,同时生成一种无污染的气体,该气体的化学式为______.小明认为应该在装A物质的试管与烧杯之间增加一个防倒吸装置,你认为是否有必要______(填“有”或“没有”),原因是______.
(3)取少量产物B加入足量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,该反应的离子方程式为______.高三化学解答题中等难度题查看答案及解析
-
无水硫酸铜受热分解生成氧化铜和气体,受热温度不同生成的气体成分也不同。气体成分可能含SO3、SO2和O2中的一种、两种或三种。某化学课外活动小组设计探究性实验,测定反应产生的SO3、SO2和O2的物质的量,并计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如下图所示:
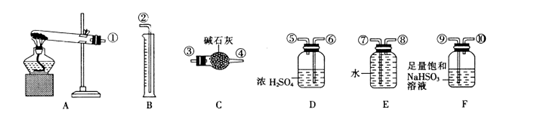
【提出猜想】
猜想I.硫酸铜受热分解所得气体的成分可能只含SO3一种;
猜想Ⅱ.硫酸铜受热分解所得气体的成分可能只含_______两种。
猜想Ⅲ.硫酸铜受热分解所得气体的成分可能含有_______三种。
【实验探究】
已知实验结束时,硫酸铜完全分解。
(1)组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为①→⑨→⑩→⑥→⑤→____→_____→_____→______→②。(填接口序号)
(2)若实验结束时装置B中量筒没有收集到水,则证明猜想_______(填“I”“Ⅱ”或“Ⅲ’’)正确。
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不
同,数据如下:
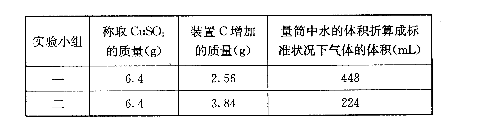
请通过计算,推断出在第一小组和第二小组的实验条件下CuSO4分解的化学方程式:
第一小组:_____________________________________________________________;
第二小组:_____________________________________________________________。
高三化学实验题困难题查看答案及解析
-
某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究。
[探究目的] 分析黑色粉末X的组成,并进行相关实验。
[查阅资料]
①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
④3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O
[实验探究]
I.定性检验
编号
实验操作
实验现象
①
取少量黑色粉末X放入试管1中,注入浓盐酸,微热
黑色粉末逐渐溶解,溶液呈黄绿色;有气泡产生
②
向试管1中滴加几滴KSCN溶液,振荡
溶液出现血红色
③
另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置
有极少量红色物质析出,仍有较多黑色固体未溶解
(1)实验③发生的反应的离子方程式为_____________________________。
(2)上述实验说明黑色粉末X中含有_______________________________。
II.定量测定
根据下图所示的实验方案进行实验并记录数据:

(1)操作Z的名称是_________。
(2)通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为_________。
(3)若溶液Y的体积仍为200mL,则溶液Y中c(Fe3+)=________mol/L。
高三化学实验题困难题查看答案及解析
-
(17分)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验可能用到的仪器如下图所示:
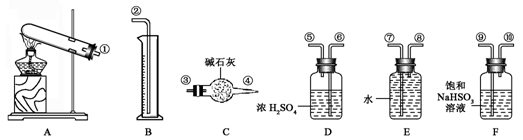
【提出猜想】
Ⅰ.所得气体的成分可能只含________一种;
Ⅱ.所得气体的成分可能含有 ________二种;
Ⅲ.所得气体的成分可能含有 ________ 三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。请回答下列问题:
(1) 请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
__________(填序号)
(2) 若实验结束,B中量筒没有收集到水,则证明猜想 ________ 正确。
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由。答:________
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
实验小组
称取CuSO4
的质量(g)
装置C增加
的质量(g)
量筒中水的体积折算成标
准状况下气体的体积(mL)
一
6.4
2.56
298.7
二
6.4
2.56
448
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:_____________________ ;
二组:_________ 。
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是________和_______(填代号)。
高三化学实验题简单题查看答案及解析
-
(16分)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式,实验用到的仪器如下图所示:
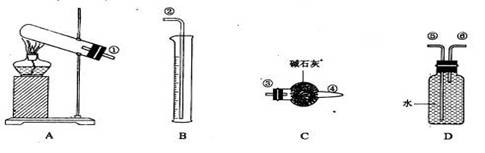
【提出猜想】
I.所得气体的成分可能只含_________一种;
II.所得气体的成分可能含有__________二种;
III.所得气体的成分可能含有SO2、SO3、O2三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。
请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,行仪器接口连接顺序为__________(填序号);
(2)若实验结束,B中量筒没有收集到水,则证明猜想__________正确;
(3)实验过程,仪器C的作用是 ________________________;
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
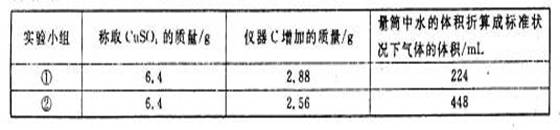
请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式:
① 组_________________________________________________________________;
② 组_______________________________________________________________。
高三化学实验题中等难度题查看答案及解析
-
某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末能被磁铁吸引。查阅资料得知:在温度不同、受热不均时会生成具有磁性的Fe3O4。为进一步探究黑色粉末的组成及含量,他们进行如下实验。
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有___________;
(2)用以下装置可以说明产物有Fe3O4存在:检查装置的气密性,往装置中添加相应的药品,接下来的一步操作为_______________________________。
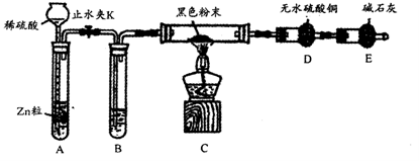
(3)为进一步证明黑色粉末是否含Fe3O4,某同学设计实验方案如下:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象。请分析此方案是否可行,并解释原因。______________________________________。
高三化学简答题困难题查看答案及解析
-
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如下图所示:
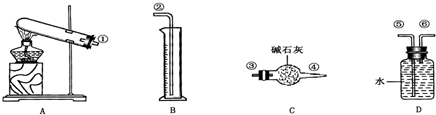
[提出假设]
Ⅰ.所得气体的成分可能只含______一种;
Ⅱ.所得气体的成分可能含有______二种;
Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种.
[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为______(填序号).
(2)实验过程中,仪器C的作用是______.
[验证假设,分析推理]
(3)若实验结束,B中量筒没有收集到水,则证明猜想______正确.
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同.数据如下:
请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式:实验
小组称取CuSO4
的质量/g仪器C增
加的质量/g量筒中水的体积折算成标
准状况下气体的体积/mL① 6.4 2.88 224 ② 6.4 2.56 448
①组______ 4CuO+2SO3↑+2SO2↑+O2↑高三化学解答题中等难度题查看答案及解析