-
(11分)某研究性学习小组,利用固体Na2SO3与中等浓度的H2SO4反应,制备SO2气体并进行有关性质探究实验。该反应的化学方程式为:Na2SO3(固)+H2SO4=Na2SO4 + SO2↑+H2O。除固体Na2SO3和中等浓度的H2SO4外,可供选择的试剂还有:
①溴水 ②浓H2SO4 ③品红试液 ④紫色石蕊试液 ⑤澄清石灰水 ⑥NaOH溶液
回答下列问题:
(1)欲验证SO2的漂白作用,应将SO2气体通入 中(填物质编号),观察到的现象是 ;
(2)欲验证SO2的还原性,应将SO2气体通入 中(填物质编号),观察到的现象是 ;
(3)为说明SO2的氧化性,通常利用的反应是 (写化学反应方程式);
(4)为防止多余的SO2气体污染环境,应将尾气通入 中(填物质编号),
反应离子方程式为 ;
(5)有一实验小组发现,SO2产生缓慢(不考虑SO2在溶液中的溶解,实验中也不存在漏气、反应温度等装置和操作上的问题),请你推测可能的原因(至少填写一种):
① ,② 。
高一化学实验题中等难度题查看答案及解析
-
某研究性学习小组,利用固体Na2SO3与中等浓度的H2SO4反应,制备SO2气体并进行有关性质探究实验。该反应的化学方程式为:Na2SO3(s)+H2SO4=Na2SO4 ↑+H2O+ SO2↑,除固体Na2SO3和中等浓度的H2SO4外,可供选择的试剂还有:
①溴水②浓H2SO4③品红试液④紫色石蕊试液
⑤澄清石灰水⑥NaOH溶液⑦氢硫酸(H2S的水溶液)
回答下列问题:
(1)欲验证SO2的漂白作用,应将SO2气体通入______(填物质编号),观察到的现象是______;
(2)欲验证SO2的还原性,应将SO2气体通入______(填物质编号),观察到的现象是______;
(3)为说明SO2的氧化性,应将SO2气体通入______(填物质编号),发生的化学反应方程式为______;
(4)为防止多余的SO2气体污染环境,最好将尾气通入______(填物质编号),反应离子方程式为______。
高一化学填空题中等难度题查看答案及解析
-
研究性学习小组进行SO2的制备及性质探究实验。
(1)SO2气体制备:原理:Na2SO3(固)+H2SO4(浓)==== Na2SO4+SO2↑+H2O。下列简图是一套实验室制取气体的装置,用于发生、干燥、收集和吸收SO2尾气。

①实验前首先应该进行的操作是____________。
②实验过程中,使分液漏斗滴加浓硫酸的操作是:_______________________。
装置D中所加的试剂是_________________,其作用是__________________。
(2)将SO2气体分别通入下列溶液中:
①品红溶液,现象是__________________________________________________。
②溴水,现象是______________________________________________________。
(3)有一组同学在实验时发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因_______________,验证方法_____________________________。
②原因_______________,验证方法_____________________________。
高一化学实验题简单题查看答案及解析
-
某研究性学习小组通过下列反应原理制备SO2并进行性质探究。反应原理为:Na2SO3(固)+H2SO4(浓)= Na2SO4 + SO2↑+ H2O

(1)根据上述原理制备并收集干燥SO2的实验装置连接顺序为________________。(填接头序号)
(2)D中盛装的试剂为_________________。
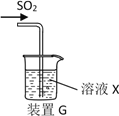
(3)甲同学用注射器吸取纯净的SO2并结合装置G进行SO2的性质实验,若X是Na2S溶液,其目的是检验SO2的_____________,可观察到的现象_________ 。
(4)实验1:乙同学将溶液X换为浓度均为0.1mol/L Fe(NO3)3和BaCl2的混合溶液(已经除去溶解氧),通入少量SO2后观察到烧杯产生白色沉淀,乙同学认为白色沉淀为BaSO4,为探究白色沉淀的成因,他继续进行如下实验验证:(已知:0.1mol/L Fe(NO3) 3的pH=2)
实验
操作
现象
结论和解释
2
将SO2通入0.1mol/L ____和BaCl2混合液
产生白色沉淀
Fe3+能氧化H2SO3
3
将SO2通入_______ 和 BaCl2混合液
产生白色沉淀
酸性条件NO3-能将H2SO3氧化为SO42-
高一化学实验题困难题查看答案及解析
-
某化学兴趣小组为探究SO2的性质,查阅相关资料知:实验室制取SO2气体的反应原理为Na2SO3 + H2SO4
Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
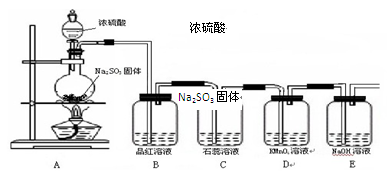
Na2SO3固体
请回答下列问题:
(1)盛装浓硫酸的仪器的名称是________。
(2)按上图连接好装置再________ ________(填操作名称),然后加入试剂并加热。
(3)实验过程中, 装置B、C中可观察到的实验现象分别是________、________。
(4)D中可观察到的现象是_______________,说明SO2具有________性。
(5)装置E的作用是________。
高一化学实验题中等难度题查看答案及解析
-
某同学用如图所示装置探究SO2的性质及其有关实验。
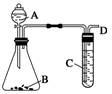
(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2气体,写出该反应的化学方程式:________
(2)分别将SO2气体通入下列溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是________。
②SO2通入氯水溶液,现象是__________,其反应的离子方程式为__________。
③过量SO2慢慢地通入澄清石灰水中,现象是__________。
④若C取双氧水,则通入SO2后,请大胆判断所得溶液是__________(填溶质的化学式),若该同学制备的SO2气体中混有CO2气体,产生杂质的原因可能是亚硫酸钠固体中混有__________。
高一化学实验题困难题查看答案及解析
-
某同学用如图所示装置探究SO2的性质及其有关实验。

(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2 气体,写出该反应的化学方程式________
(2)分别将SO2 气体通入下列C 溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是_______,继续通入过量SO2 气体,现象是____________
②SO2 通入紫色KMnO4溶液,现象是_______,其反应的离子方程式为__________
③过量SO2慢慢地通入澄清石灰水中,现象是_________
④若C为双氧水,则通入SO2 后,请大胆判断所得溶液是_______(填溶质的化学式),若该同学制备的SO2 气体中混有CO2 气体,产生杂质的原因可能是亚硫酸钠固体中混有______________
高一化学实验题中等难度题查看答案及解析
-
许多非金属元素是重要的化工原料,某学习小组对某些非金属的化合物性质和制备进行如下实验探究:
Ⅰ.探究实验一:将一定量的浓H2SO4与足量Zn置于装置A中充分反应,对反应后的气体X进行气体成分分析
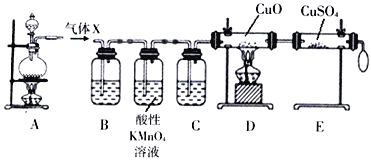
回答下列问题:
(1)气体X可能是________。(水蒸气除外)
(2)酸性高锰酸钾溶液的作用是________
(3)D、E装置用于证明气体X中的另一种组分,按照D、E装置顺序观察到的实验现象分别是____、______。
Ⅱ.下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备及A中酒精灯已略)。
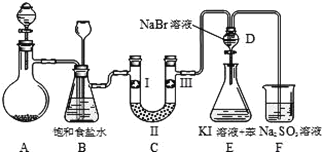
(1)实验室制氯气的离子方程式为________。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是_______(填编号)。
编号
a
b
c
d
Ⅰ
干燥的有色布条
干燥的有色布条
湿润的有色布条
湿润的有色布条
Ⅱ
碱石灰
硅胶
浓硫酸
无水氯化钙
Ⅲ
湿润的有色布条
湿润的有色布条
干燥的有色布条
干燥的有色布条
高一化学实验题中等难度题查看答案及解析
-
某研究性学习小组请你参与“研究铁与水蒸气反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水蒸气反应”的实验。
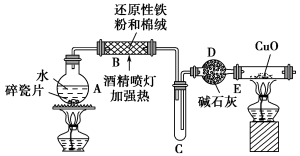
(1)硬质玻璃管B中发生反应的化学方程式为____________________。
(2)反应前A中投放碎瓷片的目的是______________________。
(3)装置E中的现象是___________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变红色,推断硬质玻璃管B中固体物质的成分为________。
①一定有Fe3O4 ②一定有Fe ③只有Fe3O4 ④只有Fe
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
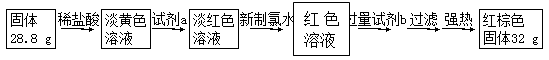
(6)试剂b的化学式是________。
(7)计算反应后B装置中铁元素的质量分数为________。
高一化学实验题中等难度题查看答案及解析
-
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计右图所示装置进行“铁与水反应”的实验。
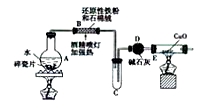
(1)硬质试管中发生反应的化学方程式为 。
(2)反应前A中投放碎瓷片的目的是 。
(3)装置E中的现象是 。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质试管B冷却后,取少许其中的固体物质溶于 后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同) 。若溶液未变红色,推断硬质玻璃管B中固体物质的成分
①一定有Fe3O4,可能有Fe ②Fe3O4和Fe ③只有Fe3O4 ;④只有Fe。
(6)另一份用___ (填仪器名称)加入 ,可以证明溶液中存在Fe2+。
【探究三】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
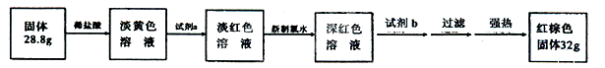
(7)试剂b的化学式是 ____。
(8)计算反应后B装置中铁元素的质量分数为 。
高一化学实验题简单题查看答案及解析