-
下列指定反应的离子方程式正确的是
A.用KIO3溶液氧化酸性溶液中的KI:5I-+ IO3- + 3H2O = 3I2 + 6OH-
B.醋酸溶液与水垢中的CaCO3反应:CaCO3 + 2H+ = Ca2+ + H2O + CO2
C.Cu溶于稀HNO3:Cu + 2H+ + NO3- = Cu2+ + NO2↑+ H2O
D.Ca(HCO3)2溶液与足量NaOH溶液反应:2HCO3- + Ca2+ + 2OH-= CaCO3↓ + CO32-+ 2H2O
-
下列反应的离子方程式书写正确的是
A.用KIO3氧化酸性溶液中的KI:5I﹣+ IO3﹣+ 3H2O = 3I2 + 6OH-
B.以石墨作电极电解AlCl 3溶液:2Cl-+2H2O 2OH- + H2 ↑+ Cl2↑
2OH- + H2 ↑+ Cl2↑
C.FeSO4溶液与稀H2SO4、双氧水混合:2Fe2++H2O2+2H+ =2Fe3++2H2O
D.NaHSO4溶液与足量Ba(OH)2溶液至混合:2H+ + SO42- + Ba2++ 2OH- =BaSO4↓+ 2H2O
-
某同学取海带灰加蒸馏水煮沸2~3 min,冷却,过滤,获得含I−的溶液,并设计以下实验方案,从中提取I2。

已知:3I2 + 6NaOH == 5NaI + NaIO3 + 3H2O
(1)试剂a的作用是________。
(2)试剂b应选择________(填序号)。
A.CCl4 B.苯 C.酒精 D.植物油
(3)操作1的名称是________。
(4)反应3的离子方程式是________。
-
卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O
② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O
④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
| 步骤 | 现象 |
| ⅰ. 向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液的滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
| ⅱ. 继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
请回答:
(1)步骤ⅰ开始时发生的反应如资料①所示,溶液中I-完全被氧化时转移 mol e-,该反应中硫酸表现出的化学性质是 。
(2)上述资料中的反应 (填序号)可表示步骤ⅱ中的反应,通过该反应 (填“能”或“不能”)说明碘的非金属性强于溴,原因是 。
(3)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(4)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。

-
NA为阿伏加德罗常数,下列叙述正确的是( )
A.反应5I—+IO3—+6H+ = 3I2 +3H2O生成3mol碘单质转移电子数为5NA
B.1 mol Na2O2溶于水作用时转移的电子数为2NA
C.在标准状况下,含NA个氦原子的氦气所含的分子数是0.5 NA
D.在7.8 g Na2O2晶体中阳离子与阴离子总数为0.4 NA
-
NA为阿伏加德罗常数,下列叙述正确的是
A.标况下,2.8 L丙烷中含有的极性共价键数为NA
B.在反应KIO3 + 6HI = KI + 3I2 + 3H2O 中,每生成3 mol I2转移的电子数为6 NA
C.已知CH3COONH4溶液的PH=7,则1L 0.1mol/L的CH3COONH4溶液中,CH3COO- 数为0.1NA
D.39g Na2O2和Al(OH)3的混合物中阴、阳离子的总数为2NA
-
检验溶液中是否有S2O32﹣的一种方法:取待测液,向其中逐滴滴加硝酸银溶液,如果有S2O32﹣,会发生如下反应:
Ag++2S2O32﹣→[Ag(S2O3)2]3﹣;
3Ag++[Ag(S2O3)2]3﹣→2Ag2S2O3↓(白色);
Ag2S2O3+H2O→Ag2S↓(黑色)+H2SO4;
下列叙述正确的是( )
A.此实验可在酸性溶液中进行 B.此实验可在碱性溶液中进行
C.此实验只能在中性溶液中进行 D.硝酸银溶液必须过量
-
为检验某加碘食盐中是否含有KIO3,取相同食盐样品进行下表所示实验:

(已知:KIO3 + 5KI + 3H2SO4= 3I2 + 3K2SO4 + 3H2O)
下列说法中正确的是
A. 仅由实验①就能证明食盐样品中存在KIO3
B. 实验②中发生反应的离子方程式为4I-+ O2 + 4H+= 2I2 + 2H2O
C. 实验③能证明食盐样品中不存在KIO3
D. 以上实验说明离子的还原性:I- > Fe2+
-
为检验某加碘食盐中是否含有KIO3,取相同食盐样品进行下表所示实验:
(已知:KIO3 + 5KI + 3H2SO4 3I2 + 3K2SO4 + 3H2O)
3I2 + 3K2SO4 + 3H2O)

下列说法中正确的是
A. 仅由实验①就能证明食盐样品中存在KIO3
B. 实验②中发生反应的离子方程式为4I-+ O2 + 4H+  2I2 + 2H2O
2I2 + 2H2O
C. 实验③能证明食盐样品中不存在KIO3
D. 以上实验说明离子的还原性:I- > Fe2+
-
(16分)已知在溶液中IO3-与I-、I2与S2O32-有如下反应:
IO3-+5I-+6H+=3I2+3H2O I2+2S2O32-=2I-+S4O62-
某课外活动小组为测定混有MgCl2的食用加碘盐中所含MgCl2、KIO3的含量,按下图所示实验步骤进行实验.
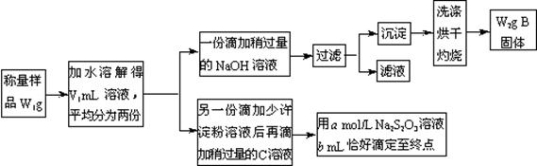
请回答下列问题:
(1)写出B和C的化学式:B________________,C________________。
(2)加入NaOH溶液必须稍过量的原因是________________________________。
(3)过滤用到的玻璃仪器有__________________________________________。
(4)该滴定实验所需仪器有下列中的_____________(填序号)
A.酸式滴定管
B.碱式滴定管
C.量筒
D.锥形瓶
E.铁架台
F.滴定管夹
G.烧杯
H.白纸
I.胶头滴管
J.漏斗
滴定时,判断滴定达到终点的现象是____________________________。
(5)MgCl2的质量分数是__________________________________________,KIO3的质量分数是_______________________________(列出计算式,可不化简)。
(6)使所测MgCl2的质量分数可能偏高的操作是_____________(填写字母)
A.过滤后未洗涤所得沉淀,直接烘干灼烧
B.在敞口容器中用托盘天平称量样品时,操作时间过长
C.沉淀灼烧不彻底




