-
已知X、Y、Z、M、W、R是前四周期中的六种元素。X元素原子形成的离子是一个质子,Y原子的价电子构型为2s22p2,Z的单质在常温下是无色气体且Z原子的单电子个数是同周期元素原子中最多的。
(1) 24R原子最外层的电子排布图是________,ZO3-的空间构型是________;
(2) Z、M、W原子序数依次增大,三种元素的第一电离能由大到小的顺序是________;Y、Z、W三种元素的电负性由大到小的顺序是________。(填元素符号)
(3) Ne与Wn-的电子数相同,W所在族的各元素的氢化物的水溶液均显酸性,则该族元素的氢化物中沸点最低的是________。(填化学式)
(4)ZX4W在物质中,各种粒子间的相互作用力包括________。(填字母编号)
A.非极性共价键 B.极性共价键 C.配位键 D.离子键 E.氢键
高三化学推断题困难题查看答案及解析
-
(8分)已知X、Y、Z、M、W、R是前四周期中的六种元素。X元素原子形成的离子是一个质子,Y原子的价电子构型为2s22p2,Z的单质在常温下是无色气体且Z原子的单电子个数是同周期元素原子中最多的。
(1) 24R原子最外层的电子排布图是________,ZO3-的空间构型是________;
(2) Z、M、W原子序数依次增大,三种元素的第一电离能由大到小的顺序是________;Y、Z、W三种元素的电负性由大到小的顺序是________。(填元素符号)
(3) Ne与Wn-的电子数相同,W所在族的各元素的氢化物的水溶液均显酸性,则该族元素的氢化物中沸点最低的是________。(填化学式)
(4)ZX4W在物质中,各种粒子间的相互作用力包括________。(填字母编号)
A.非极性共价键 B.极性共价键 C.配位键 D.离子键 E.氢键
高三化学填空题中等难度题查看答案及解析
-
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
元素
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一电离能至第四电离能分别是:I1=578kJ·mol-1,I2=1817kJ·mol-1,I3=2745kJ·mol-1,I4=11575kJ·mol-1
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1)TY2是一种常用的溶剂,是__(填“极性分子”或“非极性分子”),分子中存在 ___个
键。W的最简单氢化物容易液化,理由是___。
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为__。
(3)基态Y原子中,电子占据的最高能层符号为__;该能层具有的原子轨道数为___、电子数为___,Y、氧、W元素的电负性由大到小的顺序为___(用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g·cm-3,则晶胞边长为___;
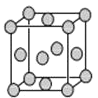
ZYO4常作电镀液,其中YO42-的空间构型是__,其中Y原子的杂化轨道类型是___,Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸
不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是__。
A.O2是氧化剂 B.HO2是氧化产物
C.HO2在碱中能稳定存在 D.1molZ参加反应有1mol电子发生转移
高三化学推断题中等难度题查看答案及解析
-
周期表中前四周期中的六种元素A、B、C、D、E、F原子序数依次增大,已知A原子2p轨道有3个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体熔点在同周期形成的单质中是最高的;F2+核外各电子层电子均已充满。
根据以上信息回答下列问题:
(1)写出D原子核外电子排布式:____________________________________________。
(2)A、B、C、D的第一电离能由小到大的顺序为________________________________(用元素符号表示)。
(3)B的氯化物的熔点比D的氯化物的熔点________(填“高”或“低”);理由是_______________________________________________________。
(4)E的最高价氧化物分子的空间构型是________,是________(填“极性”或“非极性”)分子。
(5)E、F形成的某种化合物有如图所示的晶体结构:该化合物化学式为________;E原子配位数为________________________________________________。
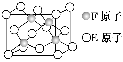
高三化学填空题中等难度题查看答案及解析
-
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元索
相关信息
T
T元素可形成自然界硬度最大的单质
W
W与T同周期,核外有一个未成对电子
X
X原子的第一离能至第四电离能分别I1=578 kJ/mol; I2= l817 kJ/mol;
I3=2745 kJ/mol;I4=11575kJ/mol
Y
常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质
Z
Z的一种同位素的质量数为63,中子数为34
(1)TY2的结构式是__________是__________(填“极性分子”或“非极性分子”),1mol该分子中存在________个σ键。
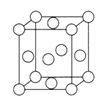
(2)基态Y原子中,电子占据的最高能层符号为__________,该能层具有的原子轨道数为_____________、电子数为_________。Y、氧、W元素的电负性由大到小的顺序为_________(用元素符号作答)。
(3)已知Z的晶胞结构如图所示,又知Z的密度为a g/cm3,则Z 的半径为___________pm;ZYO4常作电镀液,其中YO42-的等电子体是__________,其中Y原子的杂化轨道类型是___________。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z +HCl+O2=ZC1+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是___________。
A.O2是氧化剂 B.HO2是氧化产物
C.HO2在碱中能稳定存在 D.1 mol Z参加反应有1 mol电子发生转移
高三化学简答题极难题查看答案及解析
-
(1 4分)X.Y、Z、W是元素周期表前四周期中常见的元素,原子序数依次增大,其相关信息如下表
元素
相关信息
X
由X形成的单质是最清洁的能源
Y
基态原子核外p能级电子总数比s能级少一个
Z
由Z形成的多种单质,其中之一是地球生物的“保护伞”
W
含量位居地壳中金属元素的第二位
回答下列问题:
(1)Z位于元素周期表第 周期第 族,W的基态原子核外电子排布式为 。
(2)Y的第一电离能比Z (填“大”或者“小”);由X、Y、Z三种元素组成的一种盐的化学式为 。
(3)写出W元素的单质与X2Z在高温条件下反应的化学方程式 。
(4)在500℃、30MPa下,将1mol X2 与足量的Y2 置于密闭容器中充分反应生成YX3,当X2 的转化率为25%时,放出热量为7.7kJ,则该反应的热化学方程式为: 。
高三化学填空题中等难度题查看答案及解析
-
下列用原子最外层电子排布式表示的各对元素中,能形成离子化合物的是( )
A. 3s23p3和2S22p2 B. 3s2和4S24p5
C. 1s1和3s23p4 D. 2S22p2和2S22p4
高三化学选择题简单题查看答案及解析
-
(题文)X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是( )
A. X、Z、W三元素形成的化合物为共价化合物
B. 五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X
C. 化合物YW2、ZW2都是酸性氧化物
D. 用M单质作阳极,石墨作阴极电解NaHCO3溶液,在阳极区出现白色沉淀
高三化学单选题简单题查看答案及解析
-
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M元素的原子是短周期中原子半径最大的。下列说法正确的是
A. X、Z、W三元素形成的化合物都是共价化合物
B. 简单离子的半径从大到小的顺序是:M>Y>Z>W
C. 氢化物的稳定性强弱顺序为:Y>Z>W
D. M2W2既含有离子键,也含有非极性键
高三化学单选题中等难度题查看答案及解析
-
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是( )
A. X、Z、W三元素形成的化合物为共价化合物
B. 五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X
C. 化合物YW2、ZW2都是酸性氧化物
D. 用M单质作阳极,石墨作阴极电解NaHCO3溶液,在阳极区出现白色沉淀
高三化学单选题简单题查看答案及解析