-
铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛。铁还有很多重要的化合物及其化学反应。如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反应的平衡常数表达式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
则△H=_______。
(3)在t0C时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe
H2O(g)
Fe3O4
H2
甲/mol
1.0
1.0
1.0
1.0
乙/mol
1.0
1.5
1.0
1.0
①甲容器中H2O的平衡转化率为_______ (结果保留一位小数)。
②下列说法正确的是_______ (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
Fe
H2O(g)
Fe3O4
H2
起始/mol
3.0
4.0
0
0
平衡/mol
m
n
p
q
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
Fe
H2O(g)
Fe3O4
H2
A/mol
3.0
4.0
0
0
B/mol
0
0
1
4
C/mol
m
n
p
q
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是
________(用A、B、C表示)。
(5)已知Fe(OH)3的Ksp=2.79×10-39,而FeCl3溶液总是显示较强的酸性,若某FeCl3溶液的pH为3,则该溶液中c(Fe3+)=________mol • L-1 (结果保留3位有效数字)
高三化学填空题困难题查看答案及解析
-
(10分)氢是一种重要的非金属元素。氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)工业上一般采用CO和H2反应合成可再生能源甲醇。反应如下:
CO(g) + 2H2(g)
CH3OH(g) ΔH= -90.1KJ·mol-1
在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol·L-1)变化如下表所示:(前6min没有改变条件)
2min
4min
6min
8min
…
CO
0.07
0.06
0.06
0.05
…
H2
x
0.12
0.12
0.20
…
CH3OH
0.03
0.04
0.04
0.05
…
①x= 。
②250℃时该反应的平衡常数K的计算式为: (不必化简)。
③若6min~8min只改变了某一条件,所改变的具体条件是 。
④第8min时,该反应是不是达到平衡状态 。(填“是”或“不是”)
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2。已知:
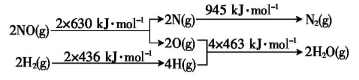
H2还原NO生成氮气和水蒸气的热化学方程式是 。
高三化学填空题中等难度题查看答案及解析
-
乙酸乙酯是重要的工业溶剂和香料,广泛用于化纤、橡胶、食品工业等。
在标准状态时,由元素最稳定的单质生成1mol纯化合物时的反应热称为该化合物的标准摩尔生成。请写出标准状态下,乙酸和乙醇反应的热化学方程式为___________。
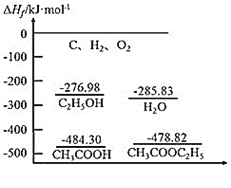
取等物质的量的乙酸、乙醇在TK下密闭容器中发生液相
反应物和生成物均为液体
酯化反应,达到平衡,乙酸的转化率为
,则该温度下用物质的量分数表示的平衡常数
________;
注:对于可逆反应:
达到化学平衡时,
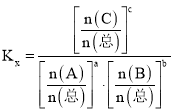 )。而相同条件下实验室采用回流并分离出水的方式制备乙酸乙酯时,乙酸转化率可以高达
)。而相同条件下实验室采用回流并分离出水的方式制备乙酸乙酯时,乙酸转化率可以高达,可能的原因是__________。
若将乙醇与乙酸在催化剂作用下发生气相
反应物和生成物均为气体
酯化反应,其平衡常数与温度关系为:
式中T为温度,单位为
,则气相酯化反应为________
填“吸热”或“放热”
反应。
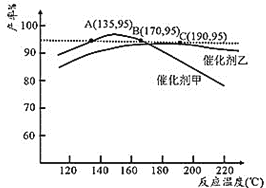
乙酸和乙醇酯化反应在甲、乙两种催化剂的作用下,在相同时间内乙酸乙酯的产率随温度变化如图所示。由图可知,产率为
时,应该选择催化剂和温度分别是________、________;使用催化剂乙时,当温度高于
,随温度升高,乙酸乙酯产率下降的原因________________________。
为了保护环境,
的排放必须控制。化学工作者尝试各种方法将燃煤产生的二氧化碳回收利用,以达到低碳排放的目的。如图是通过人工光合作用,以
和
为原料制备乙醇
和
的原理示意图:
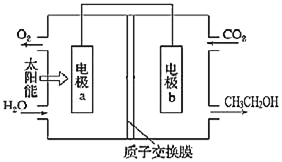
判断
迁移的方向________
选填“从左向右”、“从右向左”
。
写出电极b的电极反应式:________________。
高三化学综合题中等难度题查看答案及解析
-
氢是一种重要的非金属元素。氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)NaH是一种生氢剂,NaH与H2O反应放出H2。NaH含有的化学键为 (填“离子键”或“共价键”),NaH与H2O反应的化学方程式为 。
(2)金属-有机框架物(MOFs)储氢材料是由金属氧化物团簇通过有机高分子链组装形成的晶态材料。MOFs储氢材料比表面积大,空隙率高,储氢容量大,其储氢和放氢的原理可表示为
MOFs(s)+nH2(g)
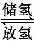 (H2)nMOFs(s) ΔH<0,则储氢时的适宜条件为 (填字母)。
(H2)nMOFs(s) ΔH<0,则储氢时的适宜条件为 (填字母)。A.低温低压 B.低温高压 C.高温低压 D.高温高压
(3)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2。已知:
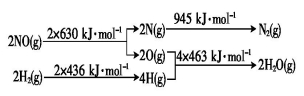
则:H2还原NO生成氮气和水蒸气的热化学方程式是 。
(4)一定条件下,用H2将二氧化碳转化为甲烷的反应如下:CO2(g)+4H2(g)
CH4(g)+2H2O(g),向一容积为2 L的恒容密闭容器中充入一定量的CO2和H2,在300 ℃时发生上述反应,10 min后达到平衡时各物质的浓度分别为:CO2:0.2 mol/L H2 :0.8 mol/L CH4 : 0.8 mol/L H2O:1.6 mol/L。
①0~10 min内v(H2)= 。
②300 ℃时上述反应的平衡常数K= 。
若200 ℃时该反应的平衡常数K = 64.8,则该反应的ΔH 0。(填“>”或“<”)
高三化学填空题困难题查看答案及解析
-
硼元素、钙元素、铜元素在化学中站有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为 ______。
② CaC2中C22-与O22+互为等电子体,1mol O22+中含有的
键数目为 ______。
③乙炔与氢氰酸反应可得丙烯睛(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是 ______,构成丙烯腈元素中第一电离能最大的是 ______。
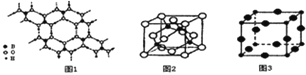
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢健相连(如上图1)则1molH3BO3的晶体中有 ______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为 ______。
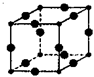
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
该晶体化学式为 ______。
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 ______ (填“离子”、“共价”)化合物。
(4)Cu3N的晶胞结构如上图3,N3-的配位数为 ______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为 ______g•cm-3(阿伏加德罗常数用NA表示)。
高三化学综合题中等难度题查看答案及解析
-
硼元素、钙元素、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用。
已知
与水反应生成乙炔。请回答下列问题:
将乙炔通入
溶液中生成
红棕色沉淀,
基态核外电子排布式为 ______ ,其在酸性溶液中不稳定,可发生歧化反应生成
和Cu,但CuO在高温下会分解成
,试从结构角度解释高温下CuO何会生成
:______。
中
与
互为等电子体,
中含有的
键数目为 ______ 。
乙炔与氢氰酸反应可得丙烯腈
丙烯腈分子中碳原子轨道杂化类型是 ______ ,构成丙烯腈元素中第一电离能最大的是 ______ 。
硼酸
是一种片层状结构的白色晶体,层内的
分子间通过氢键相连
如图
则
的晶体中有 ______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸
,它电离生成少量
和
,则
含有的化学键类型为 ______ 。

高三化学填空题中等难度题查看答案及解析
-
(16分)氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)NaH是一种生氢剂,NaH与H2O反应放出H2.NaH含有的化学键为________(填“离子键”或“共价键”),NaH与H2O反应的化学方程式为________________.
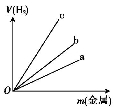
(2)写出实验室用锌与稀硫酸反应制取H2的离子方程式:_________.图中三根曲线表示锌、铝、铁分别与稀硫酸反应时金属质量与H2体积的关系,其中能表示铝的是________(填“a”“b”或“c”).
(3)金属-有机框架物(MOFs)储氢材料是由金属氧化物团簇通过有机高分子链组装形成的晶态材料.MOFs储氢材料比表面积大,空隙率高,储氢容量大,其储氢和放氢的原理可表示为MOFs(s)+nH2(g)
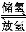 (H2)nMOFs(s),ΔH<0,则储氢时的适宜条件为________(填字母).
(H2)nMOFs(s),ΔH<0,则储氢时的适宜条件为________(填字母).A.低温低压 B.低温高压 C.高温低压 D.高温高压
(4)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2.
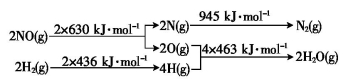
已知:H2还原NO生成氮气和水蒸气的热化学方程式是_________________________.
(5)一定条件下,用H2将二氧化碳转化为甲烷的反应如下:
CO2(g) + 4H2(g)
CH4(g) + 2H2O(g)
向一容积为2 L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,10 min后达到平衡时各物质的浓度分别为: CO2为0.2 mol·L-1, H2为0.8 mol·L-1, CH4为0.8 mol·L-1, H2O为1.6 mol·L-1.
①0~10 min内v(H2)=_______________.
②300℃时上述反应的平衡常数K=___________,若200℃时该反应的平衡常数K=64.8,则该反应的ΔH__________(填“>”或“<”)0.
高三化学填空题困难题查看答案及解析
-
(16分)硼元素、钙元索、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用。
(1)已知CaC2与水反应生成乙炔.请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl榕液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为 。其在酸性溶液中不跪定,可发生歧化反应生成Cu2十和Cu,但CuO在高温下会分解成Cu2O,
试从结构角度解释高温下CuO为何会生成Cu2O: 。
②CaC2中C22-与O22+互为等电子体.1molO22+中含有的π键数目为 。
③乙炔与氢氰酸反应可得丙烯睛(H2C=CH一C≡N)。丙烯腈分子中碳原子轨道杂化类型是 ,构成丙烯腈元素中第一电离能最大的是 (填元素符号)。
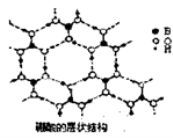
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢健相连(如上图〕.则1 mo1H3BO3的晶体中有 mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为
(3)Cu3N的晶胞结构如图,N3-的配位数为 。Cu+半径为a cm,N3-半径为bcm,Cu3N的密度为___ g/cm3,(阿伏加德罗常数用NA表示)
高三化学填空题极难题查看答案及解析
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。探究二氧化硫的制取和性质都有着非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:
该反应中被氧化的元素是__________(填元素符号)。当该反应转移5.50mol电子时,生成的二氧化硫在标准状况下的体积为________L。
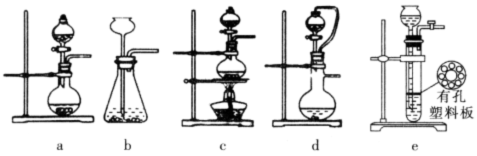
(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是_______(填写字母)。
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有4.0%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠_______g(保留一位小数)。
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。
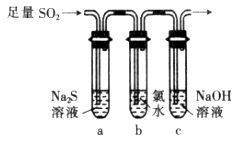
①能说明二氧化硫具有氧化性的实验现象为___________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______________。
高三化学实验题极难题查看答案及解析
-
(本题12分)
磷是重要的非金属元素。磷单质及其化合物在工业生产中有着广泛的应用。
次磷酸钠(NaH2PO2)可用于化学镀镍等等。
完成下列填空
(1).磷原子的最外层电子排布的轨道表示式为 ______ ;氧原子核外电子云有 种不同的伸展方向,其最外层有 种不同运动状态的电子。NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为 。
(2).写出与磷同周期的主族元素中,离子半径最小的元素,其最高价氧化物对应水化物的电离方程式 。
(3).磷酸二氢钠主要用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。其水溶液呈酸性的原因是__________________________________________________。(请用文字描述)
已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO。
(4).写出该反应的化学方程式__________________________。
(5).每消耗24.0g碳时,有 mol电子发生转移。反应所得混合气体,折算成标况下,其气体密度为 g/L。
高三化学填空题困难题查看答案及解析