-
CuCl2广泛应用于工业生产,溶于水形成绿色溶液。CuCl晶体呈白色,难溶于水, 露置于潮湿空气中易被氧化,实验室用下图所示的实验仪器及药品来制备纯净、千燥的氯气并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。
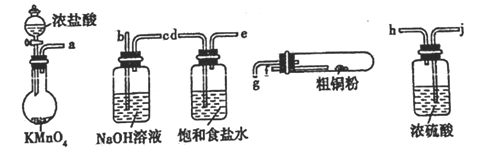
(1)完成上述实验,气流方向连接各仪器接口的顺序是a→______________________________________;反应时,圆底烧瓶中发生反应的离子方程式为_________。盛粗铜粉的试管中现象是________________________。
(2)实验完毕,取试管中的固体用盐酸溶解后,欲提纯氯化铜,可向溶解液中加入过量__________。(填物质化学式,己知:室温下Fe(OH)3)沉淀完全的pH为3.2)
(3)向制得的氯化铜溶液中通入SO2,加热一段时间即可制得CuCl,写出该反应的离子方式:________________________________。
(4)己知:i.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气
某同学利用如下图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成
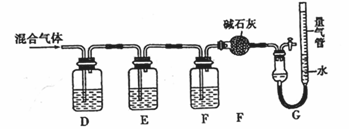
①D瓶测定的气体是_________________;
②E瓶中发生反应的离子方程式为__________________________________。
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意_____________________________。
-
CuCl2广泛应用于工业生产,溶于水形成绿色溶液。CuCl晶体呈白色,露置于潮湿空气中易被氧化,实验室用图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。

(1)完成上述实验,气流方向连接各仪器接口的顺序是________a→______、____→______、_____→______、 _________→________;反应时,盛粗铜粉的试管中现象是_______________。
(2)实验完毕,取试管中的固体有盐酸溶解后,欲提纯氯化铜,请简述实验方案:_________________。(室温,Fe(OH))3 沉淀完全的pH为3.2)
(3)向制得的氯化铜溶液中通入SO2,加热一段时间既可制得CuCl,写出该反应的离子方式:_______。
(4)已知:ⅰ.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ⅱ.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
某同学利用如图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成
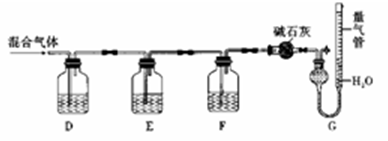
①D瓶测定__________;F洗气瓶中盛放的试剂是__________________。
②E瓶中发生反应的离子方程式为____________________。
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意__________。
-
氯化亚铜是重要的铜盐系列化工产品,广泛应用于石油化工、有机合成等行业。CuCl晶体呈白色,微溶于水,不溶于稀盐酸和乙醇,露置于潮湿空气中易水解氧化为绿色的[Cu 2(OH)3C1],见光易分解。某研究小组以CuCl2(含少量Fe2+)粗品为原料制取CuCl,设计的合成路线如下:
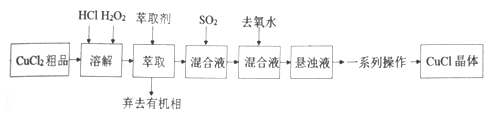
己知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮。
②CuCl在溶液中存在:CuCl(s)+2Cl-(aq) [CuCl3]2-(aq)。
[CuCl3]2-(aq)。
请回答:
(1)下列叙述正确的是__________。
A.CuCl2原料中含有的Fe2+等杂质经氧化、萃取几乎都在有机相中被除去
B.加入萃取剂后,混合物转移至分液漏斗中,塞上玻璃塞,如图用力振摇
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.用浓盐酸洗涤分液后的有机相时,需在分液漏斗中进行
(2)上述合成路线中,SO2通入混合液的实验装置如下图所示:
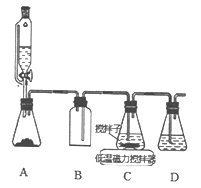
①装置D的作用是_______________。
②C中反应的离子方程式为_____________。
(3)上述合成路线中,向混合液中加入大量去氧水的目的是________________。
(4)上述合成路线中,一系列操作包括:抽滤、洗涤、干燥。干燥时应注意密封、____________。
(5)现称取l.200g产品,用硫酸酸化的硫酸铁溶解,并稀释成250mL。每次用移液管移取25.00mL溶液于锥形瓶中,用0.01000,mol·L-1KmnO4溶液滴定平均消耗24.00mL。
①用移液管吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为____________。
②产品中CuCl的纯度为__________(本实验条件下,Cl-难于被MnO4-氧化)。
-
氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,见光易分解,在潮湿空气中易被氧化,难溶于水。
(1)实验室保存新制CuCl晶体的方法是_________________。
(2)已知:Cu(s)+Cl2(g)=CuCl2(s) △H1=-218.8kJ/mol
2Cu(s)+O2(g)=2CuO(s) △H2=-310.6kJ/mol
2CuCl2(s)=2CuCl(s)+Cl2(g) △H3=+152.3kJ/mol
则反应4CuCl(s)+O2(g)=2CuCl2(s)+2CuO(s)的△H=____kJ/mol。
(3)利用CuCl难溶于水的性质,可以除去废水中的Cl-。向含Cl-的废水中同时加入Cu和CuSO4,溶液中平衡时相关离子浓度关系如图所示。[已知:pc(离子)=-lgc(离子)]

①除去废水中Cl-的离子方程式为_________________。
②Ksp(CuCl)=___________。
③已知:Cu+Cu2+ 2Cu+ K=7.6×10-7。通过计算说明上述除Cl-的反应能完全进行的原因______________________________。
2Cu+ K=7.6×10-7。通过计算说明上述除Cl-的反应能完全进行的原因______________________________。
(4)T℃时,用H2还原CuCl制备活性铜:H2(g)+2CuCl(s) 2Cu(s)+2HCl(g),达到平衡时,H2的转化率(
2Cu(s)+2HCl(g),达到平衡时,H2的转化率( )为80%。反应速率v=v正-v逆=
)为80%。反应速率v=v正-v逆= ,k正、k逆分别为正、逆反应速率常数,x为气体的物质的量分数。当
,k正、k逆分别为正、逆反应速率常数,x为气体的物质的量分数。当 =60%时,
=60%时, =________(保留1位小数)。
=________(保留1位小数)。
(5)CuCl溶于浓氨水的反应原理为CuCl+2NH3·H2O [Cu(NH3)2]-+2H2O+Cl-,该反应控制温度为70~80℃,其原因是_______________________。
[Cu(NH3)2]-+2H2O+Cl-,该反应控制温度为70~80℃,其原因是_______________________。
-
氯化亚铜 是有机合成中应用广泛的催化剂。它微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化,但在干燥的空气中稳定,见光会分解。实验室制备CuCl的过程如下:
是有机合成中应用广泛的催化剂。它微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化,但在干燥的空气中稳定,见光会分解。实验室制备CuCl的过程如下:
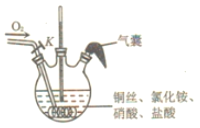
Ⅰ、检査图装置气密性,依次向三颈瓶中加入铜丝、 、
、 、HCl,关闭K;
、HCl,关闭K;
Ⅱ、加热至 时停止加热,铜丝表面产生无色气泡,液面上方气体逐渐变为红棕色,气囊鼓起;
时停止加热,铜丝表面产生无色气泡,液面上方气体逐渐变为红棕色,气囊鼓起;
Ⅲ、打开K,通入 ,待气囊变瘪、瓶内红棕色气体消失时关闭K,冷却至室温,制
,待气囊变瘪、瓶内红棕色气体消失时关闭K,冷却至室温,制
Ⅳ、将液体转移至烧杯中用足量蒸馏水稀释,产生白色沉淀,过滤得CuCl粗品和滤液;
Ⅴ、粗品用 乙醇洗涤、烘干得CuCl。
乙醇洗涤、烘干得CuCl。
请回答下列问题:
⑴实验室中CuC1的保存方法是______
⑵通入 的目的是______,为便于观察和控制产生
的目的是______,为便于观察和控制产生 的速率,制备
的速率,制备 的装置最好选用______
的装置最好选用______ 填字母
填字母
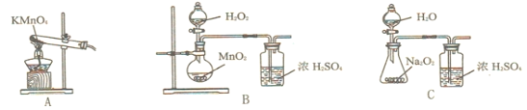
⑶①三颈瓶中生成 的总反应的离子方程式为______
的总反应的离子方程式为______
②步骤Ⅳ中产生白色沉淀的化学方程式为______
⑷步骤V中洗涤时试剂选用 乙醇的原因是______
乙醇的原因是______
⑸ 纯度测定:称取样品
纯度测定:称取样品 置于预先放入玻璃珠30粒和10mL过量的
置于预先放入玻璃珠30粒和10mL过量的 溶液的锥形瓶中,不断摇动;待样品溶解后,加水50mL和指示剂2滴;立即用
溶液的锥形瓶中,不断摇动;待样品溶解后,加水50mL和指示剂2滴;立即用 硫酸铈标准溶液滴定至终点并记录读数,再重复实验两次,测得数据如表所示。(已知:
硫酸铈标准溶液滴定至终点并记录读数,再重复实验两次,测得数据如表所示。(已知: ,
, )
)
 玻璃珠的作用______
玻璃珠的作用______
 的纯度为______
的纯度为______ 保留三位有效数字
保留三位有效数字 。
。
-
CuCl 晶体微溶于水和稀硫酸,不溶于乙醇,但易溶于浓盐酸和氯化铵溶液,发生的反应为:CuCl+Cl- CuC12,且其见光易分解,露置于潮湿空气中易被氧化。回答下列问题:
CuC12,且其见光易分解,露置于潮湿空气中易被氧化。回答下列问题:
(1)实验室保存新制CuCl 晶体的方法是__________。
(2)向硫酸铜溶液中加入亚硫酸铵和氯化铵,会发生反应生成CuCl。
①该反应的离子方程式为_____________。
②(NH4)2SO3 要适当过量,目的为保证Cu2+的还原速率、_____________。
③已知Cu2+ 的沉淀率与NH4Cl、CuSO4的物质的量之比[n(NH4Cl)/n(CuSO4)]的关系如图甲所示,当氯化铵用量增加到一定程度后,Cu2+的沉淀率减小,原因是_______________。

(3)已知:CuCl 固体、CuOH 固体分别为白色和橙黄色,且Ksp(CuCl)= 1.2×10-6,Ksp(CuOH)=1.2×10-14。用铜电极电解饱和食盐水的装置如图乙所示,阳极的电极反应式为Cu-e-+Cl -=CuCl。则实验过程中的实验现象为_________________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl是白色固体,难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以硫化铜精矿为原料生产CuCl的工艺过程如下:
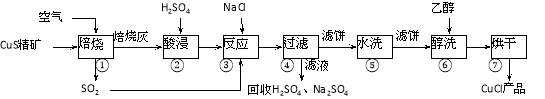
回答下列问题:
(1)CuS精矿经250 ℃低温焙烧后生成CuO,步骤②中主要反应的离子方程式是 。
(2)步骤③先加NaCl、通入SO2时无沉淀,加水稀释就产生大量白色沉淀,其原因是 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_______(写名称);步骤⑥醇洗的作用是 。
(4)已知25℃,101 kPa时:S(s)+O2(g)==SO2(g) ∆H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) ∆H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) ∆H=-53.1 kJ/mol
步骤①中CuS与O2反应的热化学方程式是 。
(5)CuS晶胞结构如图所示,其中含有硫原子的数目是 。
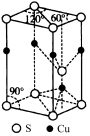
(6)假设上述①~③步反应完全转化,④~⑦步操作共损失产品3.5%,反应生成的硫酸全部被循环利用,则生产100 kg 96.5%的CuCl(Mr=99.0)产品,除循环利用之外,需要处理的尾气中含SO2 m3(标准状况)。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,在潮湿空气中易水解氧筑化,且在氯离子浓度较大的体系中存在CuCl+Cl-=[CuCl2]-。工业上用低品铜矿(主要含CuS、Cu2S、FeO等)制备CuCl的一种工艺流程如下:
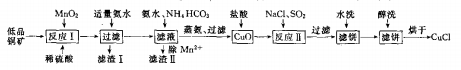
回答下面问题:
(1)反应I中被氧化的元素有_________。(填元素符号)
(2)滤渣II的成分主要为MnCO3,写出除Mn2+的离于方程式_________。
(3)写出反应II中发生反应的离子方程式_________。
(4)在进行反应II时,通入的SO2一般都要适当过量,目的是_________。
(5)滤饼进行醇洗的目的是_________。
(6)在进行反应II时,当氯化钠用量增加到一定程度后氯化亚铜的沉淀率减小,原因是_________。
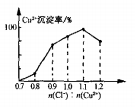
(7)Cu2+的沉淀率是指转化为CuCl的n(Cu2+)占总的n(Cu2+)的百分比。在一定条件下Cu2+沉淀率与沉淀前的Cl-、Cu2+的物质的量之比[n(Cl-): n(Cu2+)]的关系如下图所示。CuCl+Cl- [CuCl2]-的平衡常数K=6.5×10-2,则该条件下Cu2+的最大沉淀率为_________。(保留两位小数)。
[CuCl2]-的平衡常数K=6.5×10-2,则该条件下Cu2+的最大沉淀率为_________。(保留两位小数)。
-
CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s) + 3HCl(aq)  H3CuCl4(aq)。
H3CuCl4(aq)。
(1)实验室用下图所示装置制取CuCl,反应原理为:
2Cu2+ + SO2 + 8Cl− + 2H2O=2CuCl43− + SO42− + 4H+
CuCl43−(aq) CuCl(s) + 3Cl−(aq)
CuCl(s) + 3Cl−(aq)

① 装置C的作用是 。
② 装置B中反应结束后,取出混合物进行如下图所示操作,得到CuCl晶体。

操作ⅱ的主要目的是 ;操作ⅳ中宜选用的试剂是 。
③实验室保存新制CuCl晶体的方法是 。
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成。

已知:i. CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O。
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
① D、F洗气瓶中宜盛放的试剂分别是 、 。
② 写出保险粉和KOH的混合溶液吸收O2的离子方程式: 。
-
CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s) + 3HCl(aq)  H3CuCl4(aq)。
H3CuCl4(aq)。
(1)实验室用下图所示装置制取CuCl,反应原理为:
2Cu2+ + SO2 + 8Cl− + 2H2O=2CuCl43− + SO42− + 4H+
CuCl43−(aq) CuCl(s) + 3Cl−(aq)
CuCl(s) + 3Cl−(aq)

① 装置C的作用是 。
② 装置B中反应结束后,取出混合物进行如下图所示操作,得到CuCl晶体。

操作ⅱ的主要目的是 ;操作ⅳ中宜选用的试剂是 。
③实验室保存新制CuCl晶体的方法是 。
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成。

已知:i. CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O。
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
① D、F洗气瓶中宜盛放的试剂分别是 、 。
② 写出保险粉和KOH的混合溶液吸收O2的离子方程式: 。



















