-
2013年诺贝尔化学奖授予三位美国科学家,以表彰他们在开发多尺度复杂化学系统模型方面所做的贡献。可以用量子化学计算小区间内(如光合作用叶绿体光反应时酶中、生物固氮时固氮酶中)的化学反应。
(1)固氮酶有由铁蛋白和钼铁蛋白两种,它们不仅能够催化N2还原成NH3以外,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有 (不定项选择)。
a.C2H2、C2H4都是非极性分子
b.碳负离子CH3-呈三角锥形
c.NO+电子式为

d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极也可人工合成的二价钒(V)固氮酶(结构如下图)。
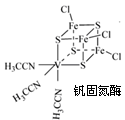
①V2+基态时核外电子排布式为 。
②钒固氮酶钒的配位原子有 (写元素符号)。
③熔融空气电池钒硼晶体晶胞结构如下图所示,该晶胞中含有钒原子数目为 。
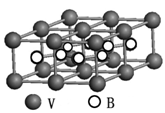
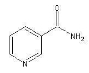
(3)烟酰胺(结构式如图)可用于合成光合辅酶NADPH ,烟酰胺分子中氮原子的杂化轨道类型有 ,1mol该分子中含σ键数目为 。
-
2013年诺贝尔化学奖授予美国科学家马丁·卡普拉斯、迈克尔·莱维特、阿里耶·瓦谢勒,以表彰他们“在开发多尺度复杂化学系统模型方面所做的贡献”。这种用电脑取代木棒作试验模型,催生了现代化学研究手段的一次新飞跃。下列不属于现代化学对物质结构进行研究的手段的是( )
A.X射线 B.天平 C.质谱 D.核磁共振
-
2013年诺贝尔化学奖授予美国科学家马丁·卡普拉斯、迈克尔·莱维特、阿里耶·瓦谢勒,以表彰他们“在开发多尺度复杂化学系统模型方面所做的贡献”。这种用电脑取代木棒作试验模型,催生了现代化学研究手段的一次新飞跃。下列不属于现代化学对物质结构进行研究的手段的是
A.X射线 B.天平 C.质谱 D.核磁共振
-
2013年诺贝尔化学奖授予美国科学家马丁·卡普拉斯、迈克尔·莱维特、阿里耶·瓦谢勒,以表彰他们“在开发多尺度复杂化学系统模型方面所做的贡献”。这种用电脑取代木棒作试验模型,催生了现代化学研究手段的一次新飞跃。下列不属于现代化学对物质结构进行研究的手段的是( )
A.X射线 B.天平 C.质谱 D.核磁共振
-
2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁•沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献.蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法.其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应
式为:2(-NH2)+H2SO4+2H+ ______.
______.
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7.
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量.
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为______.
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石.
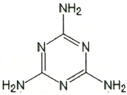
①三聚氰胺的结构如图所示,其化学式为______,含氮量(氮元素的质量分数)为______;
②下列关于三聚氰胺的说法中,正确的有______;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入______g的三聚氰胺就可使奶粉“达标”.
-
2005年10月5日,瑞典皇家科学院将本年度诺贝尔化学奖授予法国化学家伊夫·肖万和两位美国化学家罗伯特·格拉布和理查德·施罗克,以表彰他们在烯烃复分解反应研究和应用方面做出的卓越贡献。



伊夫·肖万 罗伯特·格拉布 理查德·施罗克
烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——2-丁烯和乙烯:

现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
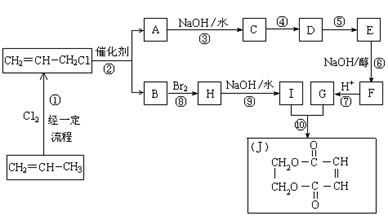
请按要求填空:
(1)写出下列反应的反应类型:
③:________,⑥:________,⑧:________。
(2)反应②的化学方程式是:。
(3)反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是;物质E的结构简式是________。
(4)反应⑩的化学方程式是________。
-
2019年度诺贝尔化学奖授予美国得州大学奥斯汀分校JohnB.Goodenough教授等人,以表彰其在锂离子电池的发展方面作出的突出贡献。研究表明:Li-Cu4O(PO4)2电池的正极的活性物质Cu4O(PO4)2制备的原理为:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O。请回答:
(1)在周期表中,与Li的化学性质最相似的邻族元素在周期表中位置是__。
(2)Cu4O(PO4)2中Cu2+基态电子排布式为__,PO43-的空间构型是___。
(3)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则[Cu(CN)4]2-中含有的σ键与π键的数目比为__。
(4)(NH4)2SO4中电负性最大的元素是__。所含化学键的类型有__。
(5)冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如图:
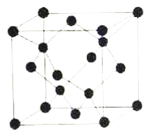
①每个冰晶胞平均占有__个水分子,冰的熔点远低于金刚石熔点的原因是__。
②在气相中NH3易与H2O通过氢键以水合物形式存在。试写出水合物NH3·H2O的结构式:__。
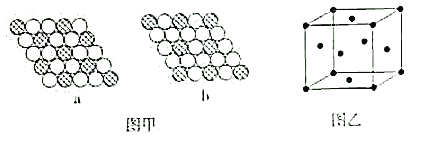
(6)如图甲所示为二维平面晶体示意图。其中表示CuCl2的晶体结构的是___(填“a”或“b”)。金属铜的晶胞如图乙所示,铜原子的配位数是__。若此晶胞立方体的边长为apm,金属铜的密度为ρg·cm-3,则阿伏加德罗常数可表示为___mol-1(用含a、ρ的代数式表示)。
-
2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
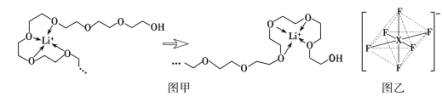
①聚乙二醇分子中,碳、氧的杂化类型分别是___、___。
②从化学键角度看,Li+迁移过程发生___(填“物理变化”或“化学变化”)。
③PF6中P的配位数为___。
④相同条件,Li+在___(填“LiPF6”或“LiAsF6”)中迁移较快,原因是___。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为___g·cm-3(列出计算表达式)。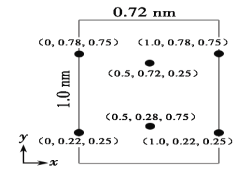
-
2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①聚乙二醇分子中,碳、氧的杂化类型分别是___、___。
②从化学键角度看,Li+迁移过程发生___(填“物理变化”或“化学变化”)。
③PF6中P的配位数为___。
④相同条件,Li+在___(填“LiPF6”或“LiAsF6”)中迁移较快,原因是___。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的品胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H2O晶体的密度为___g·cm-3(列出计算表达式)。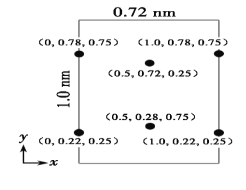
-
2019年10 月9 日诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。PC15、LiFePO4聚乙二醇、LiPF6、LiAsF6等可作制锂离子电池的材料。回答下列问题:
(l)Fe 的价层电子排布式为______________。Li、Fe、Cl、P 四种元素的第一电离能由大到小的顺序为___________________。
(2) PC13中心原子P 杂化类型是___________。将氨水和FeCl3 溶液混合后过滤出沉淀,再将沉淀溶入KOH 饱和溶液中,得到6 – 羟基配合物溶液,该配合物的化学式为_____。
(3)下列物质沸点最高的是_____________。
.A.正戊烷[ CH3 ( CH2)3CH3 ] B. l-丙醇 ( CH3 CH2 CH2OH)
C.乙二醇( HOCH2 CH2OH) . D. 丙醛( CH3CH2 CHO)
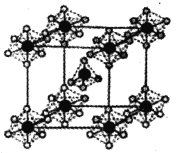
(4)熔融的PC15冷却后变为白色的离子晶体,晶体的晶胞如图所示,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子,写出阴、阳离子的化学式 __________;正四面体形阳离子中键角大于PC13 的键角原因为______________。
(5)电池工作时,Li+ 沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图所示(X=P、As)。
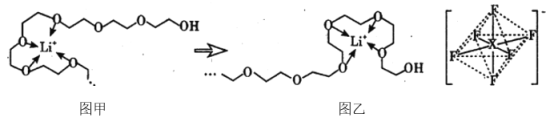
相同条件,Li+ 在LiAsF6 中比在LiPF6 中迁移较快,原因是 ________________。














