-
Fe、Zn、Al分别与盐酸反应(结果可用分数表示,不必化简):
(1)若盐酸足量,等物质的量的Fe、Zn、Al产生H2的质量之比为_____________。
(2)若盐酸足量,等质量的Fe、Zn、Al产生H2的质量之比为_________________, (3)若盐酸足量,等质量的Fe、Zn、Al产生H2在同温同压下的体积比为________。
高一化学填空题简单题查看答案及解析
-
(6分) Fe、Al分别与盐酸反应(结果可用分数表示):
(1)若盐酸足量,等物质的量的Fe、Al产生H2的质量之比为_____________。
(2)若盐酸足量,等质量的Fe、Al产生H2的质量之比为_________________。
(3)若盐酸足量,等质量的Fe、Al产生H2在同温同压下的体积比为_______。
高一化学填空题困难题查看答案及解析
-
将适量的下列物质,分别投入等质量、等溶质质量分数的稀盐酸中,恰好完全反应后,产生的气体全部逸出,所得溶液中的MgCl2的质量分数最小的是
A.Mg B.MgO C.Mg(OH)2 D. MgCO3
高一化学选择题简单题查看答案及解析
-
I.Fe、Al分别与盐酸反应(结果化简成最简单整数比,否则不给分):
(1)若盐酸足量,与等物质的量的Fe、Al反应产生H2的质量之比为_____________。
(2)若盐酸足量,与等质量的Fe、Al反应产生H2的质量之比为_________________。
(3)若盐酸不足,与足量Fe、Al反应产生H2在同温同压下的体积比为___________。
II.铝分别与盐酸、NaOH溶液反应(结果化简成最简单整数比,否则不给分):
(1)若盐酸、NaOH溶液足量,与等质量的两份铝反应产生H2的体积之比是_______。
(2)若盐酸、NaOH溶液等体积、等物质的量浓度,与足量的两份铝反应产生H2的体积之比是________。
(3)若HCl、NaOH溶液与足量的两份铝反应,二者产生的H2相等,则HCl和NaOH的物质的量之比是________。
(4)若甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲):V(乙)=1:2,则加入铝粉的质量为________g。
高一化学填空题中等难度题查看答案及解析
-
如图表示金属X、Y及它们的合金Z分别与足量盐酸反应放出H2量的情况,横坐标表示消耗金属的物质的量,纵坐标表示在标准状况下产生H2的体积.下列有关合金组成的判断正确的是

A.n(Na)∶n(Fe)=2∶1 B.n(Mg)∶n(K)=1∶2
C.n(Na)∶n(Al)=1∶3 D.n(K)∶n(Al)=1∶1
高一化学选择题简单题查看答案及解析
-
把在空气中久置的铝片5.0g投入盛有500mL0,5mol•L-1盐酸溶液的烧杯中该铝片与盐酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:
(1)曲线由0→a段不产生氢气的原因,用化学方程式为______;
(2)曲线由b→c段产生氢气的速率增加较快的主要原因______;
(3)向溶液中加入下列物质,能加快上述化学反应速率的是______.
A.蒸馏水 B.改用铝粉 C.饱和氯化钠溶液 D.浓盐酸 E.少量硫酸铜溶液.
高一化学解答题中等难度题查看答案及解析
-
把5.1 g铝镁合金的粉末放入100 mL某盐酸中,恰好完全反应得到5.6 L H2(标准状况下)。试计算:
(1)该盐酸的物质的量浓度;
(2)该合金中铝的质量分数(结果精确到0.1%)。
高一化学计算题中等难度题查看答案及解析
-
(9分)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1盐酸溶液的烧杯中,该铝片与盐酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示,回答下列问题:
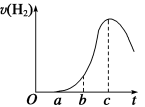
(1)曲线O→a段不产生氢气的原因,用化学方程式解释为 。
(2)曲线b→c段产生氢气的速率增加较快的主要原因是 。
(3)向溶液中加入下列物质,能加快上述化学反应速率的是 。
A.蒸馏水
B.改用铝粉
C.饱和氯化钠溶液
D.浓盐酸
E.少量硫酸铜溶液
高一化学填空题极难题查看答案及解析
-
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
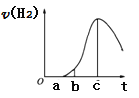
A.O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸
B.a→b段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时刻,反应处于平衡状态
D.t>c,产生氢气的速率降低的主要原因是溶液中H+浓度下降
高一化学单选题中等难度题查看答案及解析
-
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是
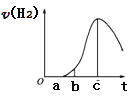
A. O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸
B. b→a段产生氢气的速率增加较快的主要原因之一是温度升高
C. t=c刻,反应处于平衡
D. t>c,产生氢气的速率降低的主要原因是溶液中H+浓度下降
高一化学单选题困难题查看答案及解析