-
金属铜具有良好的导电性和导热性,在电气和电子工业中应用广泛。
(1)用H2O2 和H2SO4 的混合溶液可溶出印刷电路板金属粉末中的铜,写出发生反应的离子方程式 。
(2)某学习小组用“间接碘量法”测定含有CuSO4·5H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.625 g试样溶于水,加过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32—=S4O62—+2I-
①选用 作滴定指示剂,滴定终点的现象是 。
②CuSO4溶液与KI反应的离子方程式为 。
③试样中CuSO4·5H2O的质量分数为 。
高三化学填空题困难题查看答案及解析
-
(14分)金属铜具有良好的导电性和导热性,在电气和电子工业中应用广泛。请回答下列问题:
(1)资料显示:加热条件下氨气能够还原CuO得到金属铜。某同学用装置I和Ⅱ制取纯净干燥的氨气,装置I中应选用试剂______(供选用的试剂有:NH4Cl固体、NH4HCO3固体),试剂a最好选用__________,其作用是_________________________________________;装置III吸收尾气,如何检验所得溶液中数目最多的阳离子(只回答试剂名称和实验现象)_____________________。
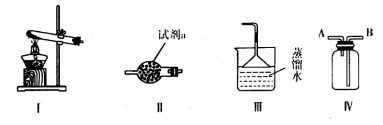
(2)电解硫酸铜溶液也可得到金属铜。
①以黄铜矿(主要成份为CuFeS2)为原料采用电解法可制取硫酸铜溶液。实验室用如图所示装置模拟其过程,阳极区稀硫酸的作用是溶解矿粉得到Cu2+、Fe2+、H2S,硫酸铁的作用是氧化吸收H2S,防止逸出造成污染。电解过程中,阳极区Fe3+的浓度基本保持不变,原因是(用电极反应式回答)______________,阴极上先有固体析出,然后又溶解,阴极区通入O2的作用是(用离子方程式回答)__________________。
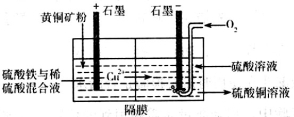
②用惰性电极电解一定浓度CuSO4溶液制取金属铜,一段时间后停止通电,此时加入9.8gCu(OH)2恰好能使电解质溶液恢复至初始状态,则该过程中阳极产生气体的体积为____________L(标准状况)。
高三化学填空题极难题查看答案及解析
-
(15分)铝、铁、铜是应用最普遍的金属。
(1)铜是印刷电路工业的重要材料。用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,是工业上采用的方法之一。已知
Cu(s) + 2H+(aq) == Cu2+(aq) + H2(g) △H= +64.39kJ/mol
2H2O2(l) == 2H2O(l) + O2 (g) △H= ﹣196.46kJ/mol
H2(g) +1/2 O2 (g)== H2O(l) △H= ﹣285.84kJ/mol
在H2SO4溶液中Cu和H2O2反应生成Cu2+和H2O的热化学方程式为
________
(2)镁铝合金生活中应用广泛。取样品a克,溶于200ml 5mol/L的HCl溶液,收集到标况下氢气3.36L,a的取值范围,向反应后溶液中加入4mol/L NaOH溶液________ml,沉淀质量达到最大值。
(3)标准状况下,铁铜合金ag加入足量稀硝酸中,收集了一定量气体NO,在混合了67.2mlO2后,可完全被H2O吸收,无气体剩余。则生成的NO为________ml;向反应后溶液加足量的NaOH溶液,得到沉淀的质量________g。(用含a的代数式表示)
高三化学填空题中等难度题查看答案及解析
-
铝、铁、铜是应用最普遍的金属。
(1)铜是印刷电路工业的重要材料。用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,是工业上采用的方法之一。已知
Cu(s) + 2H+(aq) == Cu2+(aq) + H2(g) △H= +64.39kJ/mol
2H2O2(l) == 2H2O(l) + O2 (g) △H= ﹣196.46kJ/mol
H2(g) +1/2 O2 (g)== H2O(l) △H= ﹣285.84kJ/mol
在H2SO4溶液中Cu和H2O2反应生成Cu2+和H2O的热化学方程式为
________
(2)镁铝合金生活中应用广泛。取样品a克,溶于200ml 5mol/L的HCl溶液,收集到标况下氢气3.36L,a的取值范围________,向反应后溶液中加入4mol/L NaOH溶液ml,沉淀质量达到最大值。
(3)标准状况下,铁铜合金ag加入足量稀硝酸中,收集了一定量气体NO,在混合了67.2mlO2后,可完全被H2O吸收,无气体剩余。则生成的NO为________ml;向反应后溶液加足量的NaOH溶液,得到沉淀的质量________ g。(用含a的代数式表示)
高三化学填空题中等难度题查看答案及解析
-
(8分)研究化学反应原理对于生产、生活及环境保护具有重要意义。
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=+64.39kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ•mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ•mol-1
在H2SO4溶液中Cu与H2
O2反应生成Cu2+和H2O的热化学方程式为______________。
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
①已知0.4 mol KB
rO3在反应中得到2 mol电子生成X,则X的化学式为_______;该反应的还原剂及其配平后的系数是_____。
②根据上述反应可推知_______。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
高三化学填空题困难题查看答案及解析
-
金属具有良好的导电、导热及延展性等,因此广泛应用于制造各种材料.请回答下列问题:
(1)家庭中“钢精锅”是由铝合金做成的,它能长期使用的原因是:______.
(2)下列关于铁制品保护措施的说法中不正确的有______(填序号).
①在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
②相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
③在海轮的外壳上常焊有锌块,且定期更新
④将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理.高三化学解答题中等难度题查看答案及解析
-
(1)镁燃烧不能用CO2灭火,用化学方程式表示其理由 。
(2)用H2O2和稀H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,请写出表示该过程的化学方程式 。
(3)在NaAlO2溶液中通入过量的CO2 (用离子方程式表示)
(4)污水及自来水处理的方法有很多。
Fe2(SO4)3 净水的原理是 。
使用时发现Fe2(SO4)3 并不能使酸性废水中的悬浮物沉降除去,其原因是 。
在酸性环境下,向含重铬酸根的废水中加入FeSO4溶液,然后调节pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应的离子方程式 。
(5)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+,则下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
①硫酸铝和氨水 ②偏铝酸钠和稀盐酸 ③ 硫酸锌和氢氧化钠 ④ 硫酸锌和氨水
高三化学填空题困难题查看答案及解析
-
废弃物的回收利用可实现资源再生,并减少污染.
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196kJ•mol-1
H2(g)+
O2(g)═H2O(l)△H=-285kJ•mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________________
(2)①在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl(氯化亚铜)沉淀,同时溶液的酸性增强.制备CuCl的离子方程式是___________
②在
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=9时,
________ mol/L(已知Ksp[Cu(OH)2]=2.2×10-20)
③若在0.15
硫酸铜溶液中通入过量
气体,使
完全沉淀为CuS,此时溶液中的
浓度是______
(3)工业上常用氨水吸收H2S进行废气脱硫,生成NH4HS。一定温度下1molNH4HS固体在定容真空容器中可部分分解为硫化氢和氨气。下图1是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图1上画出t2时刻后氨气、硫化氢的浓度随时间的变化曲线_________________________。
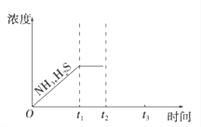
(4)可利用H2S废气进行高温热分解制取氢气,实现化废为宝。
已知:
在恒温密闭容器中,控制不同温度进行
分解实验。以
起始浓度均为0.2
测定
的转化率,结果见下图。
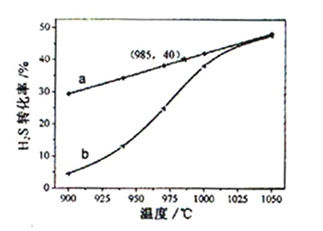
图中a为
的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时
的转化率。据图计算985℃时
按上述反应分解的平衡常数K=______(保留2位有效数字);说明随温度的升高,曲线b向曲线a逼近的原因:_________________________。
高三化学综合题中等难度题查看答案及解析
-
15.用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= +64.39kJ·mol-1
②2H2O2(l)=2H2O (l)+O2(g) △H= -196.46kJ·mol-1
③H2(g)+O2(g)=H2O(l) △H= -285.84kJ·mol-1
下列有关说法错误的是( )
A.铜可以溶解于稀盐酸与H2O2的混合溶液
B.铜溶解于酸性双氧水的热化学方程式为:
Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) △H= —319.68 kJ·mol-1
C.反应①是在任何条件下都不可能发生的化学反应
D.用H2O2和H2SO4的混合溶液溶解铜比用浓硫酸溶解铜环保
高三化学选择题简单题查看答案及解析
-
银是一种美丽的银白色的金属,其导电性和导热性非常好,银及其合金广泛应用于电子电器材料、感光材料、化工材料等方面。
(1)银与铜同族,铜元素在周期表中的位置是__________。基态铜原子的电子排布式是____________________。
(2)Ag+能与NH3、
、CN−等形成配位数为2的配合物。
①C、N、O三种元素的第一电离能从大到小的顺序为__________。
②利用AgNO3和氨水可配制[Ag(NH3)2]OH溶液,在[Ag(NH3)2]OH中存在的化学键的类型有__________(填字母)。
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
③
中N原子的杂化轨道类型是__________,空间构型为__________。写出一种与
、SO2互为等电子体的短周期元素单质分子的化学式__________。
(3)银晶体的晶胞如图所示,为面心立方最密堆积,则银原子的配位数为__________。

晶体空间利用率是指构成晶体的微粒在整个晶体空间中所占的体积分数,即空间利用率=
 ×100%。则银晶体的空间利用率为__________(保留2位有效数字,
×100%。则银晶体的空间利用率为__________(保留2位有效数字,)。
高三化学填空题中等难度题查看答案及解析