-
金属钛因为其优越的性能被称为“未来金属”,其工业冶炼涉及到的反应如下:TiO2+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
回答下列相关问题:
(1)钛的价层电子排布式为______________。
(2)已知部分物质熔沸点如下:
| 名称 | 金红石 | 金刚石 | 四氯化钛 | 四溴化钛 | 四碘化钛 |
| 化学式 | TiO2 | C | TiCl4 | TiBr4 | TiI4 |
| 熔 点 | 1830℃ | 3550℃ | -24.1℃ | 38℃ | 150℃ |
| 沸点 | 2927℃ | 4827℃ | 136.4℃ | 233.1℃ | 377.2℃ |
| 晶型 | 离子晶体 | | 分子晶体 |
表中金刚石的晶型为_________;自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是_____________。
(3)配位数为6,组成为TiCl3·6H2O 的晶体有两种:化学式为[TiCl( H2O)5]Cl2·H2O 的 X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y 与AgNO3以1:3物质的量比反应生成沉淀,则Y的化学式为___________,Y配离子的空间构型为_________。
(4)钙钛矿是重要的含钛矿物之一,其主要成分Z的晶胞如下图所示:
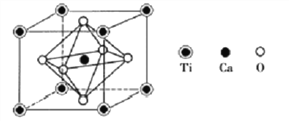
推测Z的化学式为________________。
(5)若晶胞参数a=384.1pm,Z晶体的密度为______g/cm3( 已知 NA≈6.0×1023;3.8413≈ )。
)。
-
金属钛因为其优越的性能被称为“未来金属”,其工业冶炼涉及到的反应如下:TiO2+2C+2Cl2 TiCl4+2CO。回答下列相关问题:
TiCl4+2CO。回答下列相关问题:
(1)基态钛原子的价层电子排布式为____ ,上述反应中非金属元素电负性由大到小是______;
(2)已知部分物质熔沸点如下:
| 名称 | 金红石 | 金刚石 | 四氯化钛 | 四溴化钛 | 四碘化钛 |
| 化学式 | TiO2 | C | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 1830 | 3550 | -24.1 | 38 | 150 |
| 沸点/℃ | 2927 | 4827 | 136.4 | 233.1 | 377.2 |
自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是__________。
(3)配位数为6,组成为TiCl3•6H2O 的晶体有两种:化学式为[TiCl(H2O)5]Cl2•H2O的X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y与AgNO3 以1:3物质的量之比反应生成沉淀,则Y的化学式为 ______。
(4)钙钛矿是重要的含钛矿物之一。其主要成分Z 的晶胞如图所示。推测Z的化学式为__________,Ca填充在O围成的_________空隙中。
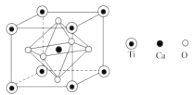
(5)若晶胞参数 a=384.1pm,Z晶体的密度为 _________列出计算表达式并计算出两位有效数字结果,3.8413≈56.67,阿伏加德罗常数用 6.0×1023 mol-1)
-
钛被誉为“21世纪金属”。工业冶炼钛的第一步反应为:
TiO2+2C+2Cl2  TiCl4+2CO。下列关于该反应的说法正确的是
TiCl4+2CO。下列关于该反应的说法正确的是
A.TiO2是氧化剂
B.氧化剂与还原剂的物质的量之比为1:1
C.Cl2发生氧化反应
D.当2 mol C参加反应时,转移的电子数目为2 mol
-
钛被誉为“21世纪金属”。工业冶炼钛的第一步反应为:TiO2+2C+2Cl2 → TiCl4+2CO。下列关于该反应的说法错误的是
A. Cl2是氧化剂
B. CO是氧化产物
C. 氧化剂与还原剂的物质的量之比为1:1
D. 当2 mol C参加反应时,转移的电子数目为2mol
-
钛是一种现代工业应用广泛的优良金属,使用量可能会超过金属铁。工业上冶炼金属钛的方法有多种,下列反应原理是比较常见的冶炼钛的一种方法:
①TiO2+2Cl2 +2C TiCl4+2CO;②TiCl4+2Mg
TiCl4+2CO;②TiCl4+2Mg  Ti+2MgCl2。
Ti+2MgCl2。
请回答下列问题:
(1)与钛同周期元素中未成对电子数最多的基态原子的电子排布式为_________________。
(2)反应①中涉及的非金属元素电负性由大到小的顺序为_________(用元素符号表示);与CO互为等电子体的离子为__________(填化学式,写一种即可)。
(3)①TiCl4在常温下是无色液体,分子中4 个氯原子不在一个平面上,TiCl4空间构型为____,该物质能否溶解在苯溶剂中__________(填“能”或“否”) 。
②三氯化钛与酒石酸( )反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
)反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
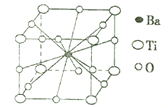
(4)钛酸钡晶体的结构示意图如图所示,若晶胞参数为a pm,则钛酸钡晶体的密度=_____g/cm3(阿伏加德罗常数用NA表示)。
-
工业冶炼钛的第一步反应为:TiO2(s)+2C(s)+2Cl2 TiCl4(g)+2CO。下列关于该反应的说法正确的是( )
TiCl4(g)+2CO。下列关于该反应的说法正确的是( )
A.TiCl4既是氧化产物又是还原产物
B.氧化剂与还原剂的物质的量之比为1:1
C.当转移电子数目为0.2NA时,气体体积增大1.12L
D.当有26g固体参加反应时,转移电子数目为NA
-
钛(Ti)被称为继铁、铝之后的第三金属,以TiO2制取Ti的主要反应有:
①TiO2+2C+2Cl2 TiCl4+2CO ②TiCl4+2Mg
TiCl4+2CO ②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
下列叙述正确的是
A.反应①是置换反应 B.反应②是复分解反应
C.反应②中金属镁是还原剂 D.反应①中TiO2是氧化剂
-
工业上用金红石(主要成分TiO2)制金属钛可通过以下反应进行:
①TiO2+2C+2Cl2 TiCl4+2CO ②TiCl4+2Mg
TiCl4+2CO ②TiCl4+2Mg  Ti+2MgCl2
Ti+2MgCl2
对于上述两个反应的叙述正确的是
A.都是氧化还原反应 B.都是置换反应
C.反应中钛元素都被还原 D.加热时金属钛和氩气(Ar)能反应
-
将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一。已知:
TiO2(s) + 2Cl2(g) == TiCl4(l) + O2(g) △H = +140.5 kJ/mol
C(s,石墨) + 1/2O2(g) == CO(g) △H = -110.5 kJ/mol
则反应TiO2(s) + 2Cl2(g) + 2C(s,石墨) == TiCl4(l) + 2CO(g) 的△H 是
A. +80.5 kJ/mol B. +30.0 kJ/mol C. -30.0 kJ/mol D. -80.5 kJ/mol
-
钛被誉为“21世纪金属”,工业冶炼钛的第一步反应为TiO2+2C+2Cl2 TiCl4+2CO。下列关于该反应的说法正确的是( )
TiCl4+2CO。下列关于该反应的说法正确的是( )
A. TiO2是氧化剂 B. 四氯化钛是还原产物
C. Cl2发生氧化反应 D. 氧化剂与还原剂的物质的量之比为1∶2
TiCl4+2CO

)。

 Ti+2MgCl2。
Ti+2MgCl2。 )反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
)反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。