-
25 ℃时,现有浓度均为0.10 mol·L−1的两种溶液:① 氨水、② 盐酸。请回答:
(1)溶液①的pH______13(填“>”、“<”或“=”)。
(2)两溶液等体积混合后所得溶液显酸性,原因是______(用离子方程式表示)。
(3)下列说法正确的是______(填字母)。
a.向①中滴加②,溶液的导电性增强
b.NH3·H2O和 HCl均能促进水的电离
c.若两溶液混合后pH = 7,则溶液中离子浓度存在关系:c(NH4+)= c(Cl-)> c(H+)= c(OH-)
(4)用石墨作电极电解盐酸时,阳极反应式是______。
高二化学综合题中等难度题查看答案及解析
-
25摄氏度时,现有浓度均为0.10 mol/L的四种溶液:①氨水 ② NaOH溶液 ③CH3COOH溶液 ④盐酸。请回答:
(1)①溶液中c(H+) c(OH-) (填“>”、“<”或“=”)。
(2)醋酸的电离方程式是 。
(3)①对水的电离平衡产生的影响是 ,理由是 。
(4)溶液②和溶液③等体积混合后所得溶液显碱性,原因是 (用离子方程式表示)。
高二化学填空题中等难度题查看答案及解析
-
室温下,用0.10mol/L的盐酸分别滴定20.00mL浓度均为0.10mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。
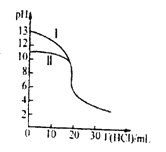
下列说法不正确的是
A. Ⅱ表示的是滴定氨水的曲线,当V(HC1)=20mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且c(NH4+)=c(Cl-)
C. 滴定氢氧化钠溶液,V(HCl) >20 mL 时一定有: c(Cl-) >c(Na+) >c(H+) >c(OH-)
D. 当滴定氨水消耗V(HC1)=10 mL 时,有: 2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
高二化学单选题中等难度题查看答案及解析
-
25℃时,现有浓度均为0.10mol·L-1的两种溶液:①CH3COOH溶液、②NaOH溶液。请回答:
(1)溶液①的pH __________(填“>”“=”或“<”)1,原因是______________。
(2)将等体积①和②混合,所得溶液显__________(填“酸”“碱”或“中”)性,原因是__________________(用离子方程式表示)。
(3)向①中逐滴加入②至所得溶液pH=7的过程中(不含pH=7时的溶液),下列关系正确的是_________(填选项序号)。
a.c(H+)>c(OH-)
b.c(Na+)<c(CH3COO-)
C.c(Na+) =c(CH3COO-)+c(CH3COOH)
d.c(OH-) +c(CH3COO-) =c(H+) +c(Na+)
高二化学填空题中等难度题查看答案及解析
-
25℃时,现有浓度均为0.10mol/L的三种溶液:①NaCl溶液、②CH3COONa溶液、③CH3COOH溶液。请回答:
(1)三种溶液中,pH>7的是__________(填序号),其原因是________________________________________(用离子方程式表示)。pH<7的是__________(填序号),其原因是________________________________________(用化学用语表示)。
(2)下列说法正确的是__________(填序号)。
a.CH3COONa是弱电解质
b.CH3COONa和CH3COOH都能促进水的电离
c.①②两种溶液等体积混合后,溶液中c(Na+)+c(H+)=c(Cl-)+c(CH3COO-)+c(OH-)
(3)②③两种溶液等体积混合后,溶液pH<7,该混合溶液中离子浓度大小关系是_____________________
(4) 25℃时,电解1.00L饱和NaCl溶液一段时间后,收集到1.12LH2(标准状况)。该反应的离子方程式是____________,此时溶液的pH是____________(不考虑溶液体积的变化)。
高二化学解答题简单题查看答案及解析
-
现有25℃时0.1mol•L-1的氨水,请回答以下问题:
(1)氨水呈碱性的原因为(用离子方程式表示)___。
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式___;若所得溶液的pH=5,则溶液中水所电离出的氢离子浓度为___。
(3)若向氨水中加入少量硫酸铵固体,此时溶液中
__(填“增大”、“减小”或“不变”)。
(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=__。
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___。
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因___。
高二化学综合题中等难度题查看答案及解析
-
下列关于室温下氨水的叙述,正确的是( )
A. 同pH同体积的氨水和NaOH溶液,能分别与同浓度同体积的盐酸恰好完全中和
B. 加水稀释0.10 mol•L-1的氨水,溶液中n(OH-)减小
C. 若温度不变,在氨水中加入少量NH4Cl固体,氨水的电离度和电离平衡常数均变小
D. 氨水中的离子浓度关系满足:c(OH-)=c(H+)+c(NH4+)
高二化学单选题困难题查看答案及解析
-
下列关于室温下氨水的叙述,正确的是( )
A.同pH同体积的氨水和NaOH溶液,能分别与同浓度同体积的盐酸恰好完全中和
B.加水稀释0.10 mol?L-1的氨水,溶液中n(OH-)减小
C.若温度不变,在氨水中加入少量NH4Cl固体,氨水的电离度和电离平衡常数均变小
D.氨水中的离子浓度关系满足:[OH-]=[H+]+[NH4+]
高二化学选择题困难题查看答案及解析
-
在25℃时,向浓度为0.1mol▪L-1、体积为1.0L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线如图所示,d点两种溶液恰好完全反应。请根据图中信息回答下列问题:
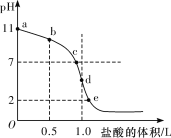
(1)在25℃时,NH3▪H2O的电离常数K=________。
(2)比较b、d两点时的溶液中,由水电离出的c(OH-)大小为b_____(填“>”“<”或“=” )d。
(3)滴定过程中所用盐酸的pH=____________。
(4)滴定时,不考虑中和滴定放热引起的温度变化,由b点到c点的过程中,下列各选项中数值会发生变化的是_________(填字母代号)。
高二化学综合题困难题查看答案及解析
-
下图是向25.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH变化的图象,根据图象分析,下列结论中不正确的是
A.盐酸起始浓度为0.10 mol·L-1
B.NaOH溶液浓度为0.10 mol·L-1
C.滴到中点时,耗NaOH物质的量为0.0025mol
D.滴入碱量为20.00mL时,向混合溶液中滴入2滴酚酞试液,溶液显红色
高二化学选择题中等难度题查看答案及解析