-
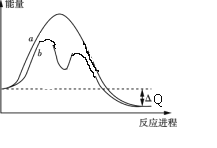
氯及其化合物在生活和生产中应用广泛。已知:900 K时,4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) 反应过程能量变化如图所示。该反应是 __________反应(放热还是吸热),有催化剂参与反应过程 ________(填a或b)。
2Cl2(g)+2H2O(g) 反应过程能量变化如图所示。该反应是 __________反应(放热还是吸热),有催化剂参与反应过程 ________(填a或b)。
-
氯及其化合物在生活和生产中应用广泛。
(1)已知:900 K时,4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。
①该反应是放热还是吸热,判断并说明理由___________________________。
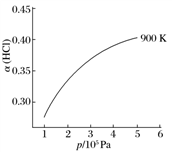
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5 ×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________
(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:________________________________。
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=________________(用c0、ct表示)mol·L-1。
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO + Cl-
+ Cl-
Ⅱ.ClO +ClO-===ClO
+ClO-===ClO +Cl-
+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:______________________________________________________。
-
氯气及其化合物在生产生活中有重要的应用。
(1)可用O2将HCl转化为Cl2:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。已知相关化学键的键能如下表所示
| 化学键 | H-Cl | O=O | Cl – Cl | H-O |
| E(kJ·mol-1 | a | b | c | d |
则该反应的△H=______________。(用含a、b、c、d的代数式表示)
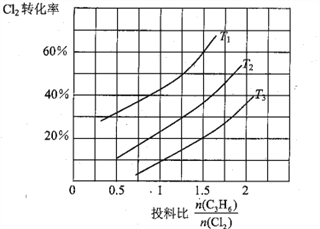
(2)氯气是有机合成中的重要试剂,丙烯(CH2=CHCH3)和Cl2在一定条件下发生如下反应: CH2=CHCH3 (g)+Cl2(g)  CH2=CHCH2Cl(g)+HCl(g)。一定压强下,该反应在不同温度、不同投料比时,达平衡时Cl2的转化率如图所示(T12< T3)
CH2=CHCH2Cl(g)+HCl(g)。一定压强下,该反应在不同温度、不同投料比时,达平衡时Cl2的转化率如图所示(T12< T3)
①该反应的△H______________0(填“>”或“<”)
②下列措施能增大丙烯的平衡转化率的是______________ (填标号)。
A.降低温度 B.减小容器的体积
C.使用新型催化剂 D.从容器中移走氯化氢
③T1时,在容积为5L的密闭容器中充入0.15mol丙烯和0.10 molCl2,10min时达到平衡,则v(Cl2)为______________mol·〔L·min)-1,平衡常数K为______________,保持温度不变,减小投料比 ,K值将______________ (填“增大”“减小”或“不变”);若起始时向该容器中充入0.30mol丙烯、0.20 molCl2、0.15 mol CH2=CHCH2Cl和0.30 molHCl,判断反应进行的方向并说明理由____________________________。
,K值将______________ (填“增大”“减小”或“不变”);若起始时向该容器中充入0.30mol丙烯、0.20 molCl2、0.15 mol CH2=CHCH2Cl和0.30 molHCl,判断反应进行的方向并说明理由____________________________。
④上述反应在低于某温度时,CH2=CHCH2Cl的产率快速下降,可能的原因是____________________________。
-
(14分)近年来,碳和碳的化合物在生产生活实际中应用广泛。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:① 2 CH4 (g) + 3O2 (g) = 2 CO (g) + 4 H2O(l) △H1 = -1214.6 KJ/mol
② 2 CO (g) + O2(g) = 2 CO2 (g) ΔH2 = -566 kJ/mol
则反应CH4(g) + 2 O2 (g) = CO2 (g) + 2 H2O (l) 的△H =________。
(2)将两个石墨电极插人KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。通入CH4的一极,其电极反应式是:CH4 + 10 OH―― 8e-= CO32-+ 7 H2O;通入O2的一极,其电极反应式是________。
(3)若用石墨做电极电解500 ml饱和食盐水,写出电解反应的离子方程式为:________ ;电解一段时间后两极共收集到标准状况下的气体1.12 L(不考虑气体的溶解)。停止通电,假设反应前后溶液体积不变,则所得溶液的pH=________。
(4)将不同量的CO (g) 和H2O (g) 分别通入到体积为2 L的恒容密闭容器中,进行反应
CO (g) + H2O (g)  CO2 (g) + H2 (g),得到如下三组数据:
CO2 (g) + H2 (g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min |
| H2O | CO | CO2 | CO |
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
① 实验1中以υ(H2) 表示的反应速率为________ 。
② 实验2中的平衡常数是________ (计算结果保留两位小数)。
③ 该反应的正反应为 ________(填“吸”或“放”)热反应。
④ 若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),
则a、b应满足的关系是________ (用含a、b的数学式表示)。
-
在298K、100kPa时,已知:
①2H2O(g)=O2(g)+2H2(g)△H1;
②H2(g)+Cl2(g)=2HCl(g)△H2;
③2H2O(g)+2Cl2(g)=4HCl(g)+O2(g)△H3;
则△H3与△H1和△H2间的关系正确的是
A.△H3 =△H1+2△H2 B.△H3 =△H1+△H2 C.△H3 =△H1—2△H2 D.△H3 =△H1—△H2
-
氮和碳的化合物在生产生活中应用广泛。
(1)①氯胺(NH2Cl)的电子式为______。可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如下表所示(假定不同物质中同种化学键的键能一样),则上述反应的△H=_________。
| 化学键 | N﹣H | Cl﹣Cl | N﹣Cl | H﹣Cl |
| 键能/(kJ·mol﹣1) | 391.3 | 243.0 | 191.2 | 431.8 |
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为_______________________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为_________(填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=__________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
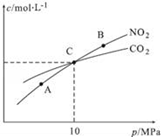
①A、B两点的浓度平衡常数关系:Kc(A)___Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是__(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=________(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O CH3CHOH+CH3CHOOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如图所示:
CH3CHOH+CH3CHOOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如图所示:
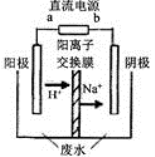
①试写出电解过程中,阴极的电极反应式:______________________ 。
②在实际处理过程中,当电路中I=50A时,10min处理乙醛8.8g,则电流效率为______(计算结果保留3位有效数字,每个电子的电量为1.6×10-19C,电流效率=实际反应所需电量/电路中通过电量×100%)。
-
在298K、101kPa时,已知:2H2O(g)=O2(g)+2H2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2;
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是( )
A. △H3=△H1+2△H2 B. △H3=△H1+△H2
C. △H3=△H1—2△H2 D. △H3=△H1—△H2
-
【加试题】氮及其化合物在生活和生产中应用广泛。
(1)N2O是一种强大的温室气体,在一定条件下,其分解的化学方程式为:2N2O(g)=2N2(g)+O2(g) ΔH<0,你认为该反应的逆反应是否自发进行,请判断并说明理由___________。
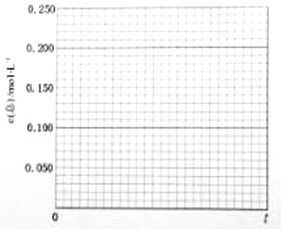
某研究小组为针对N2O的分解进行研究,常温下,在1L恒容容器中充入0.100mol N2O气体,加热到一定温度后使之反应,请画出容器中气体的总浓度c(总)随时间t变化的总趋势图。_____________
(2)①N2O5是一种新型硝化剂。工业上可用N2O4通过电解制备N2O5,阴、阳极室之间用质子交换膜隔开,两极电解液分别为稀硝酸溶液和溶有N2O4的无水硝酸,用惰性电极电解时,生成N2O5极室的电极反应式为_____________。
②已知,一定条件下有下列反应:
Ⅰ2N2O5(g)  4NO2 (g)+ O2(g) ΔH1
4NO2 (g)+ O2(g) ΔH1
Ⅱ2NO2(g)  2NO (g)+ O2(g) ΔH2
2NO (g)+ O2(g) ΔH2
Ⅲ2NaOH(aq)+N2O5(g)=2NaNO3(aq)+H2O(1) ΔH3
写出NO和O2的混合物溶于NaOH溶液生成硝酸盐的热化学方程式___________。
在容积为2L的恒容密闭容器中充入1.00mol N2O5,假设在T℃时只发生反应Ⅰ、Ⅱ,若达到平衡状态后O2为1.00mol,NO2为0.400mol,则T℃时反应Ⅰ的平衡常数的值为_________。
(3)NH3和Cr2O3固体在高温下可以制备多功能材料CrN晶体,其反应为Cr2O3(s)+2NH3(g)  2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
-
氮及其化合物在生活和生产中应用广泛。
I.(1)N2O是一种典型的温空气体,在一定条件下,其分解的化学方程式为:2N2O(g)==2N2(g) +O2(g) △H________________。
(2)已知一定条件下有下列反应:
①2N2O5(g) 4NO2(g)+ O2(g) △H1
4NO2(g)+ O2(g) △H1
②2NO2(g) 2NO(g)+ O2(g) △H2
2NO(g)+ O2(g) △H2
③2NaOH(aq)+ N2O5(g) 2NaNO3(aq)+H2O(1) △H3
2NaNO3(aq)+H2O(1) △H3
写出NO与O2的混合物溶于NaOH 溶液生成硝酸盐的热化学方程式_____________________________。在容积为2L 的恒容密闭容器中充入1.00mol N2O5,假设在T℃时只发生反应①、②,若达到平衡状态后O2 为1.00mol,NO2为0.400mol,则T℃时反应①的平衡常数的值为_______________________。
II.联氨(N2H4)是一种绿色环保的还原剂,其氧化产物为氮气。
(3)联氨为二元弱碱,在水中的电离方式与氨相似,写出联氨与过量盐酸反应的离子方程式_______________。
(4)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3:2,则该分解反应的化学方程式为_____________________________________。
(5)SCR法是工业上消除氮氧化物的常用方法,反应原理为:4NH3(g) +4NO(g) +O2(g)  4N2(g) +6H2O(g)△H<0其他条件相同,某2L密闭容器中分别投入2mol NH3、2molNO、lmolO2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图所示。下列叙述不正确的是_________。
4N2(g) +6H2O(g)△H<0其他条件相同,某2L密闭容器中分别投入2mol NH3、2molNO、lmolO2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图所示。下列叙述不正确的是_________。
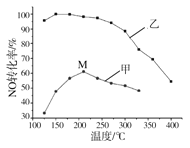
A.在催化剂甲作用下,图中Y点处(210℃) NO的转化率一定不是该温度下的平衡转化率
B.在催化剂甲作用下,高于210℃时,NO转化率降低的原因可能是催化剂活性降低
C.300℃时,NO的平衡转化率M点高于Z点的原因是乙催化剂催化效率高
D.其他条件不变,增加NH3的浓度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
III.NH3是一种重要的化工原料。
(6)NH3和Cr2O3 固体高温下可以制备多功能材料CrN晶体,其反应为Cr2O3 (s) +2NH3(g)  2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因_____________________________________________。
2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因_____________________________________________。
-
氨是化学实验室及化工生产中的重要物质,应用广泛。
(1)已知25℃时:N2(g)+O2(g) 2NO(g) ΔH=+183 kJ/mol
2NO(g) ΔH=+183 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH=-1164.4 kJ/mol
则N2(g)+3H2(g) 2NH3(g) ΔH=______kJ/mol
2NH3(g) ΔH=______kJ/mol
(2)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
| N2 | H2 | NH3 |
| 投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
| 投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_______。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
④L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。

ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
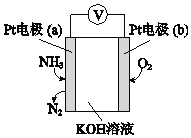
①电极b上发生的是______反应(填“氧化”或“还原”)。
②写出电极a的电极反应式_________。
2Cl2(g)+2H2O(g),反应自发。
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________

+ Cl-
+ClO-===ClO
+Cl-






