-
[化学—选修物质结构与性质](15分)
下面的表格是元素周期表的一部分,其中的字母对应不同的元素。(用元素符号回答问题)
A
M
Q
R
E
B
D
G
L
C
请回答下列问题:
(1)M、Q、R按第一电离能由小到大的顺序为 ________。
(2)Q元素的氢化物分子的立体结构呈________ 形,该分子属于________分子(填“极性”或“非极性”),中心原子呈________杂化方式;
(3)写出L基态原子核外电子排布式 ________,L的硫酸盐溶液中加入过量Q的氢化物的水溶液可得深蓝色溶液,请写出该溶液显深蓝色的微粒的化学式________。
(4)已知AMQ分子是直线型分子,则其分子中含有σ键和π键的数目之比为。
(5)试比较Q、B和C的氢化物沸点高低及热稳定性并说明理由________。________
高三化学填空题简单题查看答案及解析
-
(化学——物质结构与性质,13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
A
M
Q
R
E
D
G
J
请回答下列问题:
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有 个。该晶体属于 晶体
A.离子晶体 B.原子晶体 C.分子晶体 D.金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种 分子(填极性或非极性)。
(3)请写出D-的电子排布式: 。
(4)M2A2也是直线型分子,1个分子中含有 个σ键。
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式(用元素符号表示) 。
高三化学填空题中等难度题查看答案及解析
-
[化学一选修3物质结构与性质]
下表为长式周期表的一部分,其中的字母A--J分别代表对应的10种元素.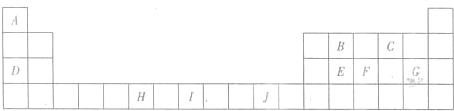
请回答下列问题:
(1)元素I的原子结构示意图为______.
(2)B、E两元素分别与元素C按原子个数比为1:2形成化合物时,中心原子的杂化方式分别为______和______,这两种化合物的熔沸点差别很大的原因是______.
(3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的______.该配离子中含有的化学键类型是______,其中G的核外电子排布式为______.
(4)元素D与元素G形成的化合物DG的晶胞结构如图所示,每个D离子周围与之最近的D离子的个数为______.若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该化合物的密度为______.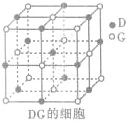
高三化学解答题中等难度题查看答案及解析
-
( 13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
A
M
Q
R
E
D
G
J
请回答下列问题:
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有 个。该晶体属于 晶体
A .离子晶体 B . 原子晶体 C . 分子晶体 D. 金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种 分子(填极性或非极性)。
(3)请写出D-的电子排布式: 。
(4)M2A2也是直线型分子,1个分子中含有 个σ键。
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式。(用元素符号表示)
高三化学计算题困难题查看答案及解析
-
【化学——选修3 物质结构与性质】选考(15分)下图为元素周期表的一部分,字母下方数值为该元素电负性,根据信息回答下列问题(用相应元素符号进行答题):
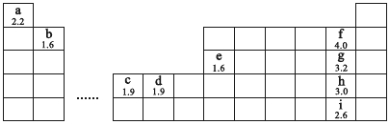
(1)b、h两元素可形成化合物bh2,写出其电子式: 。
(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为 ,eg3、e2g6中心原子e的杂化方式分别为 、 。
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式: 。
(4)f、g、h、i四种元素对应单质分子的键能如下表:
共价键
f—f
g—g
h—h
i—i
键能(kJ/mol)
157
242.7
193.7
152.7
试从原子半径角度阐述f—f键键能反常的原因: 。
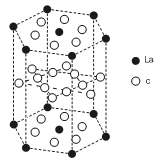
(5)c元素的元素符号是 ,价电子排布式为 ,下图是
一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图中勾画出该晶体的一个晶胞。计算出该合金的化学式为: 。
高三化学填空题极难题查看答案及解析
-
下面的表格是元素周期表的一部分,其中的字母对应不同的元素.
请回答下列问题:A M Q R E D G J
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同.该合金中每个G原子周围与其最近且等距的J原子有______个.
该晶体属于______晶体
A.离子晶体 B.原子晶体 C.分子晶体 D.金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种______分子(填极性或非极性).
(3)请写出D-的电子排布式:______.
(4)M2A2也是直线型分子,1个分子中含有______个σ键.
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式.(用元素符号表示)高三化学解答题中等难度题查看答案及解析
-
(15分)【化学---选修模块:物质结构与性质】
下表为周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是________(填编号)。
(2)元素⑥形成的最高价含氧酸根的立体构型是________,其中心原子的杂化轨道类型是_______。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是________。
A.分子中含有氢键 B.属于非极性分子
C.含有4个σ键和1个π键 D.该氢化物分子中,②原子采用sp2杂化
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为________;该元素与元素①形成的分子X构形为________;X在①与③形成的分子Y中的溶解度很大,其主要原因是________。
(5)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为________(用对应的元素符号表示)。

高三化学填空题中等难度题查看答案及解析
-
本题对应于“物质结构与性质”选修模块的内容。
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
Z
M
L
Q
R
D
A
T
X
Y
E
J
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LX2分子的电子式是_________,MY3分子是_________(填“极性分子”或“非极性分子”)。
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最
高记录。右图中所示的是该化合物的晶体结构单元。图中上,下
底面中心“Δ”处的原子是_______(填元素符号)。

高三化学填空题中等难度题查看答案及解析
-
【化学一选修3:物质结构与性质】
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
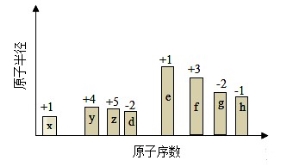
根据判断出的元素回答问题:
(1)f在元素周期表的位置是____。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_ _>____;比较g、h的最高价氧化物对应的水化物的酸性强弱是:__ _>_ _。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:①R离子浓度由大到小的顺序是:______ _。②写出m点反应的离子方程_ 。③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
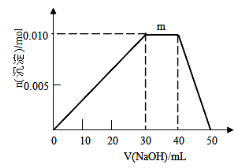
高三化学填空题困难题查看答案及解析
-
【选修3-物质的结构与性质】(15分)

上表为周期表的一部分,其中的编号代表所对应的元素。请回答下列问题:
(1)⑨号元素的基态原子的价电子排布式是________,与其同周期,且基态原子的核外未成对电子数最多的元素是______(写出元素符号),②号元素基态原子的电子排布图为___。
(2) ①号与③号元素形成的含有18电子的物质为________(写出名称),②号与③号元素形成的,能造成温室效应的物质的空间构型为________。
②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为________(用对应的元素符号表示),常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因是____________。
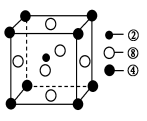
(3)①、②两种元素能形成多种平面形分子,其中有一种相对分子质量最小,有关该分子的说法中正确的是________。
a.该分子属于含有极性键的非极性分子b.该分子含有4个σ键和1个π键
c.该分子中的②原子采取sp2杂化d.该物质易溶于水,并能和水反应得到酒精
(4)某元素的价电子排布式为nsnnpn+1,该元素可与元素①形成含有10个电子的分子X,将过量的X通入盛有硫酸铜溶液的试管里,产生的现象为_______。
(5) 若D元素与Fe元素形成某种晶体如图所示。若晶胞的边长为a nm,则合金的密度为________g/cm3。
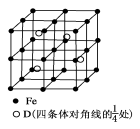
高三化学简答题中等难度题查看答案及解析