-
常温下,1.0mol/L一元酸HA与等体积等浓度KOH溶液混合,所得溶液粒子的浓度关系如右表(不含水分子的5种粒子,A为短周期元素),下列说法正确的是
粒子
K+
A-
X
Y
Z
浓度(mol/L)
0.50
0.49
c(X)>c(Y)>c(Z)
A.元素A最高价氧化物对应水化物为HAO4
B.表格中X表示HA,Y表示H+
C.所得溶液中c(X)+ c(A-)= c(K+)
D.等体积等浓度的HA和盐酸分别加水稀释10倍后,pH (HA) >pH(HCl)
高三化学选择题困难题查看答案及解析
-
常温下,0.1mol·L﹣1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A.该混合溶液pH=7.0
B.原HA溶液中:c(HA)>c(H+)>c(A﹣)
C.图中X表示HA,Y表示OH﹣,Z表示H+
D.混合溶液中:c(X)+x(A﹣)=c(K+)
高三化学单选题中等难度题查看答案及解析
-
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
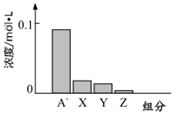
A.将HA加水稀释,溶液中所有粒子的浓度均减小
B.等浓度的HA和NaOH溶液中水的电离程度相同
C.图中X表示HA,Y表示H+,Z表示OH-
D.该混合溶液中:
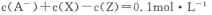
高三化学选择题困难题查看答案及解析
-
下列溶液中粒子的物质的量浓度关系正确的是:
A.0.1 mol·L - 1 NaHC2O4溶液与0.1 mol·L – 1KOH溶液等体积混合,所得溶液中:
c(Na+)>c(K+) >c(C2O42-) >c(OH-) >c(HC2O4-)
B.20mL 0.1 mol·L - 1NH4Cl溶液与10mL 0.1 mol·L - 1NaOH溶液混合后溶液呈碱性,所得溶液中:c(Cl-)>c(NH4+) >c(Na+)>c(OH-)>c(H+)
C.常温下,pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:
c(Na+)+ c(OH-) >c(H+)+ c(F-)
D.0.1 mol·L – 1 NH3·H2O溶液与0.1 mol·L – 1 HNO3溶液等体积混合,所得溶液中:
c(H+) >c(OH-) + c(NH3·H2O)
高三化学选择题困难题查看答案及解析
-
实验测得常温下0.1 mol/L某一元酸(HA)溶液的pH不等于1,0.1 mol/L某一元碱(BOH)溶液里:
=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
A.c(B+)>c(A-)>c(OH-)>c(H+)
B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(H+)>c(A-)>c(OH-)>c(B+)
D.c(B+)>c(A-)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
-
常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A. c(H+) >1.0×10-7mol/L
B. c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C. c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)
D. c(Cl-)> c(NH4+)> c(HCO3-)> c(CO32-)
高三化学选择题困难题查看答案及解析
-
常温时,下列溶液中各粒子的浓度关系正确的是
A. pH=2的HA溶液与pH=12的KOH 溶液等体积混合:c(H+)>c(OH-)
B. 0.1mol/L的NaHC2O4溶液,其pH=4:c(HC2O4-)>c(H+)>c(H2C2O4)>c(C2O42-)
C. 醋酸钠和醋酸的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. 0.1mol/L的NaHSO3溶液中:c(H+)+c(H2SO3)=c(SO32-)+c(OH-)
高三化学单选题中等难度题查看答案及解析
-
常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.
<1.0×10-7mol/L
B.c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)
D.c(Cl-)> c(NH4+)> c(HCO3-)> c(CO32-)
高三化学选择题困难题查看答案及解析
-
常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.<1.0×10-7mol/L
B.c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3)
C.c(Cl-)> c(NH4+)> c(HCO3-)> c(CO32-)
D.c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+2 c(CO32-)
高三化学选择题困难题查看答案及解析
-
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号
HB物质的量浓度(mol/L)
KOH物质的量浓度(mol/L)
混合溶液的pH
甲
0.2
0.2
pH=a
乙
c1
0.2
pH=7
丙
0.1
0.1
pH>7
丁
0.1
0.1
pH=9
请回答下列问题:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HB是强酸还是弱酸________。
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2 mol/L________?(填“是”或“否”)。混合溶液中离子浓度c(B-)与c(K+)的大小关系是________。
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,HB是________酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol/L。写出该混合溶液中下列算式的精确结果(不能做近似计算),c(K+)-c(B-)=_mol/L。
高三化学填空题困难题查看答案及解析