-
在10mL0.1mol·L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系错误的是
A C(Na+)>C(Ac-)>C(H+)>C(OH-) B C(Na+)>C(Ac-)>C(OH-)>C(H+)
C C(Na+)=C(Ac-)>C(HAc) D C(Na+)+C(H+)=C(Ac-)+C(OH-)
高三化学选择题困难题查看答案及解析
-
在10mL0.1mol•L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系正确的是( )
A.c(Na+)>c(Ac-)>c(H+)>c(OH-)
B.c(Na+)=c(Ac-)>c(OH-)=c(H+)
C.c(OH-)=c(H+)+c(HAc)
D.2c(Na+)+c(H+)=2c(Ac-)+c(OH-)+c(HAc)高三化学选择题中等难度题查看答案及解析
-
在10ml 0.1mol·L-1NaOH溶液中加入同体积、同浓度HAc溶液,反应后溶液中各微粒的浓度关系错误的是
A.c(Na+)>c(Ac-)>c(H+)>c(OH-) B.c(Na+)>c(Ac-)>c(OH-)>c(H+)
C.c(Na+)=c(Ac-)+c(HAC) D.c(Na+)+c(H+)=c(Ac-)+c(OH-)
高三化学选择题中等难度题查看答案及解析
-
在10mL0.1mol·L-1NaOH溶液中加入同体积同浓度的弱酸HA溶液,反应后溶液中各离子的浓度关系错误的是
A.c(Na+)=c(A-)+c(HA) B.c(Na+)+c(H+)=c(A-)+c(OH-)
C.c(Na+)>c(A-)>c(OH-)>c(H+) D.c(Na+)>c(A-)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
-
25℃时,用0.1mol•L-1的NaOH溶液滴定20mL0.1mol•L-1CH3COOH(Ka=1.75×10-5)溶液过程中,消耗NaOH溶液的体积与溶液pH的关系如图所示,下列各项中微粒浓度间关系正确的是
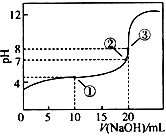
A.点①所示溶液中:2c(CH3COO-)-2c(CH3COOH)= c(H+)-c(OH-)
B.点②所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.点③所示溶液中:c(CH3COO-)-c(CH3COOH)= c(Na+)+ 2c(H+)-2c(OH-)
D.pH=12的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)>c(CH3COOH)
高三化学选择题困难题查看答案及解析
-
20℃时向10mL0.1mol·L-1醋酸溶液中不断滴入0.1mol·L-1NaOH溶液,溶液pH变化如图所示。此过程里溶液中离子浓度的关系错误的是
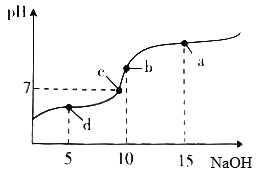
A. a点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. b点: c(H+)= c(CH3COOH)+c(OH-)
C. c点:c(Na+)= c(CH3COO-)>c(H+)=c(OH-)
D. d点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
高三化学选择题困难题查看答案及解析
-
常温下,向10mL0.1mol·L-1H2A溶液中逐滴加入0.1mol·L-1NaOH溶液。有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。根据图示分析判断,下列微粒浓度大小关系正确的是
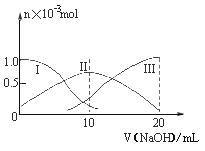
A. 当v=0时,c(H+)=c(OH-)+c(HA-)+c(A2-)
B. 当v=10时,c(Na+)=c(H2A)+c(HA-)+c(A2-)
C. 当v=20时,c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+)
D. 当pH=7时,c(Na+)>c(HA-)+ c(A2-)
高三化学选择题中等难度题查看答案及解析
-
某化学小组设计了如图所示的数字化实验装置,研究常温下,向30mL0.1mol·L-1H2A溶液中逐滴加入等浓度NaOH溶液时pH的变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系(如图所示),下列说法错误的是( )
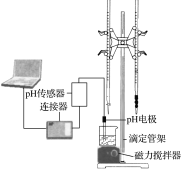
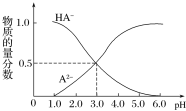
A.pH=4.0时,溶液中n(HA-)约为2.73×10-4mol
B.该实验应将左边的酸式滴定管换成右边的碱式滴定管
C.常温下,含有等物质的量浓度的NaHA与Na2A的混合溶液:pH=3.0
D.0.1mol·L-1NaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol·L-1
高三化学单选题中等难度题查看答案及解析
-
25℃时,向20mL0.1mol·L-1H3PO2溶液中滴加0.1mol·L-1的NaOH溶液,滴定曲线如图1,含磷微粒物质的量浓度所占分数(δ)随pH变化关系如图2。下列说法不正确是
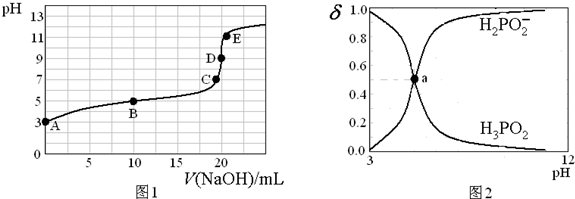
A. H3PO2的电离方程式为H3PO2
H2PO2-+H+ Ka≈10-5
B. B点时,溶液中存在关系:2c(H+)+c(H2PO2-)=2c(OH-)+c(H3PO2)
C. C点时,溶液中存在关系:c(Na+)+c(H+)=C(H2PO2-)+c(OH-)
D. D点时,溶液中微粒浓度大小关系:c(Na+)>c(H2PO2-)>c(OH-)>c(H+)
高三化学选择题困难题查看答案及解析
-
常温下,含碳微粒
、
、
存在于
草酸溶液与等浓度NaOH溶液反应后的溶液中,它们的物质的量分数
某微粒物质的量浓度与三种微粒物质的量浓度和比值
与溶液pH的关系如图所示,下列有关说法错误的是
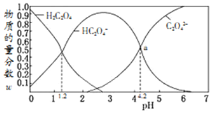
A.向
的溶液中加NaOH 溶液将pH增大至
的过程中水的电离度一直增大
B.
时,溶液中c
C.
若草酸的第二级电离平衡常数为
,则
D.将
相同物质的量浓度
和
的两份溶液等体积混合,可配得图a点所示混合液
高三化学单选题中等难度题查看答案及解析