制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现( )
|
②
对上述两个反应的下列叙述中,错误的是
A. 两个反应都是置换反应 B. 两个反应都是氧化还原反应
C. 两个反应互为可逆反应 D. 反应②是放热反应
高二化学选择题简单题
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现( )
|
②
对上述两个反应的下列叙述中,错误的是
A. 两个反应都是置换反应 B. 两个反应都是氧化还原反应
C. 两个反应互为可逆反应 D. 反应②是放热反应
高二化学选择题简单题
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现( )
|
②
对上述两个反应的下列叙述中,错误的是
A. 两个反应都是置换反应 B. 两个反应都是氧化还原反应
C. 两个反应互为可逆反应 D. 反应②是放热反应
高二化学选择题简单题查看答案及解析
工业上由粗硅制取高纯硅有以下反应:①Si(s)+3HCl(g)=SiHCl3(g)+H2(g) ΔH=-381 kJ·mol-1;
②SiHCl3(g)+H2(g)=Si(s)+3HCl(g)。对上述反应的说法中正确的是( )。
A.均为置换反应和氧化还原反应
B.反应①、②实际上互为可逆反应
C.由于反应①放热,则反应②可能是吸热的,也可能是放热的
D.提高SiHCl3产率,应采用加压和升温的办法
高二化学选择题中等难度题查看答案及解析
制太阳能电池需要高纯硅,工业上用粗硅制高纯硅可通过以下反应实现:
①Si+3HCl(气) SiHCl3(气)+H2 ②SiHCl3(气)+H2
Si+3HCl(气)
对上述两个反应的叙述错误的是
A.都是置换反应 B.都是氧化还原反应
C.反应中硅元素都被还原 D.都不是离子反应
高二化学单选题中等难度题查看答案及解析
高二化学选择题中等难度题查看答案及解析
烯烃存在顺反异构现象,已知:
① △H=-119.6kJ/mol
② △H=-115.6kJ/mol
下列说法中正确的是
A.上述两个反应中,反应物的总能量均低于生成物的总能量
B.上述两个反应中,破坏旧键需要的能量均大于形成新键所释放的能量
C.从上述反应热数据可知顺-2-丁烯比反-2-丁烯稳定
D.顺-2-丁烯转化为反-2-丁烯的反应热可表示为
△H=-4.0kJ/mol
高二化学选择题简单题查看答案及解析
甲醇是一种用途广泛的化工原料,也可作为燃料。请回答以下问题:
(1)工业上常用下列反应制备甲醇:CO(g) + 2H2(g) CH3OH(g) ΔH= —90.1KJ•mol-1,该反应自发的条件是________。
(2)实验室模拟用CO和H2反应来制甲醇。在250℃下,将一定量的CO和H2投入2L的密闭容器中,各物质的物质的量(mol)变化如下表所示:(前6min没有改变条件)
| 2min | 4min | 6min | 8min | 20min | … | |
| CO | 0.7 | 0.5 | 0.5 | 0.4 | 0.2 | … |
| H2 | 1.4 | 1 | 1 | 1.8 | 2 | … |
| CH3OH | 0.3 | 0.5 | 0.5 | 0.6 | 0.8 | … |
①从0min-4min这段时间的反应速率v(CO)=_________
②250℃时该反应平衡常数K的值为________。
③若第6min时只改变了一个条件,则所改变的条件是________。
④若反应过程中保持温度不变,第20min时,该反应的v正______v逆。(填“ > ”,“ < ”或“ = ”)
(3)若在一恒容的密闭容器中通入物质的量之比为1:1的CO和H2来生产CH3OH,画出不同温度下,反应相同时间时CO的体积分数随温度变化的图像。_______________
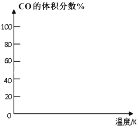
高二化学综合题中等难度题查看答案及解析
化工生产中常用的CO和H2,可通过烃与水蒸气反应得到。其中甲烷可发生以下两个反应:
①CH4(g)+1/2O2(g)== =2H2(g)+CO(g) ΔH=-36 kJ/mol
②CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+216 kJ/mol
下列热化学方程式中,反应热为零的是
A.4CH4(g)+O2(g)+2H2O(g)===4CO(g)+10H2(g)
B.7CH4(g)+3O2(g)+H2O(g)===7CO (g)+15H2(g)
C.3CH4(g)+O2(g)+H2O(g)===3CO(g)+7H2(g)
D.5CH4(g)+2O2(g)+H2O(g)===5CO(g)+11H2(g)
高二化学选择题简单题查看答案及解析
化工生产中常用的CO和H2,可通过烃与水蒸气反应得到。其中甲烷可发生以下两个反应:
①CH4(g)+1/2O2(g)== =2H2(g)+CO(g) ΔH=-36 kJ/mol
②CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+216 kJ/mol
下列热化学方程式中,反应热为零的是
A.4CH4(g)+O2(g)+2H2O(g)===4CO(g)+10H2(g)
B.7CH4(g)+3O2(g)+H2O(g)===7CO (g)+15H2(g)
C.3CH4(g)+O2(g)+H2O(g)===3CO(g)+7H2(g)
D.5CH4(g)+2O2(g)+H2O(g)===5CO(g)+11H2(g)
高二化学单选题简单题查看答案及解析
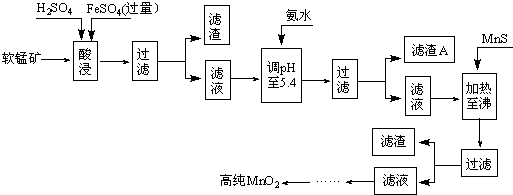
(10分)二氧化锰是制造锌锰干电池的基本原料,普通锌锰干电池的电池反应式为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2。工业上以软锰矿为原料,利用硫酸亚铁制备高纯度二氧化锰的流程如下(软锰矿中所有金属元素在酸性条件下均以阳离子形式存在):
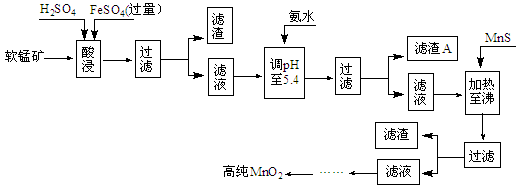
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.24%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 |
| 沉淀物 | CuS | ZnS | MnS | FeS | ||
| Ksp | 8.5×10-45 | 1.2×10-23 | 1.4×10-15 | 3.7×10-14 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要离子方程式为:
________。
(2)滤渣A的主要成分为。
(3)加入MnS的目的是除去________杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应式为________ 。
(5)从废旧碱性锌锰电池中可回收利用的物质有________(写两种)。
高二化学填空题简单题查看答案及解析
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 |
| 沉淀物 | CuS | ZnS | MnS | FeS | ||
| Ksp | 8.5×10-45 | 1.2×10-23 | 1.4×10-15 | 3.7×10-14 |
高二化学解答题中等难度题查看答案及解析