近年来研制的NH3气体可用作氟化氢一氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2 NF3+3H4F,下列说法不正确的是
A.NF3的形成过程用电子式可表示为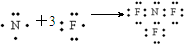
B.NF3的氧化性大于F2
C.NF3分子空间构型为三角锥形
D.NH4F中既有离子键又有极性共价键
高三化学选择题中等难度题
近年来研制的NH3气体可用作氟化氢一氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2 NF3+3H4F,下列说法不正确的是
A.NF3的形成过程用电子式可表示为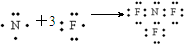
B.NF3的氧化性大于F2
C.NF3分子空间构型为三角锥形
D.NH4F中既有离子键又有极性共价键
高三化学选择题中等难度题
近年来研制的NH3气体可用作氟化氢一氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2 NF3+3H4F,下列说法不正确的是
A.NF3的形成过程用电子式可表示为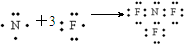
B.NF3的氧化性大于F2
C.NF3分子空间构型为三角锥形
D.NH4F中既有离子键又有极性共价键
高三化学选择题中等难度题查看答案及解析
三氟化氮(NF3)是一种无色无味的气体,可由氟与氨反应制得。
(1)该反应的方程式为NH3+F2→NF3+NH4F,配平方程式并标明电子转移的方向和数目。
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:___________________________________。
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是________。
高三化学填空题简单题查看答案及解析
氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用。
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
N2(g)+O2(g)=2NO(g) ΔH1=+229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH2=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ΔH3
则ΔH3 = kJ·mol-1
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程产生的气体无毒,写出该反应的离子方程式
(3)在微电子工业中,NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。
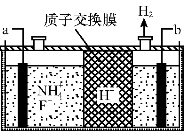
氮化硅的化学式为
a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式
高三化学填空题困难题查看答案及解析
三氟化氮(NF3)常用于微电子工业,可用以下反应制备:4NH3+3F2=NF3+3NH4F,下列说法中,正确的是( )
A.NF3的电子式为
B.NH4F分子中仅含离子键
C.在制备NF3的反应中,NH3表现出还原性
D.在制备NF3的反应方程式中,各物质均为共价化合物
高三化学单选题中等难度题查看答案及解析
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1) 利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4= kJ·mol-1。
(2) 使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
① 写出该反应的离子方程式: 。
② 在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为: ;为抑制肼的分解,可采取的合理措施有 (任写一种)。
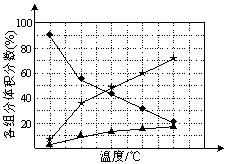
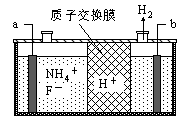
图1 图2
(3) 在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
① 氮化硅的化学式为 。
② a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式: ;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是 。
高三化学填空题极难题查看答案及解析
(15分)氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g) △H1=44.0 kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=229.3 kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-906.5 kJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H4
则△H4= kJ·mol-1。
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式: 。
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为: ;为抑制肼的分解,可采取的合理措施有 (任写一种)。
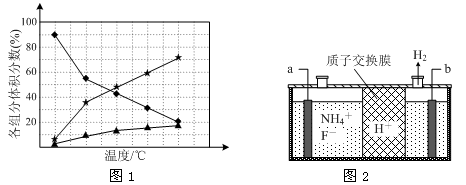
(3)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①氮化硅的化学式为 。
②a电极为电解池的 (填“阴”或“阳”)极,写出该电极的电极反应式: ;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是 。
高三化学简答题困难题查看答案及解析
三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(1)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。NH3的电子式为 _______ ,反应中氨气显示的化学性质有_____________,当有17.0g氨气发生反应时,转移电子的物质的量为_______。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为 ___________,NF3、F2、NO三种气体氧化性由弱到强的顺序为____________。
(3)三氟化氮在空气中泄漏时,很容易被发现,依据的现象是_______________________ 。
(4)NCl3的结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,且反应为非氧化还原反应,该反应的化学方程式为______________________________ 。
高三化学填空题中等难度题查看答案及解析
氮的重要化合物如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用.
(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4
则△H4=_____________kJ•mol-1.
(2)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式:_____________;
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为:_____________;为抑制肼的分解,可采取的合理措施有_____________(任写一种)。
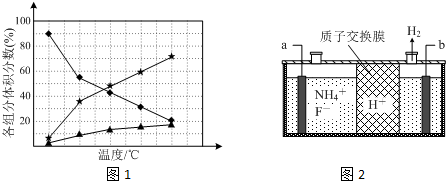
(3)在微电子工业中NF3常用作半导体、液晶和薄膜太阳能电池等生产过程的蚀刻剂,在对硅、氮化硅等材料进行蚀刻时具有非常优异的蚀刻速率和选择性,在被蚀刻物表明不留任何残留物,对表面物污染。工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。
①a电极为电解池的_____________(填“阴”或“阳”)极,写出该电极的电极反应式:_____________;
②以NF3对氮化硅(Si3N4)材料的蚀刻为例,用反应方程式来解释为什么在被蚀刻物表面不留任何残留物_____________。
③气体NF3不可燃但可助燃,故气体NF3应远离火种且与还原剂、易燃或可燃物等分开存放,结构决定性质,试从结构角度加以分析_____________。
④能与水发生反应,生成两种酸及一种气态氧化物,试写出相应的化学方程式_____________。
高三化学填空题极难题查看答案及解析
三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(l)三氟化氮可由氨气和氟气反应得到: 4NH3+3F2=NF3+3NH4F。NH3的电子式为__________,反应中氨气显示的化学性质有______________,当有17.0 g氨气发生反应时,转移电子的物质的量为_____。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为_________,NF3、F2、NO三种气体氧化性由弱到强的顺序为_________。
(3)三氟化氮在空气中泄露时,很易被发现,依据的现象是______________________。
(4)NCl3结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,目反应为非氧化还原反应,该反应的化学方程式为____________________________。
高三化学填空题中等难度题查看答案及解析
三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一。
(l)三氟化氮可由氨气和氟气反应得到: 4NH3+3F2=NF3+3NH4F。NH3的电子式为__________,反应中氨气显示的化学性质有______________,当有17.0 g氨气发生反应时,转移电子的物质的量为_____。
(2)在潮湿的空气中,NF3能与水蒸气发生反应,产物有HF、NO和一种酸,则被氧化与被还原元素原子的物质的量之比为_________,NF3、F2、NO三种气体氧化性由弱到强的顺序为_________。
(3)三氟化氮在空气中泄露时,很易被发现,依据的现象是______________________。
(4)NCl3结构类似NF3,但NCl3中N元素显-3价,NCl3遇水发生反应,目反应为非氧化还原反应,该反应的化学方程式为____________________________。
高三化学填空题中等难度题查看答案及解析