-
某研究性学习小组对用酸化的硝酸银溶液检验I-存在的合理性产生了兴趣,同学们根据变量控制思想进行如下方案设计并进行了实验探究:
[提出假设]
假设1:生成的AgI不溶于水,不能被HNO3氧化。
假设2:HNO3有氧化性,能将I-氧化成I2。
[设计实验方案,验证假设]
(1)甲同学向KI溶液中滴加硝酸化的AgNO3溶液并振荡,有黄色沉淀生成。验证了假设1成立。请写出有关化学方程式________。
(2)乙同学设计实验验证2,请帮他完成下表中内容。
实验步骤(不要求写具体操作过程)
预期现象和结论
若溶液变蓝,假设2成立。
若溶液不变蓝,假设2不成立。
……
[结论与解释]
(3)甲同学验证了假设1成立,若乙同学验证了假设2成立,则丙同学由此得出的结论:硝酸酸化的AgNO3可以使I-沉淀,也能氧化I-。你同意丙同学的结论吗,并简述理由:。
[思考与交流]
(3)研究性学习小组同学还想研究Fe3+能否氧化I-的问题,请你用两种方案来进行实验验证:
方案一:________
方案二:
假设验证成立,请写出主要离子方程式________。
高三化学实验题困难题查看答案及解析
-
某兴趣小组探究SO2气体的还原性,装置如图所示,下列说法不合理的是
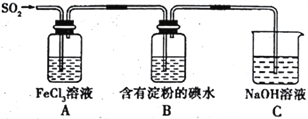
A. 为了验证A 中发生了氧化还原反应,加入稀盐酸酸化的BaCl2溶液,产生白色沉淀
B. 该实验装置至少存在一处设计缺陷
C. 向反应后的A 溶液中加入酸性KMnO4溶液,紫红色褪去,说明一定有Fe2+
D. 装置B是为了验证还原性: SO2>I-
高三化学单选题中等难度题查看答案及解析
-
某研究性学习小组在整理实验室化学试剂时,发现一瓶盛有无色溶液的试剂,标签破损,如图。某同学根据中学化学知识,对该溶液中的溶质成分进行如下预测和验证,其中错误的是(包括预测物质的化学式、检验需要的试剂、操作、现象及结论)
选项
预测物质
的化学式
检验需要的试剂
操作、现象及结论
A
Na2SO4
稀盐酸、氯化钡溶液
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液
B
Na2CO3
稀盐酸、
澄清的石灰水
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液
C
Na2SO3
稀盐酸、澄清的
石灰水、品红溶液
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液
D
Na2SiO3
过量稀盐酸
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液
高三化学选择题困难题查看答案及解析
-
某研究性学习小组在整理实验室化学试剂时,发现一瓶盛有无色溶液的试剂,标签破损,如图.某同学根据中学化学知识,对该溶液中的溶质成分进行如下预测和验证,其中错误的是(包括预测物质的化学式、检验需要的试剂、操作、现象及结论)( )
选项
预测物质的化学式
检验需要的试剂
操作、现象及结论
A
Na2SO4
稀盐酸、氯化钡溶液
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液
B
Na2CO3
稀盐酸、澄清的石灰水
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液
C
Na2SO3
稀盐酸、澄清的石灰水、品红溶液
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液
D
Na2SiO3
过量稀盐酸
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液
高三化学选择题极难题查看答案及解析
-
某研究性学习小组在整理实验室化学试剂时,发现一瓶盛有无色溶液的试剂,标签破损,如图.某同学根据中学化学知识,对该溶液中的溶质成分进行如下预测和验证,其中错误的是(包括预测物质的化学式、检验需要的试剂、操作、现象及结论)( )
选项 预测物质的化学式 检验需要的试剂 操作、现象及结论 A Na2SO4 稀盐酸、氯化钡溶液 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液 B Na2CO3 稀盐酸、澄清的石灰水 取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液 C Na2SO3 稀盐酸、澄清的石灰水、品红溶液 取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液 D Na2SiO3 过量稀盐酸 取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液 
A.A
B.B
C.C
D.D高三化学选择题中等难度题查看答案及解析
-
某研究性学习小组在整理实验室化学试剂时,发现一瓶盛有无色溶液的试剂,标签破损,如图.某同学根据中学化学知识,对该溶液中的溶质成分进行如下预测和验证,其中错误的是(包括预测物质的化学式、检验需要的试剂、操作、现象及结论)( )
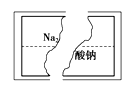
选项
预测物质的化学式
检验需要的试剂
操作、现象及结论
A
Na2SO4
稀盐酸、氯化钡溶液
取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入氯化钡溶液,如果产生白色沉淀,则原溶液是Na2SO4溶液
B
Na2CO3
稀盐酸、澄清的石灰水
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体能使澄清的石灰水变浑浊,则原溶液一定是Na2CO3溶液
C
Na2SO3
稀盐酸、澄清的石灰水、品红溶液
取少量该溶液于试管中,滴入足量稀盐酸,如果产生的无色气体既能使澄清的石灰水变浑浊,还能使品红溶液褪色,则原溶液是Na2SO3溶液
D
Na2SiO3
过量稀盐酸
取少量该溶液于试管中,滴入稀盐酸,产生白色胶状沉淀,盐酸过量时沉淀不溶解,则原溶液是Na2SiO3溶液
高三化学选择题困难题查看答案及解析
-
实验能力和创新意识是化学学科核心素养的重要内容之一。某研究性学习小组在验证反应“ Fe
”的实验中检测到
发现和探究过程如下:向硝酸酸化的
硝酸银溶液(
)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物:
①检验上层清液中所含离子的方法:取上层清液,滴加_________,产生蓝色沉淀,说明溶液中含有Fe2+。
②经检验黑色固体为Ag,检验方法:取出少量黑色固体,洗涤后,加入适量稀硝酸使固体溶解,再滴加__________(填试剂),产生_________(填现象)。
(2)针对“溶液呈黄色”,甲认为溶液中有
乙认为铁粉过量时不可能有
,乙依据的原理是______。(用离子方程式表示)o
针对这两种观点继续实验:取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号
取样时间/min
现象
I
3
产生大量白色沉淀;溶液呈红色
II
30
产生白色沉淀,较3 min时量少;溶液红色较3 min时加深
III
120
产生白色沉淀,较30min时量少;溶液红色较30min时变浅
(资料:
-生成白色沉淀AgSCN)
(3)实验中溶液变为红色的离子方程式为_______________,产生白色沉淀说明存在___________(填离子符号)。
(4)对
产生的原因做如下假设:
假设a:可能是铁粉表面有氧化层,能产生
假设b:空气中存在
发生反应
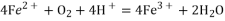 产生
产生假设c:酸性溶液中的NO3-将Fe2+氧化为Fe3+
假设d:溶液存在Ag+将Fe2+氧化为Fe3+
下述实验可证实假设a、b,c不是产生Fe3+的主要原因,并可证实假设d成立。
①实验:向硝酸酸化的__________溶液(
)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液。3min 时溶液呈浅红色,30min后溶液几乎无色。
②实验II的现象说明发生了反应__________(用离子方程式表示)。
(5)实验Ⅱ中发生的反应可以用下列装置来验证。其中甲溶液是___________,分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,_______ (“前者”或“后者”)红色更深。
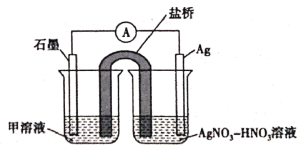
高三化学实验题中等难度题查看答案及解析
-
实验能力和创新意识是化学学科核心素养的重要内容之一。某研究性学习小组在验证反应“ Fe
”的实验中检测到
发现和探究过程如下:向硝酸酸化的
硝酸银溶液(
)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物:
①检验上层清液中所含离子的方法:取上层清液,滴加_________,产生蓝色沉淀,说明溶液中含有Fe2+。
②经检验黑色固体为Ag,检验方法:取出少量黑色固体,洗涤后,加入适量稀硝酸使固体溶解,再滴加__________(填试剂),产生_________(填现象)。
(2)针对“溶液呈黄色”,甲认为溶液中有
乙认为铁粉过量时不可能有
,乙依据的原理是______。(用离子方程式表示)o
针对这两种观点继续实验:取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号
取样时间/min
现象
I
3
产生大量白色沉淀;溶液呈红色
II
30
产生白色沉淀,较3 min时量少;溶液红色较3 min时加深
III
120
产生白色沉淀,较30min时量少;溶液红色较30min时变浅
(资料:
-生成白色沉淀AgSCN)
(3)实验中溶液变为红色的离子方程式为_______________,产生白色沉淀说明存在___________(填离子符号)。
(4)对
产生的原因做如下假设:
假设a:可能是铁粉表面有氧化层,能产生
假设b:空气中存在
发生反应
产生
假设c:酸性溶液中的NO3-将Fe2+氧化为Fe3+
假设d:溶液存在Ag+将Fe2+氧化为Fe3+
下述实验可证实假设a、b,c不是产生Fe3+的主要原因,并可证实假设d成立。
①实验:向硝酸酸化的__________溶液(
)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液。3min 时溶液呈浅红色,30min后溶液几乎无色。
②实验II的现象说明发生了反应__________(用离子方程式表示)。
(5)实验Ⅱ中发生的反应可以用下列装置来验证。其中甲溶液是___________,分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,_______ (“前者”或“后者”)红色更深。
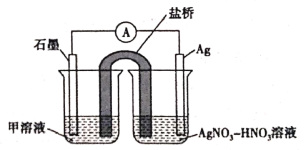
高三化学实验题中等难度题查看答案及解析
-
实验能力和创新意识是化学学科核心素养的重要内容之一。某研究性学习小组在验证反应“ Fe
”的实验中检测到
发现和探究过程如下:向硝酸酸化的
硝酸银溶液(
)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物:
①检验上层清液中所含离子的方法:取上层清液,滴加_________,产生蓝色沉淀,说明溶液中含有Fe2+。
②经检验黑色固体为Ag,检验方法:取出少量黑色固体,洗涤后,加入适量稀硝酸使固体溶解,再滴加__________(填试剂),产生_________(填现象)。
(2)针对“溶液呈黄色”,甲认为溶液中有
乙认为铁粉过量时不可能有
,乙依据的原理是______。(用离子方程式表示)o
针对这两种观点继续实验:取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号
取样时间/min
现象
I
3
产生大量白色沉淀;溶液呈红色
II
30
产生白色沉淀,较3 min时量少;溶液红色较3 min时加深
III
120
产生白色沉淀,较30min时量少;溶液红色较30min时变浅
(资料:
-生成白色沉淀AgSCN)
(3)实验中溶液变为红色的离子方程式为_______________,产生白色沉淀说明存在___________(填离子符号)。
(4)对
产生的原因做如下假设:
假设a:可能是铁粉表面有氧化层,能产生
假设b:空气中存在
发生反应
产生
假设c:酸性溶液中的NO3-将Fe2+氧化为Fe3+
假设d:溶液存在Ag+将Fe2+氧化为Fe3+
下述实验可证实假设a、b,c不是产生Fe3+的主要原因,并可证实假设d成立。
①实验:向硝酸酸化的__________溶液(
)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液。3min 时溶液呈浅红色,30min后溶液几乎无色。
②实验II的现象说明发生了反应__________(用离子方程式表示)。
(5)实验Ⅱ中发生的反应可以用下列装置来验证。其中甲溶液是___________,分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,_______ (“前者”或“后者”)红色更深。
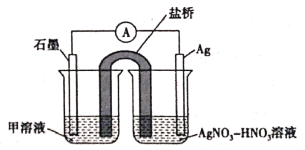
高三化学实验题中等难度题查看答案及解析
-
某兴趣小组为了分析电解硝酸溶液时放电的离子,设计了如图装置进行实验(石墨电极)。电解过程中,X极产生了红棕色气体,则下列说法不合理的是
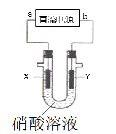
A.a极为负极,b极为正极
B.电解时,Y极附近溶液pH降低
C.相同条件下,阴阳两极气体体积比是2:1
D.X极的电极反应式是:2H++ NO3-+ e-=NO2↑ + H2O
高三化学选择题困难题查看答案及解析