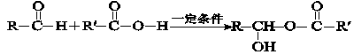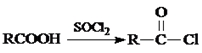-
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)工业上可利用CO生产乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又知:H2O(l)=H2O(g) ΔH2
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH=____________。
(2)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
A.v(H2)正=2v(CO)逆 B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变 D.CH3OCH3和H2O的体积之比不随时间而变化
(3)工业可采用CO与H2反应合成再生 能源甲醇,反应:CO(g)+2H2(g)
能源甲醇,反应:CO(g)+2H2(g) CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
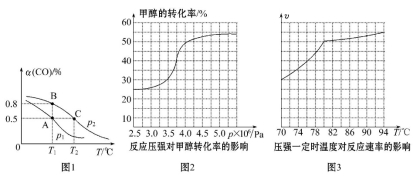
①合成甲醇的反应为______________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为____________________。p1和p2的大小关系为___________。
③若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为CH3OH(g)+CO(g) HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是________(填“3.5×106Pa”“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是___________________。
-
煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)工业上可利用CO生产乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又已知:H2O(l)=== H2O(g) ΔH2
CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则:ΔH与ΔH1、ΔH2、ΔH3之间的关系是:ΔH=_______________________。
(2)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:
4H2(g)+2CO(g) CH3OCH3(g)+H2O(g),
CH3OCH3(g)+H2O(g),
下列选项能判断该反应达到平衡状态的依据的有_____________。
A.v(H2)= 2 v(CO)
B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量不随时间而变化
(3)工业可采用CO与H2反应合成再生能源甲醇,反应:
CO(g)+ 2H2(g) CH3OH(g)
CH3OH(g)
在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如下图所示。
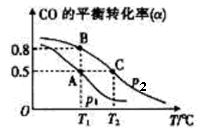
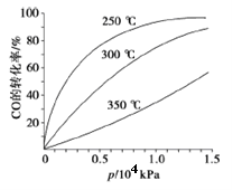
①合成甲醇的反应为___________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为___________。P1和P2的大小关系为___________。
③若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为______L。
④CO的平衡转化率(α)与温度(T)、压强(p)的关系如下图所示,实际生产时条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是__________________。
-
(有机化学基础,15分)
甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知:
(1)写出F 的结构简式 ________ ,其核磁共振氢谱图中有________个吸收峰。
(2)写出D分子式 ________,官能团名称 ________。
(3)写出下列方程式,并注明反应类型。
① A→B : ________ ,反应类型 ________
② I→J :________ ,反应类型 ________ .
(4)E 、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式:
要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
①________;②________;③________;④________。
-
(共14分)氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料。
(1)以氨为燃料可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为 。
(2)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2 2NH3。该可逆反应达到平衡的标志是________________。
2NH3。该可逆反应达到平衡的标志是________________。
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间变化
E.a molN≡N键断裂的同时,有6amolN—H键断裂
F.N2、H2、NH3的分子数之比为1∶3∶2
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25min时,以N2表示的平均反应速率= ;该温度下平衡常数K= ;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g) == NH2CO2 NH4(s) △H= —l59.5 kJ/mol
②NH2CO2NH4(s)  CO(NH2)2(s)+H2O(g) △H=+116.5 kJ/mol
CO(NH2)2(s)+H2O(g) △H=+116.5 kJ/mol
③H2O(1) == H2O(g) △H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 ;
对于上述反应②在密闭容器中将过量NH2CO2NH4固体于300K下分解,平衡时P[H2O(g)]为a Pa,若反应温度不变,将体系的体积增加50%,则P[H2O(g)]的取值范围是_________________(用含a的式子表示)。(分压=总压×物质的量分数)
-
充分利用碳的氧化物合成化工原料,既可以减少环境污染和温室效应,又能变废为宝。
Ⅰ.CO2的综合利用是解决温室效应及能源问题的有效途径。
(1)O2和H2在催化剂存在下可发生反应生成CH3OH。已知CH3OH、H2的燃烧热分别为△H1=-akJ·mol-1、△H2=-bkJ·mol-1,且1mol水蒸气转化为液态水时放出ckJ的热量。
则CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=___________kJ·mol-1。
CH3OH(g)+H2O(g)△H=___________kJ·mol-1。
(2)对于CO2(g)+3H2(g) CH3OH(g)+H2O(g).控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇产率的影响如图所示。由图可知获取CH3OH最适宜的温度是___________,下列有利于提高CO2转化为CH3OH的平衡转化率的措施是___________。
CH3OH(g)+H2O(g).控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇产率的影响如图所示。由图可知获取CH3OH最适宜的温度是___________,下列有利于提高CO2转化为CH3OH的平衡转化率的措施是___________。
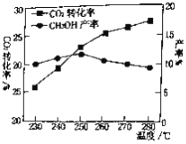
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
Ⅱ.CO是合成尿素、甲酸的原料。
(3)合成尿素的反应:2NH3(g)+CO(g) CO(NH2)2(g)+H2(g)△H=-81.0kJ·mol-1。
CO(NH2)2(g)+H2(g)△H=-81.0kJ·mol-1。
①T℃时,在体积为2L的恒容密闭容器中,将2molNH3和1molCO混合发生反应,5min时,NH3的转化率为80%。则0~5min内的平均反应速率为v(CO)=___________。
②已知:
| 温度/K | 398 | 498 | … |
| 平衡常数/K | 126.5 | K1 | … |
则:K1___________126.5(填“>”或“<”);其判断理由是___________。
(4)通过人工光合作用可将CO转化成HCOOH。
①已知常温下,浓度均为0.1mol·L-1的HCOOH和HCOONa混合溶液pH=3.7,则HCOOH的电离常数Ka的值为___________ (已知lg2=0.3)。
②用电化学可消除HCOOH对水质造成的污染,其原理是电解CoSO4、稀硫酸和HCOOH混合溶液,用电解产生的Co3+将HCOOH氧化成CO2。Co3+氧化HCOOH的离子方程式为___________;忽略体积变化,电解前后Co2+的浓度将___________ (填“增大”“减小”或“不变”)。
-
硫酸的工业制备是一个重要的化工生产过程,但在生产过程中会产生大量污染,需要在生产工艺中考虑到绿色工艺。
I尾气的吸收和综合利用。
以工业制硫酸的尾气、氨水、石灰石、焦炭、碳酸氯铵和KCI为原料可以合成硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
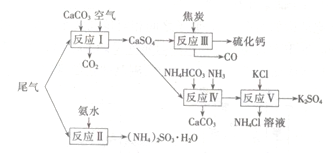
(1)反应III中氧化剂与还原剂的物质的量之比为 。
(2)反应Ⅳ的化学方程式为 。
(3)反应V在25℃、40%的乙二醇溶液中进行,该反应能顺利进行的原因为 。
Ⅱ催化剂的回收利用。
SO2的催化氧化所使用的催化剂为V2O5,实际生产中,催化剂在使用一段时间后,会含有V2O5、VOSO4和SiO2等,其中VOSO4。能溶于水。回收V2O5,的主要流程如下:
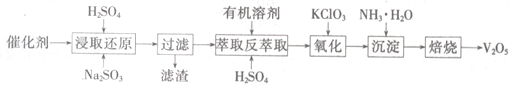
(4)若反萃取使用的硫酸用量过大,进一步处理时会增加____ 的用量。
(5)浸取还原过程的产物之一是VOSO4,反应的化学方程式为 。
氧化过程的化学方程式为KClO3+6VOSO4+3H2SO4= 2(VO)2(SO4)3+KCl+3H2O;若两步所用试剂Na2SO3与KC1O3的物质的量之比为12:7,则该催化剂中V2O5、VOSO4的物质的量之比为 。
-
【选修5—有机化学基础】(12分)石油化工的重要原料CxHy 可以合成很多有机化合物,以下是CxHy合成物质E和J的流程图:
可以合成很多有机化合物,以下是CxHy合成物质E和J的流程图:
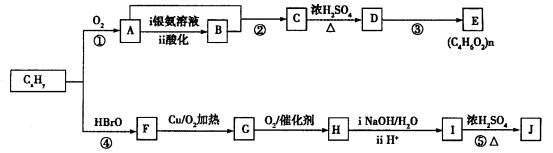
已知:
Ⅰ.下列反应中R、 代表烃基
代表烃基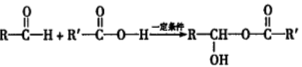
Ⅱ.J的分子式为C4H4O4,是一种环状化合物。
(1)在CxHy的同系物中,所有碳原子一定共平面且碳原子数最多的分子的名称____________。
(2)下列说法正确的是_________________________。
a.CxHy和苯都能使溴水褪色,原理相同
b.反应②和反应④的反应类型均为加成反应
c.C能与Na、NaOH、NaHCO3反应
d.E是一种水溶性很好的高分子化合物
e.J在酸性或碱性环境中均能水解
(3)K是J的同分异构体,且1 mol K与足量的NaHCO3溶液反应可放出2molCO2气体,符合条件的K结构有_____________种。
(4)写出反应⑤的化学方程式_________________。
(5)D有多种同分异构体,与D具有相同官能团的还有_____________种(含顺反异构体),其中核磁共振氢谱有3组吸收峰,且能发生银镜反应的结构简式是_____________。
-
【化学—选修5有机化学基础】石油化工的重要原料CxHy可以合成很多有机化合物,以下是CxHy合成物质E和J的流程图:

已知:Ⅰ.下列反应中R、R′代表烃基
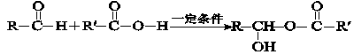
Ⅱ.J的分子式为C4H4O4 ,是一种环状化合物。
(1)在CxHy的同系物中,所有碳原子一定共平面且碳原子数最多的分子的名称是____。
(2)H的分子式是 。
(3)下列说法正确的是 。
a.CxHy和苯都能使溴水褪色,原理相同
b.反应②和反应④的反应类型均为加成反应
c.C能与Na、NaOH、NaHCO3反应
d.E是一种水溶性很好的高分子化合物
e.J在酸性或碱性环境中均能水解
(4)K是J的同分异构体,且1 mol K与足量的NaHCO3溶液反应可放出2mol CO2气体,请写出两种符合条件K的结构简式____。
(5)写出反应⑤的化学方程式______________。
(6)D有多种同分异构体,与D具有相同官能团的还有种(含顺反异构体),其中核磁共振氢谱有3组吸收峰,且能发生银镜反应的结构简式是__________。
-
【化学──有机化学基础】(15分)PX是有机物A的英文缩写, 是化工生产中非常重要的原料之一,常用于生产塑料、聚酯纤维、薄膜、药物等,有研究者设计利用其性质合成某药物,其合成路线如下(部分反应试剂和条件已略):
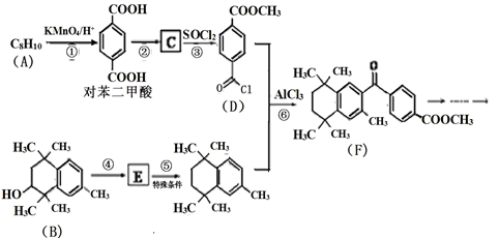
已知:Ⅰ.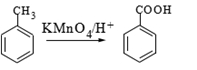
Ⅱ.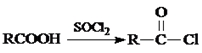
试回答下列问题:
(1)PX即原料A的结构简式为 。
(2)F分子中含氧官能团的名称为 、 。
(3)反应①、⑥所属的反应类型分别为 、 。
(4)反应④的化学方程式为___________________________。
(5)G是对苯二甲酸的同系物,分子量比对苯二甲酸大14 ,G有多种同分异构体,则同时符合下列条件的同分异构体有 种。
a.属于芳香族化合物
b.能与NaHCO3 溶液反应产生气体
c.能发生水解反应和银镜反应
(6)由A和乙烯为原料可以合成目前世界上产量最高的合成纤维——聚酯纤维(聚对苯二甲酸乙二醇酯),合成路线如下:
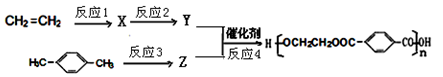
反应3的试剂为____________。
反应2和反应4的化学方程式分别为___________________、________________________。
-
CO在工农业生产中有着重要的应用。
(1)CO是制备很多有机物(如甲醇、乙醇、甲醚等)的原料,现用CO与H2合成甲醇,反应如下:CO(g)+2H2(g)= CH3OH(g) △H=-99kJ•mol–1。
①已知断裂1molCO(g)中的化学键消耗的能量为1072kJ,断裂1molH2(g)中的化学键消耗的能量为436kJ,则形成1molCH3OH(g)中化学键释放的能量为_____。
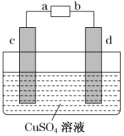
②用CH3OH 燃料电池电解精炼粗铜,装置如图所示。当消耗1mol甲醇时,d极质量增加了160g,则甲醇应加入____(填“a”或“b”)极,该电池的能量转化率为________(保留3位有效数字)。
(2)CO与Ni发生羰化反应形成的络合物可作为催化烯烃反应的催化剂。Ni的羰化反应为Ni(s)+4CO(g) Ni(CO)4(g) △H<0,T0温度下,将足量的Ni粉和3.7molCO加入到刚性密闭容器中,10min时反应达到平衡,测得体系的压强为原来的
Ni(CO)4(g) △H<0,T0温度下,将足量的Ni粉和3.7molCO加入到刚性密闭容器中,10min时反应达到平衡,测得体系的压强为原来的 倍。则:
倍。则:
①0~10min内平均反应速率v(Ni)=________g•min–1。
②研究表明正反应速率v正=k正•x4(CO),逆反应速率v逆 =k逆•x[Ni(CO)4](k正和k逆分别表示正反应和逆反应的速率常数,x为物质的量分数),则T0温度下, =_____。
=_____。
③当温度升高时k正_______k逆(填“大于”“小于”或“等于”),此时CO的转化率___________(填“变大”“变小”或“不变”)。
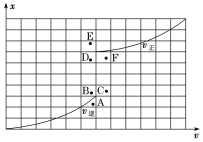
④T1温度下测得一定的实验数据,计算得到v正~x(CO)和v逆~x[Ni(CO)4]的关系可用如图进行表示。当降低温度时,反应重新达到平衡,相应的点分别为______、______。
CH3CH2OH(g)+H2O(g) ΔH1
CO2(g)+H2(g) ΔH3
CH3CH2OH(g)+3H2O(l) ΔH
CH3OCH3(g)+H2O(g),
CH3OH(g)