-
铁及其化合物在生产生活及科研中应用广泛。
(1)聚合硫酸铁的化学式为[ ]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。
]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。
(2)Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3[Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为_______,1mol [Fe(CN)6]3-离子中含有σ键的数目为__________。
②已知N3-与CS2为等电子体,则N3-的空间构型为_________。
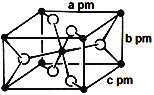
(3)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=_________g·cm-3。(列出计算式即可)(1pm=10-12m)
-
铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为_____;其最外层电子的电子云形状为_____。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐
① 电子式为___。
电子式为___。
②N、O两元素的第一电离能由大到小的顺序为___(用元素符号表示)。
③ 中S原子的杂化方式为___,VSEPR模型名称为___。
中S原子的杂化方式为___,VSEPR模型名称为___。
(3)K3[Fe(CN)6]晶体中中心原子的配位数为__,晶体的配位体为__(用化学符号表示)。
-
Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Ni原子价电子中成对电子数与未成对电子数之比为_________。
(2)MgO与CaO这两个物质,其中熔点较高的是______,原因是___________________________________________。
(3)第二周期中,第一电离能介于B元素和N元素之间的元素有_________种。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合, 其结构如图所示。
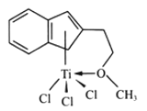
①组成M的元素中,电负性最大的是__________ (填名称)。
②M中碳原子的杂化方式为__________。
③M中不含__________ (填代号)。
a、π键 b、σ键 c、离子键 d、配位键
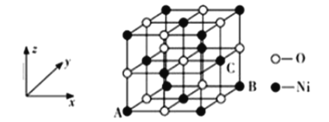
(5)NiO的晶体结构如图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为________________。
-
铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为_________________,其最外层电子的电子云形状为___________。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为_____________(用元素符号表示)。
②N、O两元素的的第一电离能由大到小的顺序为___________(用元素符号表示)。
③SO42-中S原子的杂化方式为___________,VSEPR模型名称为___________________。
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为_____,σ键和π键的数目之比为______________。其空间构型为__________。
(4)K3[Fe(CN)6]晶体中配离子的配位体为_____(用化学符号表示)
-
Co、Ni的化合物在生产生活中有着广泛的应用。
(1) 元素在周期表中的位置是4周期,_________族。基态Co原子的电子排布式为____________。
元素在周期表中的位置是4周期,_________族。基态Co原子的电子排布式为____________。
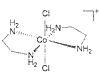
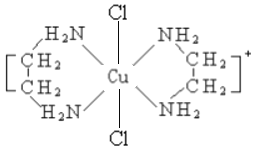
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下图所示,中心离子的配位数为________,配合物晶体中可能存在的作用力有___________。
A、离子键 B、极性共价键 C、非极性共价键 D、配位键 E、氢键
(3)NiO晶体结构如图1所示,其中离子坐标参数A为(0,0,0),B为( ),则C离子(面心处)坐标参数为_______________。
),则C离子(面心处)坐标参数为_______________。
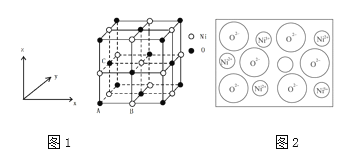
(4)天然氧化镍晶体中总是存在晶体缺陷,如图2所示。NiXO晶体中x值为 ,若晶体中的Ni分别为
,若晶体中的Ni分别为 、
、 ,此晶体中
,此晶体中 与
与 的最简整数比为______。
的最简整数比为______。
-
Co、Ni的化合物在生产生活中有着广泛的应用。
(1)Co元素在周期表中的位置是4周期________族。基态Co原子的简化电子排布式为_________。
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下左图所示,中心离子的配位数为_______,配合物晶体中可能存在的作用力有___________。
A 离子键 B 极性共价键 C 非极性共价键 D 配位键 E 氢键
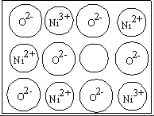
(3)天然氧化镍晶体中总是存在晶体缺陷,如图所示。NiXO晶体中x值为 ,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
,若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为______。
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列, Ni2+填充其中(如图),己知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为_____g(用a、NA表示)。

-
磷单质及其化合物在工业生产巾有着广泛的应用。向磷可用于制备高纯度的磷酸(磷酸结构简式为 ),三聚磷酸钠是常用的水处理剂,次磷酸钠(Nail2P@)可用于化学镀镍等等。完成下列填空:
),三聚磷酸钠是常用的水处理剂,次磷酸钠(Nail2P@)可用于化学镀镍等等。完成下列填空:
(1)磷元素原子核外最外层电子排布式为 。NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为 (填元素符号)。
(2)氧原子核外有 种不同能量的电子。
(3)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图。
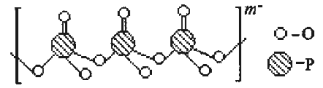
①磷原子的杂化类型为 ;②这种多聚磷酸钠的化学式为
(4) 次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性
①NaH2PO2为 (填“正盐”或“酸式盐”),其溶液显 (填“弱酸性”“中性”或“弱碱性”)
②次磷酸钠(NaH2PO2)可用于化学镀镍.化学镀镍的溶液中含有Ni2+和H2PO2-,在一定条件下能发生如下反应生成Ni和H2PO3-,写出上述反应离子方程式
-
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)Fe基态原子核外电子排布式为 。
(2)H、N、O的电负性从小到大的顺序是 。
(3)与NO2+互为等电子体的一种分子为 (填化学式)。氨基(-NH2)中氮原子的杂化类型为 。
(4)1mol苯分子中含有σ键的数目为 。
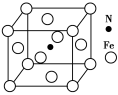
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为 。
-
铁及铁的化合物在生活、生产中具有广泛应用,如亚铁氰化钾即K4[Fe(CN)6]是食盐中常用的抗结剂、铁基(氟掺杂镨氧铁砷化合物)是高温超导材料、“愚人金”是制备硫酸的主要矿物原料。请按要求回答下列问题。
(1)K4[Fe(CN)6]配合物中存在的作用力类型有__________________________(从“金属键”、“离子键”、“共价键”、“配位键”、“氢键”、“范德华力”中选填);其中CN-中各原子最外层均满足8电子稳定结构,其电子式为_____________,其中C原子的杂化形式是_________。
(2)铁基化合物中氟、氧、砷三种元素中电负性值由大到小的顺序是_____________(填元素符号)。其中氢化物(RH3)的某种性能(M)随R的核电荷数的变化趋势如图所示,则纵轴M可能表示为_____________________(从“沸点”、“稳定性”、“分子间作用力”、“R—H键能”中选填)。

(3)FeCl3晶体熔点为306℃,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:____________________________________________。
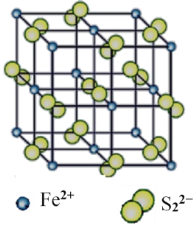
(4)“愚人金”是铁硫化合物,其晶体的晶胞如图所示。该晶体的化学式______________。
-
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)Fe基态原子核外电子排布式为________________________。
(2)H、N、O的电负性从小到大的顺序是_________________。
(3)与NO 互为等电子体的一种分子为__________(填化学式)。氨基(-NH2)中氮原子的杂化类型为_____________。
互为等电子体的一种分子为__________(填化学式)。氨基(-NH2)中氮原子的杂化类型为_____________。
(4)1mol苯胺分子中含有σ键的数目为_____________________。
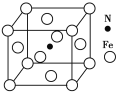
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为______________。
 ]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。
]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有_________个未成对电子。











