-
测定硫铁矿( 主要成分为FeS2)中硫和铁含量的实验步骤如下:
(硫含量的测定)
①准确称取0.5g硫铁矿粉于坩埚中,加入4.5gNa2O2,用玻璃棒充分搅拌,上面再盖一层Na2CO3,在700℃下焙烧15min。
②将坩埚及其盖放入100 mL沸水中,浸泡10 min并洗净坩埚。将所得溶液转移至烧杯中。
③向上述烧杯中先加入过量硝酸,再加入足量Pb(NO3)2溶液。过滤,洗涤、干燥,称得固体为2.02g。
(铁含量的测定)
④准确称取0.5g硫铁矿粉,加入盐酸和硝酸使其溶解。趁热加入稍过量的SnCl2溶液(Sn2++2Fe3+==2Fe2++Sn4+),再用HgCl2 氧化除去多余的SnCl2。
⑤以二苯胺磷酸钠为指示剂,用0.05mol/L的K2Cr2O7溶液滴定生成的Fe2+(K2Cr2O7被还原为Cr3+),直至终点,消耗11.20mL K2Cr2O7溶液。回答下列问题。
(1)步骤①适宜材质的坩埚是_____(填字母)。
a.铁坩埚 b.铝坩埚 c.陶瓷坩埚
(2)步骤①中上面盖一层Na2CO3的主要目的是_________________,焙烧时,FeS2和Na2O2反应生成硫酸盐和氧化钠的化学方程式为______________________________________。
(3)步骤③中得到的固体的化学式为__________________。
(4)步骤④若不除去过量的SnCl2,则会造成铁的含量测量值___(填“偏大”“偏小”或“不变”)。
(5)步骤⑤滴定时,K2Cr2O7溶液应盛放在_______(填“酸”或“碱”)式滴定管中。
高二化学综合题困难题查看答案及解析
-
在高温时硫铁矿(主要成分FeS2)和氧气反应生成三氧化二铁和二氧化硫(假设硫铁矿中的杂质不参与反应).某化学研究学习小组对硫铁矿样品进行如下实验探究:
【实验一】测定硫元素的含量
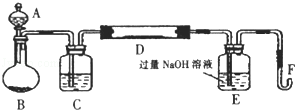
Ⅰ.实验装置如下图所示(夹持和加热装置已省略).A中的试剂是双氧水,将m1g该硫铁矿样品放人硬质玻璃管D中.从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管D中的硫铁矿样品至反应完全.
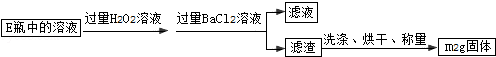
Ⅱ.反应结束后,将E瓶中的溶液进行如下处理:
【实验二】测定铁元素的含量
Ⅲ.测定铁元素含量的实验步骤如下:
①%2足量稀硫酸溶解已冷却的硬质玻璃管D中的固体,过滤,得到滤液A;
②%2②在滤液A中加入过量的还原剂使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤
液B;
③将滤液B稀释为250mL;
④取稀释液25.00mL,用浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL.
请根据以上实验,回答下列问题:
(1)Ⅰ中装置A仪器名称为 ;B仪器名称为 .
(2)Ⅰ中装置C中盛装的试剂是 ;E瓶的作用是 .
(3)Ⅱ中加入过量H2O2溶液发生反应的离子方程式为 .
(4)Ⅲ的步骤③中,将滤液B稀释为250mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;滴定终点的标志是 .
(5)假设在整个实验过程中硫元素和铁元素都没有损失,则该硫铁矿样品中硫元素的质量分数为 .(用含m1和m2的代数式表示)
高二化学实验题困难题查看答案及解析
-
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对某黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
Ⅰ、将
g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2
2Fe2O3+8SO2
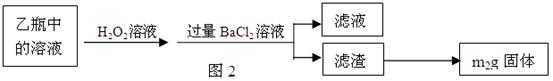
Ⅱ、反应结束后,将乙瓶中的溶液进行如图2所示处理。
[实验二]测定铁元素的含量。
Ⅲ、测定铁元素含量的实验步骤如图3所示:

问题讨论:
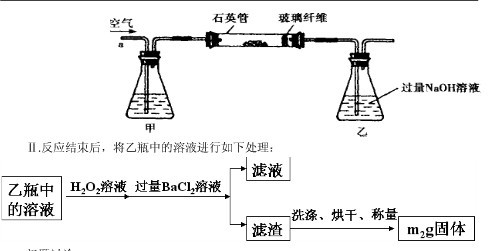
(1)Ⅰ中,甲瓶内所盛试剂是________溶液。乙瓶内发生反应的离子方程式有:
________、________。
(2)Ⅱ中的滤渣在称量前还应进行的操作是。
(3)Ⅱ中,所加H2O2溶液(氧化剂)需足量的理由是________。
(4)Ⅲ的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有________。
写出④中反应的离子方程式________。
(5)该黄铁矿中硫元素的质量分数为________。
高二化学实验题简单题查看答案及解析
-
(10分)黄铁矿(主要成分为FeS2)曾是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
I.将m1 g该黄铁矿样品放入如图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O22Fe2O3+8SO2
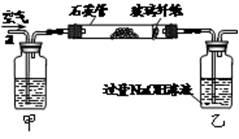
II.反应结束后,将乙瓶中的溶液进行如下图所示处理。

[实验二]测定铁元素的含量。
III.测定铁元素的含量的实验步骤如下图所示。

问题讨论:
(1)上述装置中,甲瓶内所盛试剂是________溶液。
(2)向乙瓶溶液中滴加H2O2溶液时,发生氧化还原反应的离子方程式为________。
II中除了可以用H2O2溶液作为氧化剂,还可以加入________(填序号)。
①氯水 ②浓H2SO4 ③HNO3 ④Fe2(SO4)3
(3)该黄铁矿中硫元素的质量分数为________。
(4)III的步骤②中,若选用铁粉作还原剂,你认为合理吗?并说明理由。(如合理,则此空不填)________(填“合理“或”不合理“)、________(如合理,则此空不填)。
(5)若要测定铁元素的含量,则步骤III中还需要测定的数据有________。
高二化学实验题中等难度题查看答案及解析
-
某同学进行硫酸铜晶体(
)结晶水含量的测定实验。完成下列填空:
(实验步骤):
(1)在__________(填仪器名称)准确称量瓷坩埚的质量。
(2)在瓷坩埚中加入一定量的硫酸铜晶体,并称重。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至_______(填仪器名称)中冷却到室温,并称重。
(4)重复上述实验进行恒重操作,其目的是_______________,直到两次称量结果不超过______克。
(5)下面是该学生实验的一次数据,请完成计算:
坩埚质量(克)
坩埚与晶体的质量(克)
恒重后坩埚与固体质量
13.721
24.692
20.631
______;(精确到0.01)实验相对误差是_________(保留小数后一位)。
(6)这次实验中产生误差的原因可能是_______
a. 硫酸铜晶体中含有不挥发性杂质 b. 在加热过程中发现有黑色物质生成
c. 加热时有晶体飞溅出来 d. 加热失水后露置在空气中冷却
高二化学实验题中等难度题查看答案及解析
-
某同学进行硫酸铜晶体结晶水含量的测定实验。完成下列填空:
【实验步骤】
(1)用_______(填仪器名称,下同)准确称量瓷坩埚的质量。
(2)在瓷坩埚中加入约2 g研细的硫酸铜晶体,并称量。
(3)把盛有硫酸铜晶体的瓷坩埚放在泥三角上慢慢加热,直到蓝色完全变白,然后把坩埚移至____________中冷却到室温,并称量。
(4)重复(3)的实验进行恒重操作,直至两次称量结果相差不超过0.001 g。
【数据记录与处理】
第一次实验
第二次实验
坩埚的质量(g)
29.563
30.064
坩埚+试样的质量(g)
31.676
32.051
恒重后,坩埚+硫酸铜的质量(g)
30.911
31.324
x的值
5.05
5.13
根据上表中的数据处理结果,计算本次实验的相对误差为______%(已知x的理论值为5)。
【分析与讨论】
(1)做一次实验,至少需要加热________次(填数字,下同);至少需要称量_________次。
(2)恒重操作的目的是__________________。
(3)重复两次实验求x平均值的目的是_____________________________。
(4)实验值比理论值偏大的原因可能是________(填编号)。
a.加热过程中有晶体溅出 b.被测样品中含有加热不挥发的杂质
c.实验前,晶体表面潮湿 d.晶体灼烧后直接放在空气中冷却
高二化学实验题中等难度题查看答案及解析
-
小龙同学在实验室选用碘量法测定某磁铁矿(主要成分是 Fe3O4,杂质SiO2、CuO)中铁元素质量分数,实验步骤如下:
①酸浸:取样m g,先将矿石粉碎,加入足量2mol/LH2SO4浸取,过滤后得到浸取液;
②除杂:先向浸取液中加入足量 H2S溶液,过滤后加入足量酸性 H2O2溶液氧化Fe2+(过量的H2S转化为S),再加入一定量MnO2固体除去过量的H2O2,一段时间后过滤得到Vml 滤液;
③定容:将滤液稀释至250mL,取出25.00mL于带塞子的锥形瓶中待用;
④转化:向25.00mL溶液中加入足量KI固体,塞上塞子于暗处静置30min;
⑤滴定:加入指示剂后,用cmol/LNa2S2O3标准溶液进行滴定至终点,消耗Na2S2O3标准溶液 V1mL;
⑥重复④⑤操作2次。 已知:2S2O32-+I2==S4O62-+2I-
1)①中将矿石粉碎的目的是____________________________________________,加入足量 H2SO4的目的是__________________________________。
2)写出②中加入足量 H2S 溶液发生反应的离子反应方程式:_____________________________。
3)③中用______________________________ _(填仪器名称)取出 25.00mL 溶液。
4)⑤中加入的指示剂是________,滴定终点的现象是:滴入最后一滴 Na2S2O3标准溶液 后,__________。⑥中重复进行实验的目的是______。
5)该磁铁矿中铁元素质量分数为______________(用含 m、c、V1的代数式表示,需要化简)。
6)若滴定过程中溶液 pH 过低则会导致测定结果______ (填“偏高”、“偏低”),写出 导致这种误差的离子反应方程式___________。
若②中过量的 H2O2溶液没除则会导致测定结果_____(填“偏高”、“偏低”) 若②中 MnO2固体没有过滤除去则会导致测定结果_________(填“偏高”、“偏低”)
高二化学综合题中等难度题查看答案及解析
-
某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其它成分不与盐酸反应,也不与氢氧化钠反应),实验步骤如下:
①配制
稀盐酸和
溶液各
②取一粒药片(
)研碎后加入
蒸馏水
③加入
稀盐酸
④用
溶液中和过量盐酸,用去体积为
。
请回答下列问题:
(1)测定过程中发生反应的离子方程式_________。
(2)配制上述
稀盐酸所用玻璃仪器有量筒、烧杯、________。
(3)如果选用酚酞作指示剂,滴定达到终点的现象为____。
(4)某同学四次测定的
数据如下:
测定次序
第一次
第二次
第三次
第四次
13.40
11.90
12.10
12.00
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数为_____。
(5)若在实验过程中存在下列操作,会使所测碳酸钙的质量分数偏高的是_________。
a 用没有润洗的碱式滴定管装
溶液进行滴定
b 用没有润洗的酸式滴定管量取
稀盐酸溶解样品
c 用
溶液滴定时,开始读数平视,终点俯视
d 装
溶液的滴定管,滴定前尖嘴有气泡,滴定结束后无气泡。
高二化学实验题中等难度题查看答案及解析
-
溶解氧(指溶解在水体中氧气分子)是衡量水质的一个重要指标。为测定某水样中溶解氧含量(ρ=
 )设计了如下实验方案。实验步骤如下:
)设计了如下实验方案。实验步骤如下:步骤1:水样的采集与固定
用水样瓶准确量取100mL的待测水样(不能留有气泡),并用针筒向水样下方快速注入2.0mLMnSO4溶液和3.0mL碱性KI溶液,盖好瓶盖,上下颠倒摇匀,此时生成Mn2+在碱性条件下被水中的氧气氧化为MnOOH棕色沉淀,静置至澄清。
步骤2:碘的游离
向水样瓶中加入3.0mL浓硫酸,使I-在酸性条件下被MnOOH氧化为I2,同时MnOOH被还原Mn2+,待沉淀完全溶解后,将它们全部转移到250mL锥形瓶中。
步骤3:碘的滴定
向锥形瓶中加入少量淀粉溶液,再滴加0.005mol·L-1的Na2S2O3标准溶液,恰好完全反应时,消耗Na2S2O3标准溶液的体积为16mL。(已知:I2+2S2O32-=2I-+S4O62-)
(1)MnOOH中Mn元素的化合价是___。
(2)写出步骤2中所发生反应的离子方程式___。
(3)若待测水样中留有气泡,则测定结果将___。(填“偏大”、“偏小”或“无影响”)
(4)计算该水样中溶解氧的含量ρ(以mg·L-1表示),并写出计算过程:___。
高二化学实验题中等难度题查看答案及解析
-
为测定硫酸亚铁铵晶体【(NH4)2Fe (SO4)2 · xH2O】中铁的含量,某实验小组做了如下实验:
步骤一:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250ml溶液。
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,用0.010mol/L KMnO4溶液滴定至Fe2+恰好全部氧化成Fe3+,同时,MnO4-被还原成Mn2+。
再重复步骤二两次。
请回答下列问题:
(1)配制硫酸亚铁铵溶液的操作步骤依次是:称量、 、转移、洗涤并转移、 、摇匀。
(2)用 (“酸式”或“碱式”)滴定管盛放KMnO4溶液。
(3)当滴入最后一滴KMnO4溶液,出现 ,即到达滴定终点。反应的离子方程式:
(4)滴定结果如下表所示:
滴定次数
待测溶液的体积/mL
标准溶液的体积
滴定前刻度/mL
滴定后刻度/mL
1
25.00
1.05
21.04
2
25.00
1.50
24.50
3
25.00
0.20
20.21
实验测得该晶体中铁的质量分数为 。(保留两位小数)
高二化学实验题中等难度题查看答案及解析