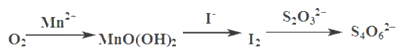-
溶解氧(指溶解在水体中氧气分子)是衡量水质的一个重要指标。为测定某水样中溶解氧含量(ρ= )设计了如下实验方案。实验步骤如下:
)设计了如下实验方案。实验步骤如下:
步骤1:水样的采集与固定
用水样瓶准确量取100mL的待测水样(不能留有气泡),并用针筒向水样下方快速注入2.0mLMnSO4溶液和3.0mL碱性KI溶液,盖好瓶盖,上下颠倒摇匀,此时生成Mn2+在碱性条件下被水中的氧气氧化为MnOOH棕色沉淀,静置至澄清。
步骤2:碘的游离
向水样瓶中加入3.0mL浓硫酸,使I-在酸性条件下被MnOOH氧化为I2,同时MnOOH被还原Mn2+,待沉淀完全溶解后,将它们全部转移到250mL锥形瓶中。
步骤3:碘的滴定
向锥形瓶中加入少量淀粉溶液,再滴加0.005mol·L-1的Na2S2O3标准溶液,恰好完全反应时,消耗Na2S2O3标准溶液的体积为16mL。(已知:I2+2S2O32-=2I-+S4O62-)
(1)MnOOH中Mn元素的化合价是___。
(2)写出步骤2中所发生反应的离子方程式___。
(3)若待测水样中留有气泡,则测定结果将___。(填“偏大”、“偏小”或“无影响”)
(4)计算该水样中溶解氧的含量ρ(以mg·L-1表示),并写出计算过程:___。
-
自然界水体中的碳元素主要以碳酸盐、碳酸氢盐和有机物形式存在。水体中有机物含量是水质的重要指标,常用总有机碳衡量(总有机碳= )。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
)。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
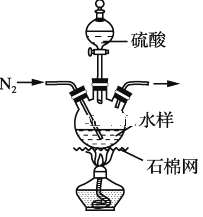
步骤1:量取50 mL水样,加入足量硫酸,加热,通N2,并维持一段时间(装置如图,夹持类仪器省略)。
步骤2:再向水样中加入过量的K2Cr2O7溶液(可将有机物中的碳元素氧化成CO2),加热,充分反应,生成的CO2完全被100mL 0.206 mol·L-1的Ba(OH)2溶液吸收。
步骤3:将吸收CO2后的浊液过滤并洗涤沉淀,再将洗涤得到的滤液与原滤液合并,加水配制成500mL溶液。量取25.00mL溶液于锥形瓶中,加入几滴酚酞试剂,并滴加0.05mol·L-1的H2C2O4溶液,发生反应:Ba(OH)2+H2C2O4===BaC2O4↓+2H2O 恰好完全反应时,共消耗H2C2O4溶液20.00 mL。
(1)步骤1的目的是____。
(2)用H2C2O4溶液滴定至终点时,溶液颜色变化是____。
(3)计算水样的总有机碳(以mg·L-1表示),并写出计算过程。____
-
水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。水中溶解氧的测定步骤如下:
(1)向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;
(2)加入适量稀H2SO4,搅拌,等MnO(OH)2与I-完全反应生成Mn2+和I2后;
(3)用Na2S2O3标准溶液滴定至终点。
测定过程中物质的转化关系如下:
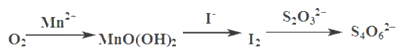
已知:MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O 2S2O32- +I2= S4O62-+2I-
①加入稀硫酸后搅拌的作用是__________;Na2S2O3标准溶液应装在______________滴定管中(填酸式或碱式)。
②滴定过程中以_____________为指示剂;达到滴定终点的标志为____________________。
③写出O2将Mn2+氧化成MnO(OH)2的离子方程式____________________;
④若加入的稀H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生误差的一个原因(用离子方程式表示)__________________。
⑤下列操作使测得水样中溶氧量(DO)比实际值偏高的是__________________。
A.第(1)步操作静置时没有密封 B.装Na2S2O3标准溶液的滴定管没有润洗
C.滴定前锥形瓶洗净后没有干燥 D.滴定前读数正确,滴定后俯视读数
⑥取加过一定量CaO2·8H2O的池塘水样l00.00mL,按上述方法测定水中溶解氧量,消耗0.01000
mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为____________mg·L-1。
-
水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I−还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32-+I2=2I−+ S4O62-)。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____________。
(2) “氧的固定”中发生反应的化学方程式为_______________。
(3)取100.00 mL水样经固氧、酸化后,用a mol·L−1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为________________;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为_________mg·L−1。滴定结束后如果俯视滴定管读取数据,导致测定结果偏___________。(填“高”或“低”)
(4)Na2S2O3溶液不稳定,需使用前配制和标定。预估实验需要使用75mL的Na2S2O3溶液,则配制该溶液所必需的仪器有天平、烧杯、玻璃棒和___________________
-
一次性饭盒中石蜡(高级烷烃)和 在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下: 剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是( )
在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下: 剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是( )
A.氢氧化钠溶液 B.盐酸 C.稀硫酸 D.正己烷
-
亚硫酸钠是工业中重要的原料。某亚硫酸钠样品因在空气中放置而被部分氧化为硫酸钠。某化学实验小组设计实验测定样品中亚硫酸钠的含量。
(1)甲方案
①准确称取5.0g样品放入烧杯中,加足量稀盐酸,充分搅拌溶解。
②边搅拌边滴加1mol·L-1BaCl2溶液至过量
③过滤,洗涤,干燥,称得固体质量为m1g
(2)乙方案
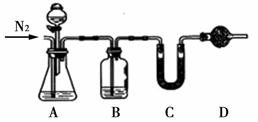
准确称取5.0g样品置于右图锥形瓶中,并通一段时间N2。打开分液漏斗活塞,逐滴加入70%硫酸至不再产生气体。再通入一段时间N2,最终称得C装置反应前后增重m2g
回答下列问题
(1)甲方案步骤①中发生了离子反应,其离子方程式为________。
(2)如何判断步骤②中滴加BaCl2溶液已过量___________。
(3)甲方案测得的样品中亚硫酸钠的含量为___________(用含带m1的代数式 表示)
表示)
(4)乙方案中第一次通入氮气的目的是___________。
(5)乙方案中B装置的作用是______,若C、D置中药品相同,则是______(填药品名称),若无D装置,测定结果___(填“偏大”、“偏小”、“无影响”)
(6)有同学设计实验通过测量产生的SO2气体体积来测定样品中的亚硫酸钠含量,下列实验装置最准确、最恰当的是_________。
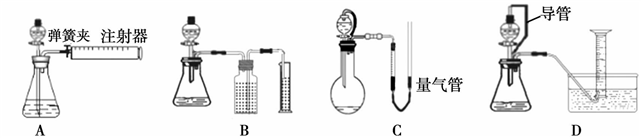
-
(11分)实验室用下列方法测定某水样中O2的含量。
(1)用如右图所示装置,使水中溶解的O2,在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为________。

实验步骤:
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是。
②用注射器抽取20.00 mL 某水样从A 处注入锥形瓶。
③再分别从A 处注入含m mol NaOH的溶液及过量的MnSO4 溶液。
④关闭止水夹a、b,将锥形瓶中溶液充分振荡;
(2)用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为:
MnO(OH)2+2I-+4H+==Mn2++I2+3H2O。
实验步骤:
⑤打开止水夹a、b,分别从A 处注入足量NaI溶液及含n mol H2SO4硫酸溶液。
⑥重复④的操作。
(3)用Na2S2O3标准溶液滴定步骤(2)中生成的I2,反应方程式为: I2+2Na2S2O3==2NaI+Na2S4O6。
实验步骤:
⑦取下锥形瓶,向其中加入2~3滴________作指示剂。
⑧用0.005 mol · L-1Na2S2O3 滴定至终点。
(4)计算。滴定过程中,滴定前后滴定管中的液面读数如右图所示。

⑨经计算,此水样中氧(O2)的含量为(单位:mg·L-1)________。
⑩本实验中所加NaOH溶液和H2SO4溶液中m和n应有一定量的关系,即应加适量的H2SO4使溶液呈________(填“酸性”、“碱性”或“接近中性”),其原因是________。
-
自来水中氯离子的测定对人体健康有重要意义,实验室常用莫尔法测定水体中氯离子含量。实验过程如下:向水样中加入K2CrO4 (黄色) 溶液作指示剂,用AgNO3溶液滴定至终点。已知:Ag2CrO4为不溶于水的砖红色沉淀;常温下Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)= 1.8×10-12。
回答下列问题:
(1)滴定时,应使用____________(填“酸式”或“碱式”) 滴定管,原因是_______________________。
(2)水样应调至中性或弱碱性,强酸性时加入K2CrO4溶液发生反应的离子方程式是___________________________________________。
(3)滴定达到终点的标志是___________________________________________。
(4)实验过程中测得数据如下表:
| 编号 | 1 | 2 | 3 |
| V(水样)/mL | 10.00 | 10.00 | 10.00 |
| c(AgNO3)/ mol·L-1 | 0.0010 |
| V(AgNO3)/mL | 3.75 | 4.01 | 3.99 |
计算水样中氯离子的含量为_______________mg/L(保留2位小数)
(5)滴定结束后:
①当溶液中的残余c(Cl-)=1.8×10-5mol/L,则此时溶液中c(CrO42-)=____________。
②已知2AgCl+ CrO42- 2Cl-+Ag2CrO4,计算出该反应的平衡常数为____________。
2Cl-+Ag2CrO4,计算出该反应的平衡常数为____________。
(6)下列情况会造成实验测定结果偏低的是____________。(填标号)
A.锥形瓶洗涤后未干燥
B.滴定前,未使用标准液润洗滴定管
C.酸式滴定管滴定前仰视读数,滴定后俯视读数
D.酸式滴定管滴定前尖嘴部分充满溶液,滴定结束时滴定管尖嘴有气泡
-
某兴趣小组设计了如下实验测定海带中碘元素的含量,依次经过以下四个步骤,下列图示装置和原理能达到实验目的的是
A.灼烧海带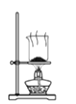
B.将海带灰溶解后分离出不溶性杂质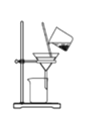
C.制备Cl2,并将I-氧化为I2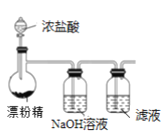
D.以淀粉为指示剂,用Na2SO3标准溶液滴定
-
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
(I)甲同学的方案是:将mg样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称得固体ng。
(1)混合物中碳酸钠的质量分数为(用m、n表示) ,甲同学洗涤沉淀的具体操作是 。
(2)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是:① ;
② 。
(Ⅱ)乙同学的方案如图所示:

(1)根据乙同学的实验装置图分析,在每次实验中,完成测定过程至少要进行 次称量操作。按照该同学的方案进行测定,结果与实际情况存在较大的误差,你认为主要原因可能是(任写两个):
① ;
② 。
(2)乙同学的方案的装置中存在一定的缺陷,请你提出改进的方法(简单叙述做法,不必画图): 。
 )设计了如下实验方案。实验步骤如下:
)设计了如下实验方案。实验步骤如下: )。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。
)。某学生兴趣小组用如下实验方法测定采集水样的总有机碳。