-
侯德榜为纯碱和氮肥工业的发展作出了杰出的贡献。下面是实验室中模拟“侯氏制碱法”制取NaHCO3的实验装置。
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在D中溶解时,再通入另一装置中产生的气体,片刻后,D中出现固体.继续向D中通入两种气体,直到不再有固体产生.
第三步:过滤D中所得的混合物,得到NaHCO3固体.
第四步:向滤液中加入适量的NaCl粉末,有NH4 Cl晶体析出.
(1)下图所示装置的连接顺序是:a接________;b接_________;________接_________。

(2)B中常选用的固体反应物为__________,C中应选用的液体为_______________,请叙述A中产生气体的原理_____________________。
(3)第二步中必须先让_______装置先发生反应。
(4)D中用球形干燥管而不用直导管,其作用是___________。
(5)第四步中分离出NH4 Cl晶体的操作名称是___________;其所得的NH4 Cl晶体中常含有少量的NaCl和NaHCO3 约占5%-8%),请设计一个简单的实验证明所得固体的成分大部分是NH4Cl.简要写出操作和现象:_____________。
(6)要检验第四步分离出NH4 Cl晶体后的溶液中含有NH4+,请叙述检验方法:______________。
-
侯德榜先生是我国举世闻名的化工专家,他对制碱技术作出了重大贡献,他所发明的联合制碱法称作“侯氏制碱法”.右图是在实验室中模拟“侯氏制碱法”中制取碳酸氢钠一步的实验装置,实验步骤为:
①连接好装置,检验气密性,在仪器内装入药品.
②先从D的分液漏斗中连续滴下浓氨水,直到产生的气体不能再在C中的饱和NaCl溶液中溶解时.再通入A中产生的气体.片刻后,烧杯中析出白色固体(碳酸氢钠).继续向C中通入两种气体,直到不再有固体产生为止.
③过滤烧杯内所得的混合物,得到碳酸氢钠固体.
④向滤液中加入适量的氯化钠固体,发生反应:
NaCl(s)+NH4Cl(aq)=NaCl(aq)+NH4Cl(s),搅拌后过滤,滤出物可用作化肥.
⑤滤液再注入烧杯C中,重复使用,进行下一次制备…
试回答下列问题:
(1)检验装置A气密性的方法是______.
(2)烧杯C中发生反应的化学方程式为______.
(3)A中常选用的固体为______;B中应选用的液体为______.
(4)步骤②中必须先让D中发生反应,产生气体后,再让A中发生反应产生气体,原因是______.
(5)步骤④是在较高温度(如60℃)下还是在较低温度下(如0℃~10℃)下进行合适?______(填“较高”或“较低”)
(6)步骤④中所得的氯化铵晶体中常含有少量的氯化钠和碳酸氢钠(约占5%~8%),请设计简单的实验证明所得固体的成分大部分是氯化铵.简要写出操作方法、现象和结论.______.

-
(8分)下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤。
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4C1晶体析出。
(1)下图所示装置的连接顺序是:a接____;____接___;b接_____。

(2)A中常选用的固体反应物为_____;D中应选用的液体为______
(3)第二步中必须先让_______装置先发生反应
(4)C中用球形干燥管而不用直导管,其作用是________
(5)第四步中分离出NH4Cl晶体的操作是_______;其所得的NH4C1晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,证明所得固体的成分大部分是NH4C1。简要写出操作和现象:_______。
-
1942年,我国化工专家侯德榜以NaCl、NH3、CO2等为原料制得纯碱,他的“侯氏制碱法”为世界制碱工业做出了突出贡献。
回答下列问题:
某探究活动小组欲在实验室中模拟制取纯碱,设计了Ⅰ、Ⅱ两种方案,并选择其一进行实验。
方案Ⅰ:(1)将足量CO2通入饱和NaCl溶液中;(2)再在所得溶液中通入足量NH3;(3)过滤;……。
方案Ⅱ:(1)将足量NH3通入饱和NaCl溶液中;(2)再在所得溶液中通入足量CO2;(3)过滤;……。
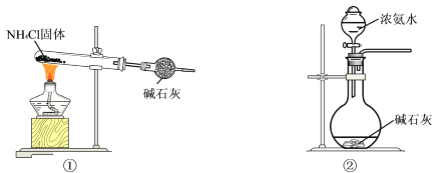
(1)部分实验装置如图所示。制取氨气的装置应选用________(选填编号)。
(2)写出实验中获得碳酸氢钠的离子方程式____________________________________________
(3)灼烧碳酸氢钠需要_________(选填编号)。
a.蒸发皿 b.坩埚 c.烧杯 d.烧瓶 e.酒精灯
(4)选择的实验方案是________(选填“Ⅰ”或“Ⅱ”),说明选择的理由____________________
(5)甲同学取少量产品完全溶于水,滴加稀硝酸2-3滴,再滴加硝酸银溶液,观察到有白色沉淀生成,得出纯碱含杂质Cl-的结论。乙同学认为甲的结论不一定正确,你认为乙同学的理由是_________________。
(6)按下列流程处理母液(提取完碳酸氢钠后的滤液)可得到NH4Cl。

通入NH3的作用是_______(选填编号)。操作a是_________________,操作b是___。
a.增大NH4+浓度,使NaHCO3更多地析出
b.增大NH4+浓度,使NH4Cl更多地析出
c.使NaHCO3转化为溶解度更大的Na2CO3,提高析出的NH4Cl纯度
-
某实验小组模拟工业侯氏制碱法原理制备少量NaHCO3固体,将实验流程分为四个步骤。下列图示装置和操作能达到实验目的的是( )
A.制取氨气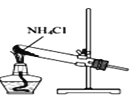
B.制取NaHCO3 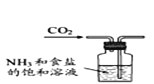
C.分离NaHCO3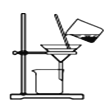
D.干燥NaHCO3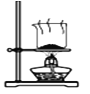
-
“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如图:下列叙述正确的是( )
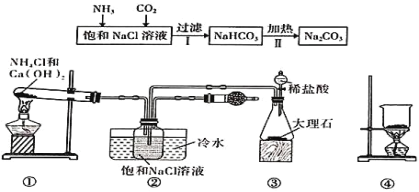
A.实验时先打开装置③中分液漏斗的旋塞,过一段时间后再点燃装置①的酒精灯
B.装置②的干燥管中可盛放碱石灰,作用是吸收多余的NH3
C.向步骤 I 所得滤液中通入氨气,加入细小的食盐颗粒并降温可析出NH4Cl
D.用装置④可实现步骤Ⅱ的转化,所得CO2可循环使用
-
“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如图:下列叙述正确的是( )

A.实验时先打开装置③中分液漏斗的旋塞,过一段时间后再点燃装置①的酒精灯
B.装置②的干燥管中可盛放碱石灰,作用是吸收多余的NH3
C.向步骤 I 所得滤液中通入氨气,加入细小的食盐颗粒并降温可析出NH4Cl
D.用装置④可实现步骤Ⅱ的转化,所得CO2可循环使用
-
“侯氏制碱法”是我国化工专家候德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如下:
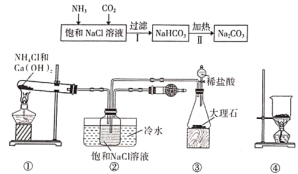
下列叙述错误的是
A. 实验时先点燃装置①的酒精灯,过一段时间后再打开装置③中分液漏斗的旋塞
B. 装置②的干燥管中可盛放蘸稀硫酸的脱脂棉,作用是吸收多余的NH3
C. 向步骤Ⅰ所得滤液中通入氨气,加入细小的食盐颗粒并降温,可析出NH4Cl
D. 用装置④加热碳酸氢钠可实现步骤Ⅱ的转化,所得CO2可循环使用
-
某研究性学习小组在实验室模拟工业“侯氏制碱法”原理制取NaHCO3。下图是该学习小组进行模拟实验时所用到的主要装置。

请回答下列问题:
(1)B装置中仪器a的名称是______________。
(2)C装置中发生的现象是_____________,反应的化学方程式是___________________。
(3)检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,向漏斗里注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若__________________________________________.说明装置不漏气。
(4)D是连接在装置A与装置C之间的气体净化装置,装置D的作用是____________________________。
(5)实验时向饱和NaCl溶液中先通入NH3,再通入CO2的原因是__________________________________。
(6)设计实验方案,检验NaHCO3产品中是否含有氯化钠_________________________________________。
-
(16分)某实验小组模拟“侯氏制碱法”制纯碱,并进行以下探究:
(1)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:
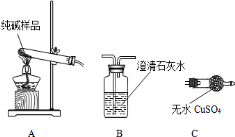
| 选择的装置 (填编号) | 实验现象 | 实验结论 |
| | 样品含 NaHCO3 |
(2)测定该纯碱样品的纯度:称取m1g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混和物过滤、 (填操作)、干燥、称量为m2g。该纯碱样品的纯度为 。
(3)该小组同学在0.1 mol/L NaHCO3溶液中滴加酚酞溶液1滴,溶液没有什么变化,但加热后显淡红色,加热较长时间后冷却,红色不褪去。为探究原因,进行了下列实验:
实验1: 加热0.1 mol/L NaHCO3溶液,测得溶液pH变化如下表
| 温度(℃) | 10 | 20 | 30 | 50 | 70 | 80 | 100 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 | 9.6 | 10.1 |
但当温度恢复到10 ℃,测得溶液pH=9.8。
实验2:加热0.1 mol/L NaHCO3溶液,将产生的气体通入澄清石灰水,澄清石灰水变浑浊。
①用离子方程式表示0.1 mol/L NaHCO3溶液中存在的平衡(除水电离平衡外) 、
________________。这两个平衡以__________为主。
②结合实验1、2分析,加热0.1 mol/L NaHCO3溶液,pH增大的原因可能是_____________(答一条)。













