-
已知:8NH3(g) +6NO2(g)
7N2(g) +12H2O(1) △H<0。相同条件下,向2 L恒容密闭容器内充入一定量的NH3和NO2,分别选用不同的催化剂进行已知反应(不考虑NO2和N2O4之间的相互转化),反应生成N2的物质的量随时间的变化如图所示。下列说法错误的是( )
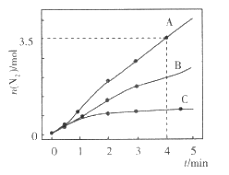
A.在催化剂A的作用下,0 ~4 min 内v(NH3)=1.0mol
L-1
min-1
B.若在恒容绝热的密闭容器中反应,当容器内温度不变时,说明反应已经达到平衡
C.不同催化剂作用下,该反应的活化能由大到小的顺序是Ea(C)> Ea(B)> Ea(A)
D.升高温度可使容器内气体颜色变浅
高三化学多选题中等难度题查看答案及解析
-
氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl2氧化法处理这种废水,涉及两个反应:反应i,CN- +OH-+Cl2
OCN- +Cl-+H2O(未配平);
反应ii,OCN- + OH-+ Cl2
X + Y + Cl-+ H2O(未配平)。
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1: 1
B.X、Y是CO2、N2,且均为反应ii的氧化产物
C.该废水处理工艺过程中须采取措施,防止Cl2逸出到空气中
D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl2 4.48×103L
高三化学多选题中等难度题查看答案及解析
-
已知:CH4(g)+2H2S(g)
CS2(g)+4H2(g)。向恒容密闭容器中充入0.1molCH4和0.2molH2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示,下列说法正确的是( )

A.该反应的ΔH<0
B.X点CH4的转化率为20%
C.X点与Y点容器内压强比为51∶55
D.维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1mol时v(正)<v(逆)
高三化学多选题中等难度题查看答案及解析
-
室温下,Ka(HCOOH)=1.77×10-4,Ka(CH3COOH)=1.75×10-5。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
A.向0.1mol·L-1的CH3COONa溶液中通入HCl气体至pH=7:c(Na+)>c(Cl-)=c(CH3COOH)
B.相同浓度的CH3COONa和HCOONa的混合溶液中:c(Na+)>c(HCOO-)>c(CH3COO-)>c(OH-)
C.c(NH
)相等的HCOONH4溶液、CH3COONH4溶液:c(HCOONH4)>c(CH3COONH4)
D.0.1mol·L-1的CH3COOH溶液和0.05mol·L-1的NaOH溶液等体积混合:c(Na+)+c(OH-)>c(CH3COOH)+c(H+)
高三化学多选题困难题查看答案及解析
-
催化剂存在下,在1 L的恒容密闭容器中充入0.1 molCO和0.3mol H2发生反应CO(g)+3H2(g)
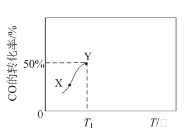
CH4(g)+H2O(g)。反应相同时间,CO的转化率与反应温度的关系如图所示。下列说法一定正确的是
A.升高温度,CO(g)+3H2(g)
CH4(g)+H2O(g)的化学平衡常数增大
B.图中X点所示条件下,延长反应时间能提高CO的转化率
C.图中Y点所示条件下,改用性能更好的催化剂能提高CO的转化率
D.T1 ℃,CO(g)+3H2(g)
CH4(g)+H2O(g)的化学平衡常数K>1
高三化学多选题中等难度题查看答案及解析
-
草酸(H2C2O4)是一种二元弱酸。室温时,下列指定溶液中微粒物质的量浓度关系正确的是
A.0.1 mol·L−1 NaHC2O4溶液:c(Na+)>c(C2O
)>c(HC2O
)
B.0.1 mol·L-1 Na2C2O4溶液:c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O
)
C.0.1 mol·L−1 H2C2O4溶液:0.2 mol·L−1 + c(OH-) = c(H+) + 2c(H2C2O4) + c(HC2O
)
D.向Na2C2O4溶液中滴加H2C2O4溶液至中性:c(Na+) = 2c(C2O
)
高三化学多选题困难题查看答案及解析
-
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项
实验操作和现象
结论
A
室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊
碳酸的酸性比苯酚的强
B
加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去
有乙烯生成
C
向5 mL 0.1 mol·L−1 KI溶液中加入1 mL 0.1 mol·L−1 FeCl3溶液,充分反应后,萃取分液,向水层中滴加KSCN溶液,溶液呈血红色
I-与Fe3+的反应有一定限度
D
向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝
Kw<Ka1(H2CO3)×Ka2(H2CO3)
A.A B.B C.C D.D
高三化学多选题困难题查看答案及解析
-
某温度下,在起始压强为80kPa的刚性容器中,发生NO的氧化反应:2NO(g)+O2(g)⇌2NO2(g) △H,该反应的反应历程分两步进行,其速率方程和反应过程中能量变化如下:
①2NO(g)⇌N2O2(g) v1正=k1正c2(NO) v1逆=k1逆c(N2O2)
②N2O2(g)+O2(g)⇌2NO2(g) v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2)
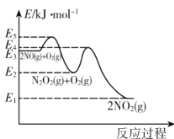
下列说法正确的是
A.NO氧化反应速率快慢的决定步骤的活化能是E5—E3
B.一定温度下,2NO(g)+O2(g)⇌2NO2 (g)平衡常数表达式K=
C.升高温度,NO氧化反应的化学平衡向逆反应方向移动
D.该温度下,将等物质的量的NO和O2混合反应(忽略2NO2⇌N2O4),NO的平衡转化率为40%时,该反应的平衡常数Kp=
kPa-1
高三化学多选题困难题查看答案及解析
-
BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,反应原理如下图所示。下列说法错误的是
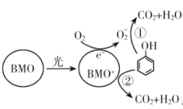
A.苯酚被氧化的总反应:C6H5OH+7O2
6CO2+3H2O
B.反应过程中BMO表现较强氧化性
C.在酸性条件下,反应①的离子方程式是3C6H5OH+28
+28H+=l8CO2↑+23H2O
D.过程①和②中被降解的苯酚的物质的量之比为1:3
高三化学多选题中等难度题查看答案及解析
-
Cl2O能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备Cl2O原理为HgO(红色粉末)+2Cl2=HgCl2(白色粉末)+Cl2O,某化学小组用下图装置制备Cl2O(夹持装置略去)
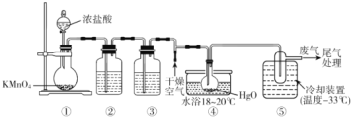
已知:①Cl2O的熔点为-116°C、沸点为3.8°C,易溶于水;②高浓度的Cl2O易爆炸,Cl2O与有机物接触或加热时会发生剧烈反应。
下列说法错误的是
A.装置③中盛装的试剂是饱和食盐水,④中现象是红色粉末逐渐变为白色
B.装置④中橡胶塞用锡箔包裹,防止Cl2O与橡胶塞反应
C.从装置⑤中逸出气体的主要成分是Cl2O
D.通入干燥空气的目的是将生成的Cl2O稀释,防止发生爆炸
高三化学多选题中等难度题查看答案及解析