-
物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)0.2 g H2含有________个H原子。
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为________。
(3)100 mL硫酸铝溶液中n(Al3+)=0.20 mol(不考虑水解因素),则其中c(SO
)=________。
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为________,该金属元素的相对原子质量为________。
(5)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为________g。
高三化学简答题简单题查看答案及解析
-
碱式次氯酸镁具有强氧化性,是一种无机抗菌剂,难溶于水,不吸湿。以次氯酸钠和氯化镁制备碱式次氯酸镁固体的实验方案和实验装置如图1所示。
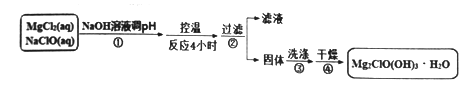
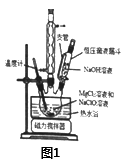
请回答:
(1)图1中支管的作用是_______________,步骤①的关键是控制温度,其措施有_______________(写两种)。
(2)步骤①发生的化学反应方程式_________________________。
(3)步骤②、③采用图2装置分离析出的Mg2ClO(OH)3·H2O固体过程中,下列操作不正确的是_____。
A.该装置中只有2处错误
B.选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
C.直接用倾析法转移溶液和沉淀至漏斗,再打开水龙头抽滤
D.洗涤晶体时,先关小水龙头,用蒸馏水缓慢淋洗,抽滤完毕时,应先断开橡皮管,以防倒吸
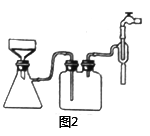
(4)碱式次氯酸镁固体的消毒能力可用“有效氯”的含量来衡量。“有效氯”的含量:从HI中氧化出相同量的I2所需Cl2的质量与指定化合物的质量之比,常以百分数表示。有效氯含量=
×100%
若测得所得碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%。则“有效氯”含量的测定值与理论值相比,是________(填偏高、偏低、相等),推测产品中最可能含有的杂质是___________________。
高三化学简答题简单题查看答案及解析
-
为探究某矿石(仅含两种元素)的组成和性质,设计并完成如下实验:
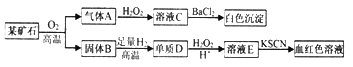
请回答:(1)某矿石的组成元素为__________(用元素符号表示)。
(2)气体A与H2O2溶液反应的化学方程式是________________。
(3)写出D→E的离子方程式____________________。
高三化学简答题简单题查看答案及解析
-
Ⅰ:氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+=Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作用是______。
(2)写出CuH在氯气中燃烧的化学反应方程式:___________。
(3)CuH溶解在稀盐酸中生成的气体是___________,如果反应中生成了标准状况下22.4L的气体,被还原的离子得电子的物质的量是__________。
Ⅱ:用高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,则化学反应方程式为___。
(2)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是_______。
(3)某同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他们进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001 mol·L-1 AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL。
①水样中Cl-的物质的量浓度是_______________。
②已知Ksp(AgCl) = 1.78×10-10,Ksp(Ag2CrO4) = 2.00×10-12。如在滴定终点时,测得溶液中CrO42-的浓度是5.0×10-3 mol·L-1。试计算此时溶液中Cl-的浓度是________________。
高三化学简答题简单题查看答案及解析
-
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)己知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)== CO2(g) +H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式______________;
(2)在一定条件下,某密闭容器中进行上述二氧化碳与氢气制备甲醇的反应,反应过程中部分数据如下表:
反应条件
反应时间
CO2(mol)
H2(mol)
CH3OH(mol)
H2O(mol)
恒温恒容
(T1℃、2L)
Omin
2
6
0
0
10min
4.5
20min
1
30min
1
①0〜l0min内,用H2O(g)表示的化学反应速率v(H2O)=__mol/(L·s)
②达到平衡时,该反应的平衡常数K=____(用分数表示),平衡时H2的转化率是____。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1___T2(填“>”、“<”或“=”),理由是_____。在其他条件不变的情况下,若30min时向容器中再充入lmolCO2 (g)和lmolH2O (g),则平衡____移动(填“正向”、“逆向”或“不”)。
(3)以甲醇为燃料的新型燃料电池,正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。
①负极的电极反应式是________________;
②若以该燃料电池作为电源,用石墨作电极电解500mL饱和食盐水,当两极共收集到标准状况下的气体1.12L (不考虑气体的溶解)时,所得溶液的pH=____ (假设反应前后溶液体积不变)。
高三化学简答题简单题查看答案及解析
-
已知A原子只有一个未成对电子,M电子层比N电子层多11个电子,试回答下列问题:
(1)N电子层的s轨道和p轨道中只有一个未成对电子的元素有哪些?
(2)写出A原子的电子排布式和元素符号。
(3)指出元素A在周期表中的位置。
(4)指出元素A的最高化合价和最低化合价。
高三化学简答题简单题查看答案及解析
-
工业上可用CO2与H2反应生成甲醇,在T ℃下,将1 mol CO2和2 mol H2充入5 L恒容密闭容器中发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得H2的物质的量随时间的变化情况如下图中曲线Ⅰ所示。
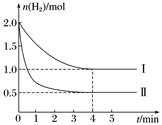
(1)按曲线Ⅰ计算反应从0到4 min时,v(H2)=____________________。
(2)在T ℃时,若仅改变某一外界条件时,测得H2的物质的量随时间的变化情况如图中曲线Ⅱ所示,则改变的外界条件为_______________________________________;
反应按曲线Ⅱ进行,计算达到平衡时容器中c(CO2)=______________。
(3)判断该反应达到平衡的依据为________(填字母)。
A.混合气体的平均相对分子质量不随时间改变
B.3v(H2)正=v(CH3OH)逆
C.混合气体的压强不随时间改变
D.单位时间内生成CH3OH和H2O的物质的量相同
高三化学简答题简单题查看答案及解析
-
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。实验室模拟海水中提取镁的主要步骤如下:
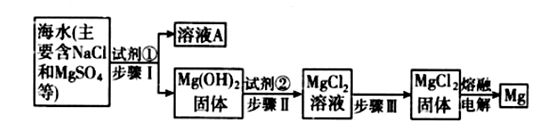
(1) 步骤Ⅰ分离物质需要的主要玻璃仪器有_____________;试剂①是__________(填化学式)。
(2)溶液A中的阴离子主要有______________________。
(3)由MgCl2.6H2O固体得到MgCl2应在什么条件下加热?____________________。
高三化学简答题简单题查看答案及解析
-
自然界中往往存在许多有趣也十分有意义的现象,下表列出了若干化合物的结构简式、化学式、相对分子质量和沸点。
结构简式
化学式
相对分子质量
沸点/℃
(1)H-OH
H2O
18
100
(2)CH3-OH
CH4O
32
64
(3)CH3CH2OH
C2H6O
46
78
(4)CH3COOH
C2H4O2
60
118
(5)CH3-O-CH3
C2H6O
58
56
(6)CH3CH2CH2OH
C3H8O
60
97
(7)CH3CH2OCH3
C3H8O
60
11
它们的沸点说明什么问题?
高三化学简答题简单题查看答案及解析
-
解释邻羟基苯甲酸在CCl4中的溶解度比对羟基苯甲酸大。
高三化学简答题简单题查看答案及解析