-
工业上用Na2SO3溶液处理硫酸厂的废气SO2得 NaHSO3溶液,然后用惰性电极电解 NaHSO3废水(原理如图所示)使吸收液再生,两膜中间的Na+和HSO3-可通过离子交换膜。下列叙述正确的是

A. 通电后中间隔室的HSO3-离子通过C膜向左侧迁移,左侧电极室溶液pH增大
B. 图中A连接电源的正极,B连接电源的负极
C. 阳极反应为HSO3-+H2O-2e-=SO42-+3H+,阳极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的Na2SO3生成
-
工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示,下列说法正确的是( )
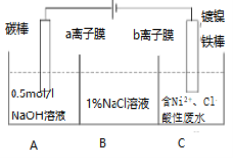
已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.铁棒上发生的电极反应:2H++2e-===H2↑
B.电解过程中,B中NaCl溶液的质量分数将不断增大
C.a膜为阴离子交换膜,b膜为阳离子交换膜
D.若将图中a离子膜去掉,将A、B两室合并,则电解反应总方程式将不发生改变。
-
工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是( )
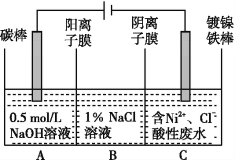
已知:①Ni2+在弱酸性溶液中发生水解②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH--4e-O2↑+2H2O
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断减小
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
-
工业上用电解法处理含镍酸性废水并得到单质镍的原理如图所示。下列说法错误的是
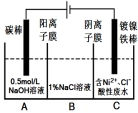
已知:①Ni2+在弱酸性溶液中发生水解;
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH−−4e−= O2↑+2H2O
B. 为了提高镍的产率,电解过程中需要控制废水的pH
C. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
-
某兴趣小组用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入右图装置(电极均为惰性材料)进行实验。下列说法正确的是

A. N极为负极
B. 反应一段时间后,左侧电解质溶液的pH增大
C. M极发生的电极反应为SO2+2H2O-2e-=SO42-+4H+
D. 在相同条件下,M、N两极上消耗的气体体积之比为1:2
-
工业上可以用Na2SO3溶液吸收SO2,并用电解法处理吸收后所得NaHSO3溶液以实现吸收液的回收再利用,装置如图所示,则工作一段时间后,下列说法正确的是
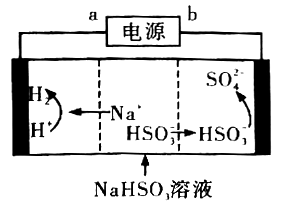
A. 电源a端是正极
B. 阴极区的pH减小
C. 阳极的电极反应式为HSO3--2e-+H2O=SO42-+3H+
D. 电路中每通过0.2mol电子,能产生2.24LH2
-
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式: 。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式: 。
③写出步骤(Ⅲ)反应的离子方程式: 。
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42-的转化率。
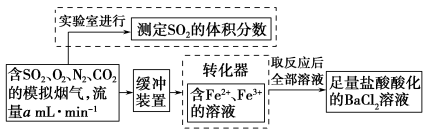
①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是 。(填写序号)
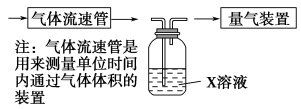
A.碘的淀粉溶液B.酸性高锰酸钾溶液
C.氢氧化钠溶液D.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO 的转化率,已知气体流速,还需测定的数据有 、 。
的转化率,已知气体流速,还需测定的数据有 、 。
-
工业含铬废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀。利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源、以废治废,还能节约生产成本。
(1)工业上处理100L Cr2O72-含量为108mg∙L-1的含铬废水,至少需要______L(标准状况) SO2。
(2)已知:Ksp[Cr(OH)3]=1×10-30,室温下,除去被SO2还原所得溶液中的Cr3+(使其浓度小于1×10-6mol∙L-1),需调节溶液pH______。
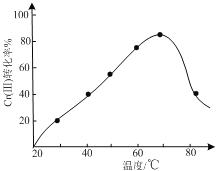
(3)三价铬Cr(III)与双氧水反应可用于合成铬黄(PbCrO4),控制其他条件不变,调节反应温度,考察反应温度对Cr(III)转化率的影响(如图所示),温度超过70℃时,Cr(III)转化率下降的原因是______。
(4)光照下,草酸(H2C2O4)也能将Cr2O72-转化为Cr3+,化学式为Al2Fe(SO4)4的某发盐(毛发状,在空气中能被氧化)对该反应具有催化作用,为确定一瓶久置发盐的化学成分,学习小组进行如下实验:
取一定质量的发盐样品溶于足量的稀硫酸中,将溶液分为两等份,其中一份与酸性KMnO4溶液充分反应(反应后MnO4-被还原成Mn2+),消耗浓度为0.4000mol∙L-1的KMnO4溶液20.00mL;往另一份溶液中加入足量稀氨水,在空气中微热并搅拌使之充分反应,待沉淀不再变化后过滤,将沉淀洗涤并充分灼烧后称量,得9.100g干燥固体粉末。通过计算与合理猜想,推测该久置发盐的可能化学组成(请给出计算过程与推测理由)。_________
-
工业上用Na2SO3溶液吸收硫酸工业尾气中的SO2,并通过电解方法实现吸收液的循环再生。其中阴、阳离子交换膜组合循环再生机理如图所示,下列有关说法中正确的是
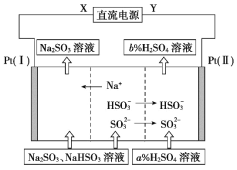
A.X应为直流电源的正极
B.电解过程中阴极区pH升高
C.图中的b%<a%
D.SO32-在电极上发生的反应为SO32-+2OH--2e-=SO42-+2H2O
-
工业上用Na2SO3溶液吸收硫酸工业尾气中的SO2,并通过电解方法实现吸收液的循环再生。其中阴、阳离子交换膜组合循环再生机理如图所示,下列有关说法中正确的是
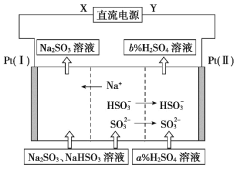
A.X应为直流电源的正极
B.电解过程中阴极区pH升高
C.图中的b%<a%
D.SO32-在电极上发生的反应为SO32-+2OH--2e-=SO42-+2H2O










