-
N、Al、Si 、S四种元素相比较,原子半径最大的是
A. S B. N C. Al D. Si
高三化学单选题简单题查看答案及解析
-
下列递变情况中,正确的是( )
A. Na、Mg、Al原子的最外层电子数依次减少
B. Si、P、S元素的最高正价依次降低
C. C、N、O的原子半径依次减小
D. Li、Na、K的金属性依次减弱
高三化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A. Si、P、S、Cl原子半径依次增大
B. HF、HCl、HBr、HI稳定性依次减弱
C. C、N、O、F 元素的最高正化合价依次升高
D. NaOH、Mg(OH)2、Al(OH)3碱性依次增强
高三化学单选题简单题查看答案及解析
-
C、N、O、Na、Al、Si、S、Cl是常见的八种元素
请回答下列问题:
(1)Si在元素周期表中的位置为__ ;CO2的电子式是_______。
(2)上述元素中原子半径最大的是(写元素符号)______;最高价氧化物对应的水化物酸性最强的是__________(写化学式)。
(3)下列事实能说明O元素的非金属性比S元素的非金属性强的是__。
a.O2与H2S溶液反应,溶液变浑浊
b.O和S两元素的简单氢化物受热分解,前者的分解温度高
c.在氧化还原反应中,1molO2比1molS得电子多
(4)金刚石具有优良的耐磨,耐腐蚀性,应用广泛。一定条件下,Na还原CCl4可制备金刚石。反应结束冷却至室温后,回收其中的CCl4的实验操作名称为_____,除去粗产品中少里钠的试剂为_______。
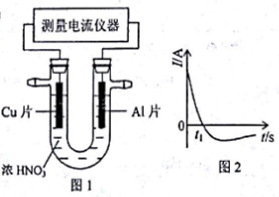
(5)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图l),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。0~t1时,原电池的负极是Al片,此时,正极的电极反应式是_______,溶液中的H+向__极移动。t1时,原电池中电子流动方向发生改变,其原因是:___________。
高三化学简答题中等难度题查看答案及解析
-
下列说法不能用元素周期律解释的是( )
A.浓硫酸的氧化性强于稀硫酸
B.与冷水反应的速率:Na>Mg
C.向淀粉KI溶液中滴入氯水,溶液变蓝
D.原子半径:Al>Si>P
高三化学单选题简单题查看答案及解析
-
下列说法不能用元素周期律解释的是
A.浓硝酸的氧化性强于稀硝酸 B.与冷水反应的速率:Na>Mg
C.向淀粉KI溶液中滴入溴水,溶液变蓝 D.原子半径:Al>Si>P
高三化学单选题中等难度题查看答案及解析
-
下列说法中,不能用元素周期律解释的是
A. 向淀粉KI溶液中滴入溴水,溶液变蓝 B. 与冷水反应的速率:Na>Mg
C. 浓硝酸的氧化性强于稀硝酸 D. 原子半径:Al>Si>P
高三化学选择题简单题查看答案及解析
-
下列有关元素或者化合物性质的比较中,正确的是
A. 结构相似的分子晶体的熔沸点,与相对分子质量呈正相关,所以
B. Na、Mg、Al原子最外层电子数依次增多,原子半径也依次增大
C. 在分子中,两个原子间的键长越长,键能越大
D. 一般而言,晶格能越高,离子晶体的熔点越高、硬度越大
高三化学单选题中等难度题查看答案及解析
-
下列有关性质的比较,不能用元素周期律解释的是
A. 原子半径:C > O B. 酸性:HCl > H2SiO3
C. 热稳定性:H2O > H2S D. 金属性:Na > Al
高三化学单选题简单题查看答案及解析
-
依据元素周期表及元素周期律,下列推断正确的是( )
A.同周期主族元素的原子形成的简单离子电子层结构相同
B.C比Si的原子半径小,CH4的稳定性比SiH4弱
C.Na、Mg、Al失电子能力和其最高价氧化物对应的水化物的碱性均依次减弱
D.在元素周期表金属与非金属的分界处可以寻找催化剂和耐高温、耐腐蚀的合金材料
高三化学选择题中等难度题查看答案及解析