-
丙烷燃烧可以通过以下两种途径:
【途径Ⅰ】4.4g丙烷完全燃烧放出热量为a kJ,写出丙烷燃烧的热化学方程式:
【途径Ⅱ】等量丙烷按下列反应进行:
①C3H8(g)═C3H6(g)+H2(g)△H=+b kJ/mol
②2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=﹣c kJ/mol
③2H2(g)+O2 (g)═2H2O(l)△H=﹣d kJ/mol (abcd均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 途径Ⅱ放出的热量.
(2)由于C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量 生成物具有的总能量.那么在化学反应时,反应物就需要 能量才能转化为生成物.因此其反应条件是
(3)b与a、c、d的数学关系式是 .
高三化学填空题困难题查看答案及解析
-
化学能与热能、电能的相互转化具有实际意义,结合所学内容回答下列问题。
(1)1g硫粉完全燃烧生成二氧化硫气体,放出9.36kJ的热量,写出硫燃烧的热化学方程式___。
(2)以下是部分共价键的键能数据:
化学键
H-S
S-S
O=O
H-O
键能(kJ•mol-1)
364
266
496
463
热化学方程式:2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-akJ•mol-1。反应产物中的S实为S8分子,是一个八元环状分子(如图1所示)。计算,a=__。

(3)工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而将其除去。图2为电解装置示意图(电极材料分别为铁和石墨)。
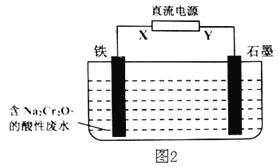
请回答:
①完成铁电极附近溶液中所发生反应的离子方程式:Cr2O72-+6Fe2++14H+=2__+6___+7__。
②写出石墨电极处的电极反应式:__。
③电解时用铁作阳极而不用石墨作阳极的原因是__。
④电解结束后,若要检验电解液中是否还有Fe2+存在,则可选用的试剂是___(填序号)。
a.KSCN溶液
b.CuCl2溶液
c.NaOH溶液
d.K3[Fe(CN)6]溶液
高三化学综合题中等难度题查看答案及解析
-
随着我国家用汽车数量的迅猛增加,加速了城市空气污染.往汽油中添加10%至15%的酒精,可以减少70%以上的污染.已知每46g酒精完全燃烧生成液态水时放出的热量为1367kJ.请写出酒精完全燃烧的热化学方程式:______.
高三化学解答题中等难度题查看答案及解析
-
己知丙烷的燃烧热△H=-2215 kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为( )
A.55 kJ B.220 kJ C. 550 kJ D.1108 kJ
高三化学选择题简单题查看答案及解析
-
己知丙烷的燃烧热△H=-2215KJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为( )
A.55 kJ B.220 kJ C. 550 kJ D.1108 kJ
高三化学选择题中等难度题查看答案及解析
-
[2015·海南]已知丙烷的燃烧热ΔH=−2 215 kJ·mol−1。若一定量的丙烷完全燃烧后生成1.8 g水,则放出的热量约为
A.55 kJ B.220 kJ C.550 kJ D.1 108 kJ
高三化学选择题中等难度题查看答案及解析
-
已知丙烷((C3H8)的燃烧热△H=﹣2215kJ•mol-1,若一定量的丙烷完全燃烧后生成 1.8g 水,则放出的热量约为
A.55kJ B.220kJ C.550kJ D.1108kJ
高三化学选择题中等难度题查看答案及解析
-
(1)写出下列物质的化学式:硫铁矿 石膏
(2)SiO2是硅最重要的化合物,其用途是 (举一例)
(3)已知1g乙醇完全燃烧生成液态水放出29.7kJ的热量,写出乙醇燃烧热的热化学方程式 。
(4)配平化学方程式:___K2Cr2O7+___HCl——___KCl+___CrCl3+___Cl2↑+___H2O
高三化学填空题中等难度题查看答案及解析
-
实验测得4g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出90.8 kJ的热量。试写出甲醇燃烧热的热化学方程式________。
高三化学填空题中等难度题查看答案及解析
-
(1)在298K时,1molCH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.0 kJ。写出该反应的热化学方程式________。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18克液态水,并放出515kJ热量,则CH4和CO的物质的量分别为________、________mol.
(2)利用该反应设计一个燃料电池:用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入甲烷和氧气。通入甲烷气体的电极应为________极(填写“正”或“负”),该电极上发生的电极反应是 (填字母代号)。
a. CH4—e- + 2O2 == CO2 + 2H2O
b. CH4—8e- + 10OH- == CO32- + 7H2O
c. O2 + 2H2O + 4 e- == 4OH-
d. O2—4 e- + 4H+ == 2H2O
(3)在如图所示实验装置中,石墨棒上的电极反应式为________;如果起始时盛有1000mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是;若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入________(填物质名称),其质量约为________。
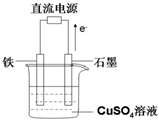
高三化学填空题困难题查看答案及解析