-
已知:常阻下, Ksp.(ZnS)=1.6×10—24; pM=—lgc(M2+)(MI2+为Cu2+或Zn2+)。常温下,向10 mL 0.10 mol/L CuCl2溶液中滴加0.10 mol/L Na2S溶液,滴加过程中pM与Na2S溶液体积(V) 的关系如图所示。下列说法错误的是( )
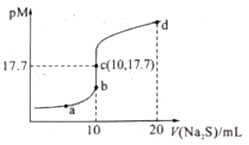
A.Ksp(CuS) 的数量级为10-36
B.a点溶液中, c(Na+) =2[c(S2—) +c(HS—) +c(H2S)]
C.d点溶液中:c(Na+)>c(Cl—)>c(S2—)>c(H+)
D.相同条件下, 若用等浓度等体积的ZnCl2溶液代替上述CuCl2溶液, 则反应终点c向b方向移动
-
已知:常阻下, Ksp.(ZnS)=1.6×10—24; pM=—lgc(M2+)(MI2+为Cu2+或Zn2+)。常温下,向10 mL 0.10 mol/L CuCl2溶液中滴加0.10 mol/L Na2S溶液,滴加过程中pM与Na2S溶液体积(V) 的关系如图所示。下列说法错误的是( )

A.Ksp(CuS) 的数量级为10-36
B.a点溶液中, c(Na+) =2[c(S2—) +c(HS—) +c(H2S)]
C.d点溶液中:c(Na+)>c(Cl—)>c(S2—)>c(H+)
D.相同条件下, 若用等浓度等体积的ZnCl2溶液代替上述CuCl2溶液, 则反应终点c向b方向移动
-
已知:常温下,Ksp(ZnS)=1.6×10-24;pM=-lgc(M2+)(M2+为Cu2+或Zn2+)。常温下,向10mL0.10mol·L-1CuCl2溶液中滴加0.10mol·L-1Na2S溶液,滴加过程中pM与Na2S溶液体积(V)的关系如图所示。下列说法错误的是
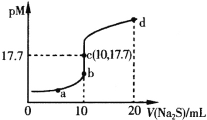
A.Ksp(CuS)的数量级为10-36
B.a点溶液中,c(Na+)=2[c(S2-)+c(HS-)+c(H2S)]
C.d点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(H+)
D.相同条件下,若用等浓度等体积的ZnCl2溶液代替上述CuCl2溶液,则反应终点c向上移动
-
已知:ZnS呈白色,CuS呈黑色;常温下,Ksp(ZnS)=3.0×10-25,Ksp(CuS)=1.0×10-36;pM=-lgc(M2+)。常温下,向10.0mL0.20mol•L-1ZnCl2溶液中逐滴滴加0.10mol•L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法不正确的是( )
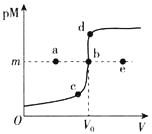
A.V0=20.0mL,m=12.5- lg3
lg3
B.相同实验条件下,若用10.0mL0.20mol•L-1CuCl2溶液代替上述ZnCl2溶液,则反应终点b向d方向移动
C.若c(ZnCl2)=0.10mol•L-1,则反应终点可能为e点
D.向b点浊液中加入0.002molCuCl2固体,白色沉淀变黑色
-
常温下.用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对 数值lgc(S2-)与lgc(M2+)关系如下图所示,下列说法正确的是
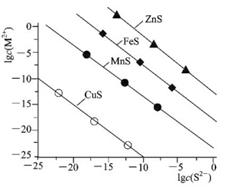
A.室温时.向ZnS悬浊液中加人ZnSO4固体,.Ksp(ZnS)将随之减小
B.Na2S溶液中:c(OH-)<c(H+)+c(HS-)+c(H2S)
C.为除去MnCl2溶液中混有的少量 CuCl2,可加入适量Na2S固体,充分搅拌后过滤
D.向100 mL浓度均为1×10-5mol/L的Fe2+、Zn2+混合溶液中逐滴加入1×10-4mol/LNa2S溶液,Fe2+先沉淀,证明Ksp(FeS)<Ksp(ZnS)
-
[2019·湖南省常德市高三第一次模拟考试]已知:常温下,Ksp(CuS)=1.0×10-36,K sp(HgS)=1.6×10-52;pM=-lgc(M2+)。常温下,向10.0mL0.20mol·L-1Cu(NO3)2溶液中逐滴滴加0.10mo l·L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法错误的是
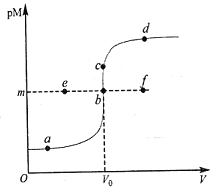
A.V0=20.0mL,m=18
B.若c[Cu(NO3)2]=0.01mol·L-1,则反应终点可能为e点
C.a、b、d三点中,由水电离的c(H+)和c(OH-)的积最大的为b点
D.相同条件下,若用等浓度等体积的Hg(NO3)2溶液代替上述Cu(NO3)2溶液,则反应终点b向c方向移动
-
已知:常温下,Ksp(CuS)=1.0×10-36,K sp(HgS)=1.6×10-52;pM=-lgc(M2+)。常温下,向10.0mL0.20mol·L-1Cu(NO3)2溶液中逐滴滴加0.10mo l·L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法错误的是
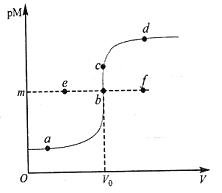
A. V0=20.0mL,m=18
B. 若c[Cu(NO3)2]=0.01mol·L-1,则反应终点可能为e点
C. a、b、d三点中,由水电离的c(H+)和c(OH-)的积最大的为b点
D. 相同条件下,若用等浓度等体积的Hg(NO3)2溶液代替上述Cu(NO3)2溶液,则反应终点b向c方向移动
-
25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法正确的是
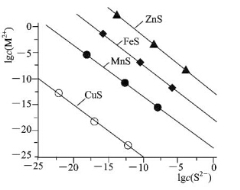
A.Ksp(CuS)约为l×10-20
B.向Cu2+浓度为10-5mol•L-1废水中加入ZnS粉末,会有CuS沉淀析出
C.向l00mL浓度均为10-5mol•L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol•L-1 Na2S溶液,Zn2+先沉淀
D.Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+)
-
某温度时,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法正确的是
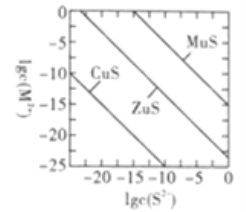
A. 三种离子对应的硫化物中Ksp(CuS)最小,约为1×10-20
B. 向MnS的悬浊液中加入少量水。沉淀溶解平衡向溶解的方向移动,c(S2-)增大
C. 可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2
D. 向浓度均为1×10-5mol/L的Cu2+、 Zn2+、Mn2+混合溶液中逐滴加入1×10-4mol/的Na2S溶液,Mn2+最先沉淀
-
某温度时,可用K2S沉淀Cu2+、Mn2+、Zn2+三种离子(M2+ ),所需S2-最低浓度的对数值lgc(S2-)与lg(M2+)的关系如图所示。下列说法正确的是
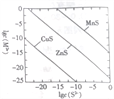
A. 三种离子对应的硫化物中Ksp(CuS)最小,约为1×10-20
B. 可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2
C. 向MnS的悬浊液中加入少量水,沉淀溶解平衡向溶解的方向移动,c(S2-)增大
D. 向浓度均为1×10-5 mol·L-1的Cu2+、Zn2+、Mn2+混合溶液中逐滴加入l×l0-4 mol·L-1的Na2S溶液,Zn2+最先沉淀









