-
锰的单质及其化合物的用途非常广泛 回答下列问题:
回答下列问题:

⑴基态锰原子的外围电子排布式为______________________,其d轨道中未成对电子数为__________。
⑵MnO的熔点(1650℃)比MnS的熔点(1610℃)高原因是_____________________________________。
⑶锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
①THF中的元素的电负性从大到小的顺序是__________________。
②与Mn2+形成配位键的原子为______(填元素符号)。
③BH4-的空间构型为_______,其中B原子的杂化轨道类型为________。
④写出两种与BH4-互为等电子体的分子或离子___________。
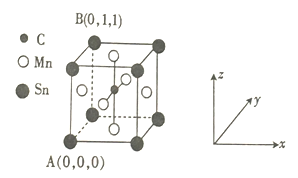
⑷一种磁性材料的单晶胞结构如图所示。
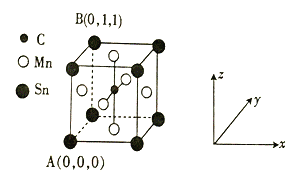
①该晶胞中碳原子的原子坐标为________。
②Mn在晶体中的堆积方式为_______(填“简单立方”“体心立方”或“面心立方最密”)堆积。
③若该晶胞的边长为a pm,NA表示阿伏加德罗常数的数值,则该晶体密度的表达式为ρ = ___________________ g∙cm-3。
-
锰的单质及其化合物的用途非常广泛.回答下列问题:
(1)基态锰原子的核外电子排布式为_______,其d轨道中未成对电子数为__________.
(2)MnO的熔点(1650℃)比MnS的熔点(1610℃)高,它们都属于___晶体。前者熔点较高的原因是_____________。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
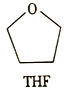
① 与Mn2+形成配位键的原子为_______(填元素符号)。
② BH4-的空间构型为_______,其中B原子的杂化轨道类型为________。
③ 写出两种与BH4-互为等电子体的分子或离子:___________。
(4)一种磁性材料的单晶胞结构如图所示。
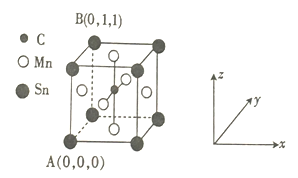
① 该晶胞中碳原子的原子坐标为________。
② Mn在晶体中的堆积方式为________(填“简单立方”“体心立方”“面心立方最密”或“六方最密") 堆积。
③ 若该晶胞的边长为a pm,NA表示阿伏加德罗常数的数值,则该晶体密度的表达式为ρ=_____。
-
锰的单质及其化合物的用途非常广泛.回答下列问题:
(1)基态锰原子的核外电子排布式为_______,其d轨道中未成对电子数为__________.
(2)MnO的熔点(1650℃)比MnS的熔点(1610℃)高,它们都属于___晶体。前者熔点较高的原因是_____________。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
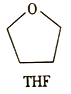
① 与Mn2+形成配位键的原子为_______(填元素符号)。
② BH4-的空间构型为_______,其中B原子的杂化轨道类型为________。
③ 写出两种与BH4-互为等电子体的分子或离子:___________。
(4)一种磁性材料的单晶胞结构如图所示。
① 该晶胞中碳原子的原子坐标为________。
② Mn在晶体中的堆积方式为________(填“简单立方”“体心立方”“面心立方最密”或“六方最密") 堆积。
③ 若该晶胞的边长为a pm,NA表示阿伏加德罗常数的数值,则该晶体密度的表达式为ρ=_____。
-
氮和磷元素的单质和化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列问题:
(1)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为___,其中的阴离子的空间构型为___。
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子的形式存在。N4H44+根系易吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。1个N4H44+中含有___个σ键。
(3)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因___。
(4)P4S3可用于制造火柴,其分子结构如图1所示。
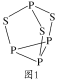
①P4S3分子中硫原子的杂化轨道类型为___。
②每个P4S3分子中含孤电子对的数目为___。
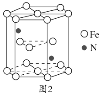
(5)某种磁性氮化铁的晶胞结构如图2所示,该化合物的化学式为___。若晶胞底边长为anm,高为cnm,则这种磁性氮化铁的晶体密度为__g·cm−3(用含a、c和NA的式子表示)
(6)高温超导材料,是具有高临界转变温度(Te)能在液氮温度条件下工作的超导材料。高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为[Ar]__;化合物中,稀土元素最常见的化合价是+3,但也有少数的稀土元素可以显示+4价,观察下面四种稀土元素的电离能数据,判断最有可能显示+4价的稀土元素是___(填元素符号)。
几种稀土元素的电离能(单位:kJ·mol−1)
| 元素 | I1 | I2 | I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 7019 |
| Y(铱) | 616 | 1181 | 1980 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3547 |
-
磷的单质及其化合物用途非常广泛。回答下列问题:
(1)基态磷原子价电子轨道表示式为______________________;磷的第一电离能比硫大,其原因是_____________________________________________。
(2)已知反应6P2H4==P4+ 8PH3↑。P2H4分子中磷原子杂化类型是________________;P4分子的几何构型是________________________。
(3)N和P同主族。
①NH3的沸点比PH3高,其原因是_________________________;NH3分子中键角比PH3分子中键角大,其原因是______________________________________________。
②氮原子间可形成氮氮双键或氮氮叁键,而磷原子之间难以形成双键或叁键。从原子结构角度分析,原因是___________________________________________。
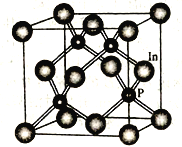
(4)磷化铟是一种半导体材料,其晶胞如下图所示,晶胞参数为a nm。In 的配位数为_______________;与In原子间距离为 a nm 的In 原子有________个。
a nm 的In 原子有________个。
-
卤族元素及其化合物的用途非常广泛。回答下列问题:
(1)基态氯原子价电子轨道表示式(电子排布图)为___;处于最高能级电子云轮廓图形状为____。
(2) 和
和 的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
的中心原子相同且杂化方式也相同,它们的键长和键角如下图所示:
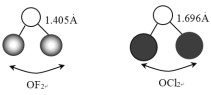
①O-F键的键长比O-Cl键的小,其原因是______。
②键角:∠FOF_____(填“>”、“<”或“=”)∠ClOCl。
(3)①试解释酸性HBrO4>HBrO3的原因_________ 。
②试解释酸性HClO3>HBrO3>HIO3的原因_________ 。
(4) 的熔点为1040℃;
的熔点为1040℃; 的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
的熔点为194℃,沸点为181℃,前者的熔点比后者高得多,其原因是______。
(5)氯化亚铜晶胞结构如图所示,晶胞参数a=0.542nm。
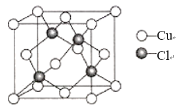
①Cu+的配位数为_____。
②氯化亚铜的密度为____ (用含NA的计算式表示)。
(用含NA的计算式表示)。
-
(化学选修3——物质结构与性质)硫、钴及其相关化合物用途非常广泛。回答下列问题:
(1)基态Co原子价电子轨道表达式为____,第四电离能I4(Co)<I4(Fe),其原因是____;Co与Ca同周期且最外层电子数相同,单质钴的熔沸点均比钙大,其原因是____。
(2)单质硫与熟石灰加热产物之一为CaS3,S32-的空间构型是____,中心原子杂化方式是____,与其互为等电子体的分子是____(任写1种)。
(3) K 和Na位于同主族,K2S的熔点为840℃,Na2S的熔点为950℃,前者熔点较低的原因是____。
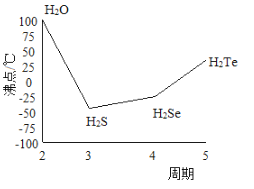
(4)S 与O、Se、Te位于同一主族,它们的氢化物的沸点如下左图所示,沸点按图像所示变为的原因是____。
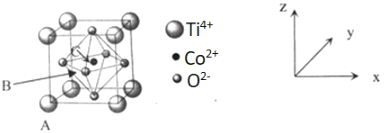
(5)钴的一种化合物晶胞结构如上图所示。
①已知A点的原子坐标参数为(0,0,0),C点为(1/2,1/2,1/2),则B点的原子坐标参数为____。
②已知晶胞参数为a=0.5485nm,则该晶体的密度为____g·cm-3 (列出计算表达式即可)。
-
镁、硅及其化合物用途非常广泛。回答下列问题:
(1)基态Si原子价层电子的电子排布图(轨道表达式)为__________,基态Mg原子电子占据最高能级的电子云轮廓图为__________形。
(2)Mg2C3与水反应可生成H2C=C=CH2,中间的碳原子杂化方式是__________,反应所涉及的元素中电负性最大的是__________(填元素符号),Mg2C3和H2C=C=CH2中均存在(填字母)__________。
A.配位键 B.σ键 C.π键 D.氢键
(3)MgO晶格能可通过图1的bom- Haber循环计算得到。
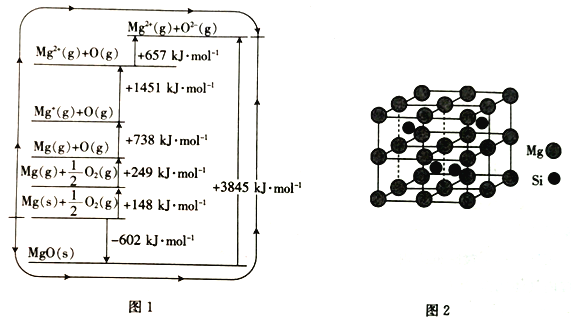
Mg的第二电离能为__________kJ·mol-1;O=O键的键能为_________kJ·mol-1;MgO的晶格能为__________kJ·mol-1。
(4)Mg2Si晶胞结构如图2所示,已知其密度为1.94g·cm-3,NA为阿伏加德罗常数的值。
①则晶胞参数a=__________nm(列出计算式)
②Mg2Si的另一种表示中,四个Mg处于上图所示立方体中的Si的位置,则Si处于____________。
-
锰及其化合物用途非常广泛。回答下列问题:
(1)基态Mn原子的电子排布式为_________。
(2)MnCl2熔点(650℃)比MnO熔点(1650℃)低, 其主要原因是____________。
(3)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____,该分子中碳原子的杂化方式为_______;C、H、N的电负性从大到小的顺序为________。
③配体CO的等电子体有:_________(任写一种),N2O的分子空间构型为__________。
(4)某种含锰特殊材料的晶胞结构如下图所示,该晶体的化学式为:_________;若晶胞边长为a nm,用NA表示阿伏加德罗常数的值,则该晶胞的密度为____( 列出代数式即可)。
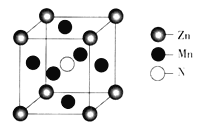
-
铜是人类最早使用的金属之一,金属铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态+2价铜离子M能层电子排布式是___________;第4周期中基态原子未成对电子数与铜原子相同的元素有________种。
(2)Cu+能与SCN-形成CuSCN沉淀。请写出一种与SCN-互为等电子体的微粒_________。SCN-对应的酸有硫氰酸(H-S-CN)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是_______(填名称),原因是_____________________。
(3)Cu2+能与NH3形成平面正方形的[Cu(NH3)4]2+。NH3分子的空间构型为__________;[Cu(NH3)4]2+中Cu采取dspx杂化,x的值是__________。
(4)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,前者熔点较高,其原因是___________。
(5)Cu3N 的晶胞(立方)结构如下图所示:
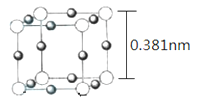
①距离最近的两个Cu+间的距离为________nm。(保留两位小数)
②Cu3N 晶体的密度为____________ g·cm-3。(NA表示阿伏伽德罗常数的值,列出计算式,不必计算出结果)
回答下列问题:














