最近我国科学家研制一种具有潜力的纳米电子学材料——石墨炔,图中丁为它的结构片段。下列有关说法中,错误的是( )

A. 甲分子中的6个溴原子位于同一平面上
B. 丙的二氯代物有2种
C. 丙能使酸性高锰酸钾溶液褪色
D. 石墨炔和C60是碳的同素异形体
高三化学单选题简单题
最近我国科学家研制一种具有潜力的纳米电子学材料——石墨炔,图中丁为它的结构片段。下列有关说法中,错误的是( )

A. 甲分子中的6个溴原子位于同一平面上
B. 丙的二氯代物有2种
C. 丙能使酸性高锰酸钾溶液褪色
D. 石墨炔和C60是碳的同素异形体
高三化学单选题简单题
最近我国科学家研制一种具有潜力的纳米电子学材料——石墨炔,图中丁为它的结构片段。下列有关说法中,错误的是( )

A. 甲分子中的6个溴原子位于同一平面上
B. 丙的二氯代物有2种
C. 丙能使酸性高锰酸钾溶液褪色
D. 石墨炔和C60是碳的同素异形体
高三化学单选题简单题查看答案及解析
我国科学家将石墨烯(由石墨剥离的层状结构)和碳纳米管经低温脱水处理,获得了一种“最轻材料”。该材料具有超强的吸附能力,且有望成为理想的储能保温、催化载体和吸音材料。下列有关说法正确的是( )
A.石墨烯属于有机物 B.该材料吸油过程为物理变化
C.碳纳米管是碳的一种同位素 D.碳纳米管属于胶体分散系
高三化学单选题简单题查看答案及解析
我国科学家将石墨烯(由石墨剥离的层状结构)和碳纳米管经低温脱水处理,获得了一种“最轻材料”。该材料具有超强的吸附能力,且有望成为理想的储能保温、催化载体和吸音材料。下列有关说法正确的是( )
A.石墨烯属于有机物 B.该材料吸油过程为物理变化
C.碳纳米管是碳的一种同位素 D.碳纳米管属于胶体分散系
高三化学选择题中等难度题查看答案及解析
我国科学家将石墨烯(由石墨剥离的层状结构)和碳纳米管经低温脱水处理,获得了一种“最轻材料”。该材料具有超强的吸附能力,且有望成为理想的储能保温、催化载体和吸音材料。下列有关说法正确的是( )
A.石墨烯属于有机物 B.该材料吸音过程为物理变化
C.碳纳米管是碳的一种同位素 D.碳纳米管属于胶体分散系
高三化学选择题中等难度题查看答案及解析
近年来科学家制造出大量的新物质,对下列三种物质的相关说法错误的是( )
|
|
|
|
| 石墨烯:从石墨中分离出来,是最薄、最坚硬的纳米材料 | 石墨炔:平面网状结构的全碳分子,具有优良的化学稳定性 | 纳米碳管:具有优良的场发射性能,制作成阴极显示管、储氢材料 |
A. 石墨烯具有良好的导电性
B. 上述三种物质与金刚石互为同素异形体
C. 石墨炔孔径略大于H2分子的直径,可作H2的提纯薄膜
D. 上述三种物质与浓硫酸都能发生反应,但反应产物不同
高三化学单选题中等难度题查看答案及解析
硼烯具有优异的电学、力学、热学等属性,将成为继石墨烯之后又一种“神奇纳米材料”。科学家已成功合成多种结构的硼烯,如图为“皱褶”式硼烯的结构。下列说法错误的是( )

A.“皱褶”式硼烯中每个硼原子共用3对电子
B.“皱褶”式硼烯中硼原子达到8电子稳定结构
C.硼烯有望代替石墨烯作电极材料
D.氧化硼的水化物是一种弱酸,与过量OH-反应可生成B(OH)4-或BO2-
高三化学单选题中等难度题查看答案及解析
【化学—选修3:物质结构与性质】我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外电子排布式为 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属 分子(选填“极性”“非极性”),其立体构型为 。
(3)橙红色晶体羰基钴[Co2(CO)8]的熔点为52℃,可溶于多数有机溶剂。该晶体属于 晶体,三种元素电负性由大到小的顺序为(填元素符号) 。配体CO中σ键与π键数之比是 。
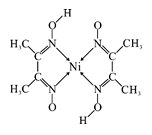
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如上图所示,分子内的作用力不可能含有 (填序号)。
A离子键 B共价键 C金属键 D配位键 E氢键
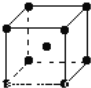
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r= cm。(只需列出计算式)
高三化学填空题简单题查看答案及解析
我国科学家已研制出一种可替代锂电池的“可充室温Na-CO2电池”,该电池结构如图所示。电极材料为钠金属片和碳纳米管,电解液为高氯酸钠-四甘醇二甲醚。下列说法错误的是( )
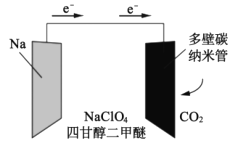
A.电池放电时钠金属片发生氧化反应
B.电池工作时,外电路流过0.01mol电子,负极材料减重0.23g
C.碳纳米管的作用主要是导电及吸附CO2,电池充电时,应该与直流电源的正极相连
D.放电时负极反应为:C+2Na2CO3-4e-=3CO2↑+4Na+
高三化学单选题中等难度题查看答案及解析
我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外电子排布式为____。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为____。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属____分子(选填“极性”“非极性”),其立体构型为____。
(3)橙红色晶体羰基钴的熔点为52℃,可溶于多数有机溶剂。该晶体属于____晶体,三种元素电负性由大到小的顺序为(填元素符号)____。配体CO中σ键与π键数之比是____。
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如图所示,分子内的作用力不可能含有____(填序号)。

A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r=____cm。(只需列出计算式)
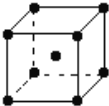
高三化学填空题简单题查看答案及解析
我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外未成对电子数为____。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为____。
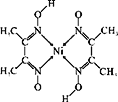
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属____分子(选填“极性”“非极性”),其中心原子的VSEPR构型为____。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于______晶体,三种元素电负性由大到小的顺序为(填元素符号)____。配体CO的任意一种等电子体的电子式:_________。配体CO中与Co形成配位键的原子是C非O,原因是_________。
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如图所示,分子内的作用力不可能含有__________(填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键 F. 范德华力
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r=____nm。(只需列出计算式)
高三化学综合题中等难度题查看答案及解析