-
习近平总书记指出“绿水青山就是金山银山”。下列观点合理的是( )
A.将工业废液排入海洋以减少河道污染
B.为了减少火电厂产生的大气污染,应将燃煤粉碎并鼓入尽可能多的空气
C.习总书记2018年4月2日参加北京植树节体现了绿色化学的思想
D.与2017年相比2018年某地区降水pH平均值增加了0.27,说明酸雨情况有所改善
高三化学单选题简单题查看答案及解析
-
习近平总书记指出“绿水青山就是金山银山”。下列观点合理的
A. 将工业废液排入海洋以减少河道污染
B. 为了减少火电厂产生的大气污染,应将燃煤粉碎并鼓人尽可能多的空气
C. 习总书记2018年4月2日参加北京植树节这体现了绿色化学的思想
D. 与2016年相比,2017年某地区降水pH平均值增加了0.27,说明酸雨情况有所改善
高三化学单选题中等难度题查看答案及解析
-
下列说法与“绿水青山就是金山银山”的绿色发展理念不一致的是
A. 将工业废液排入海洋以减少河道污染
B. 推广煤的液化、气化技术以提高煤的使用效率
C. 利用CO2制成全降解塑料可缓解日益严重的“白色污染”
D. 采用催化转化技术可将汽车尾气中的NOx和CO转化为无毒气体
高三化学单选题中等难度题查看答案及解析
-
2016年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作。下列做法不应该提倡的是
A. 用碱性废水中和处理酸性废水
B. 将工业废液排入海洋以减少河道污染
C. 生活污水无害化处理后用于绿化灌溉
D. 推广使用高效、低毒农药,减轻水体污染
高三化学选择题中等难度题查看答案及解析
-
十八大以来,习近平总书记在多个场合强调,“绿水青山就是金山银山”,对环境生态环保尤为重视,下列说法不符合绿色化学理念的是
A. 开发高效氢能、太阳能等新型电动汽车,以解决城市机动车尾气排放问题
B. 利用有机垃圾发酵生产沼气做生活燃料
C. 将造纸废水通过高压水井压到地下,节约成本
D. 积极开发废旧电池的综合利用技术,解决电池中的重金属对土壤和水体的污染
高三化学单选题简单题查看答案及解析
-
习总书记在十九大报告中明确指出:“宁要绿水青山,不要金山银山,而且绿水青山就是金山银山。”保护环境是我们的迫切需要。请回答下列问题:
(1)NH3和NO都是有毒气体,但在催化剂条件下,它们可通过反应得到对环境无害的N2和H2O:4NH3(g)+6NO(g)⇌5N2(g)+H2O(g)△H。
已知几种化学键的键能数据如下:
共价键
键能/kJ/mol
946
391
607
464
根据键能数据估算上述反应中△H=__________kJ/mol。
(2)CO2会带来温室效应。目前,工业上采用氢气还原CO2制备乙醇的方法已经实现:2CO2(g)+6H2(g)⇌C2H5OH(g)+3H2O(g)。在2L恒容密闭容器中充入4molCO2和8molH2,在一定温度下反应,测得混合气体中c(C2H5OH)与时间的关系如图所示。
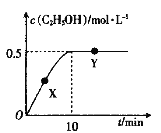
①0~10min内,v(H2O)=__________mol∙L-1∙min-1。
②反应达到平衡时,n(H2)=__________mol。
③在该温度下,该反应的化学平衡常数K__________(保留两位小数)。
(3)在恒容密闭容器中发生反应CH4(g)+4NO2(g)⇌4NO(g)+CO2(g)+2H2O(g)。下列说法能作为判断该反应达到化学平衡状态标志的是__________。
A.容器内混合气体的密度保持不变
B.v正(NO2)=4v逆(CO2)
C.容器内压强保持不变
D.单位时间内,消耗nmolNO2的同时生成nmolNO
(4)我国规定生活用水中铅排放的最大允许浓度为0.01mg/L。在某含铅废水中加入Na2S,当S2-浓度达到6.8×10-8mol/L时,水体中Pb2+浓度为_______mol/L[已知:Ksp(PbS)=3.4×10-28],此时是否符合排放标准?__________(填“是”或“否”)。
(5)电解法处理含氮氧化物废气,不仅可以减少环境污染,而且可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NO的装置如图所示(图中A、B极均为石墨电极)。
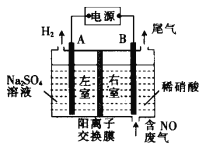
①B极的电极反应式为____________________。
②标准状况下,每消耗4.48LNO,A极得到氢气的体积为__________L。
高三化学综合题中等难度题查看答案及解析
-
习近平在十九大报告中指出“绿水青山就是金山银山”,下列做法与该理念无关的是( )
A. 提倡“低碳生活”,倡导“共享单车”出行 B. 合理食用含有蛋白质的食物,促进青少年健康成长
C. 降低住宅小区的容积率,增大公用绿地面积 D. 北方的冬季实行集中供热供暖,提高燃煤的利用率
高三化学单选题中等难度题查看答案及解析
-
“绿水青山就是金山银山”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)△H=-681.8kJ·mol-1对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
0
10
20
30
40
50
O2
1.00
0.79
0.60
0.60
0.64
0.64
CO2
0
0.42
0.80
0.80
0.88
0.88
0~10min内,平均反应速率υ(O2)__ mol·L-1·min-1;当升高温度,该反应的平衡常数K_____(填“增大”“减小”或“不变”)。
(2)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)
N2(g)+CO2(g) △H=-34.0kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
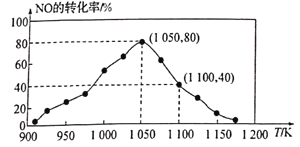
由图可知,1050K前反应中NO的转化率随温度升髙而增大,其原因为__________;在1100K时,CO2的体积分数为_____。
(3)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=___ [已知:气体分压(P分)=气体总压(Pa)×体积分数]。
(4)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)
N2(g)+2CO2(g) △H=-746.8k·mol-1,生成无毒的N2和CO2。实验测得,υ正=k正·c2(NO)·c2(CO),υ逆=k逆·c(N2)c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数___(填“>”“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1 molCO和1 molNO,在一定温度下达到平衡时,CO的转化率为40%,则
=_____。
高三化学填空题中等难度题查看答案及解析
-
中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。请回答下列问题:
(1)氨氮水体污染可用次氯酸除去,已知:
Ⅰ.
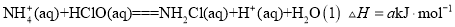
Ⅱ.

Ⅲ.
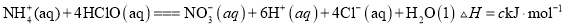
写出水体中
与
反应生成
的热化学方程式:____________________________。
(2)工业上可用排放的
与
合成尿素的方法,达到
减排的目的:
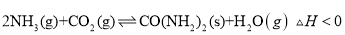 。
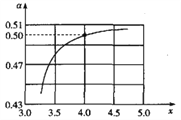
。①一定条件下,在1L的密闭容器中充入1mol
和一定量的
,模拟工业生产得到
的平衡转化率(
)随氨碳比
的变化如图所示,其他条件不变,
随
增大而增大的原因是_______________________________________________;实际工业生产中氨碳比控制在4.0左右,而不是4.5的原因是____________________________________;该温度下反应的平衡常数
______________________________。
②若
,在1L的恒容密闭容器中充入一定量的
和
,此时体系压强为
,5min达到平衡时生成1mol
,此时容器内压强为
,则用
表示该反应的平均速率为______________________________,
的平衡转化率为__________。
(3)采用电解法可使酸性废水中的
转经为
而除去,则阴极的电极反应式为________________________________________。
高三化学综合题中等难度题查看答案及解析
-
中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。请回答下列问题:
科学研究表明,当前应用最广泛的化石燃料到本世纪中叶将枯竭,解决此危机的有效途径之一便是实现燃料和燃烧产物之间的良性循环(如图甲所示):
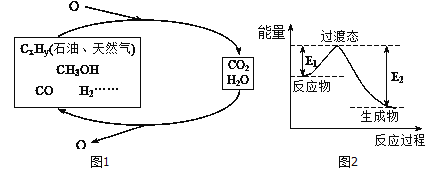
(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2,转化为甲醇蒸汽和水蒸气。图乙是生成1molCH3OH时的能量变化示意图。已知破坏1mol不同共价键的能量(kJ) 分别如下表:
C-H
C-O
C=O
H-H
H-O
413.4
351
745
436
462.8
①结合上表数据,试写出生成CH3OH的热化学反应方程式:____________________。
②已知E2=189.8kJ·mol-1,则E1=_______。
(2)将不同量的CO(g) 和H2O(g) 分别通入到体积为2L的恒容密闭容器中进行如下反应: CO(g)+H2O(g)
CO2(g)+H2(g) 得到如下表所示三组数据:
实验
温度/℃
起始量
达到平衡
CO/mol
H2O/mol
H2/mol
CO转化率
所需时间/min
1
650
4
2
1.6
6
2
900
3
2
3
3
900
①该反应的△H_______0 (填“<”或“>”)。
②实验2条件下的平衡常数K=_______。
③实验3中,若起始时在容器中加入CO、H2O、CO2、H 2各1mol,则此时v正_______v逆 (填“<”“>”或“=”)。
(3)合成甲醇时所需的CO2 可以利用Na2CO3溶液从工业废气(主要含CO2) 中捕捉,其原理如图:
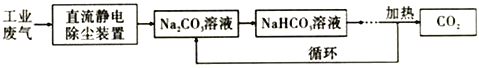
现向100mL 0.1mol/L Na2CO3溶液中通入112mL (已换算为标准状况) CO2,假设溶液中没有晶体析出,试回答下列问题:
①该工业废气处理过程中“静电除尘装置”利用了______________________________的原理。
②用离子方程式解释Na2CO3溶液呈碱性的原因:_____________________。
③反应后所得溶液中的各离子浓度由大到小的顺序是______________________________。
高三化学综合题中等难度题查看答案及解析