-
下列推断正确的是
A. pH=6.5的溶液一定显酸性
B. 0.1mol • L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)=0.1mol • L-1
C. 常温下,等体积的0.2 mol • L-1的盐酸与0.2 mol • L-1的氢氧化钡溶液混合,所得溶液的pH=13
D. 常温下,某溶液中水电离出的c(OH-)=l×10-12 mol • L-1,该溶液pH 一定等于2
高三化学选择题简单题查看答案及解析
-
下列说法正确的是( )
A.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
B.浓度均为0.1mol•L-1的下列溶液,pH由大到小排列顺序为NaOH>Na2CO3>NaHSO4>(NH4)2SO4
C.pH=3的硫酸与醋酸溶液,c()与c(
)之比为1:2
D.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小高三化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.NaHCO3和Na2CO3混合溶液中,一定有
c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO32-)
B.浓度均为0.1 mol·L-1的下列溶液,pH由大到小排列顺序为
NaOH>Na2CO3>NaHSO4>(NH4)2SO4
C.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1∶2
高三化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
B.浓度均为0.1mol·L-1的下列溶液,pH由大到小排列顺序为NaOH>Na2CO3>NaHSO4>(NH4)2SO4
C.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1:2
D.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
高三化学选择题困难题查看答案及解析
-
25℃时,0.1mol Na2CO3与盐酸混合所得溶液的体积为1L,溶液中部分微粒浓度与pH 的关系如图所示。下列有关叙述正确的是
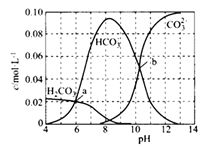
A. 随溶液pH增大,c(CO32-)/c(HCO3-)的值先减小后增大
B. 25℃时,碳酸的第一步电离常数Ka1=10-6
C. pH=4 的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32-)=0.1mol/L
D. b点所示的溶液中:c(Na+)+c(H+)= 2c(CO32-)+c(OH-)+c(Cl-)
高三化学单选题中等难度题查看答案及解析
-
常温条件下,下列各组比值为1∶2的是( )
A. 0.1 mol/L Na2CO3溶液,c(CO32-)与c(Na+)之比
B. 0.1 mol/L与0.2 mol/L 醋酸溶液,c(H+)之比
C. pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比
D. pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比
高三化学单选题中等难度题查看答案及解析
-
常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如下图,则下列说法正确的是( )
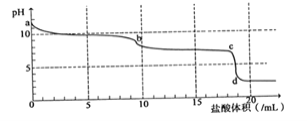
A. a点时溶液pH=11.5,原因是:CO32-+2H2O
H2CO3+2OH-
B. a-b段发生反应为:CO32-+2H+ = CO2↑+H2O
C. b-c段发生反应为:HCO3-+H+ = CO2↑+H2O
D. c-d段发生反应为:H++OH- = H2O
高三化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A. pH=2与pH=1的硝酸中c(H+)之比为1:10
B. Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1
C. 0.2 mol•L-1醋酸与0.1mol/L醋酸中c (H+)之比为2:1
D. NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为2:1
高三化学选择题中等难度题查看答案及解析
-
下列有关实验操作、现象、解释或结论都正确的是
选项
实验操作
现象
解释或结论
A
将Na2CO3溶液由0.1 mol·L-1稀释到0.01 mol·L-1,测溶液pH
溶液pH变小
稀释后CO32-的水解程度减小
B
将NaAlO2与AlCl3溶液混合
出现白色沉淀
AlO2-与Al3+发生相互促进的水解反应
C
将盛有红棕色NO2气体的注射器由10 mL压缩至5 mI
气体颜色比压缩前浅
反应2NO2⇌N2O4向右移动
D
向湿润的有色布条中通入氯气
布条褪色
氯气具有漂白性
A.A B.B C.C D.D
高三化学单选题中等难度题查看答案及解析
-
常温下,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是
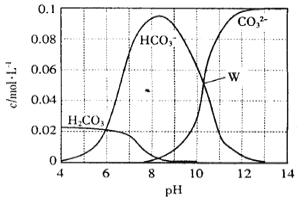
A. W点所示的溶液中:c(Na+)>c(CO32-)= c(HCO3-)>c(OH-)>c(H+)
B. pH=4的溶液中:c(H2CO3)+c(HCO3-)+ c(CO32-)=0.1mol/L
C. pH=8的溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. pH=11的溶液中:c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-)
高三化学单选题困难题查看答案及解析