-
以下关于氟、氯、溴、碘的性质叙述错误的是( )
①HF、HCl、HBr、HI中酸性最强的是HF ②单质F2、Cl2、Br2、I2中,I2沸点最高
③单质F2、Cl2、Br2、I2中,氧化性最强的是F2 ④HF、HCl、HBr、HI还原性最强的是HI
⑤单质F2、Cl2、Br2、I2中,与氢化合最容易的是F2 ⑥HF、HCl、HBr、HI沸点最高的是HI
⑦HF、HCl、HBr、HI稳定性逐渐减弱.
A.只有①
B.②⑤⑦
C.①⑥
D.③④高三化学选择题中等难度题查看答案及解析
-
以下关于氟、氯、溴、碘的性质叙述错误的是
①HF、HCl、HBr、HI中酸性最强的是HF ②单质F2、Cl2、Br2、I2中,I2沸点最高
③单质F2、Cl2、Br2、I2中,氧化性最强的是F2 ④HF、HCl、HBr、HI还原性最强的是HI
⑤单质F2、Cl2、Br2、I2中,与氢化合最容易的是F2 ⑥HF、HCl、HBr、HI沸点最高的是HI
⑦HF、HCl、HBr、HI稳定性逐渐减弱
A.只有① B.②⑤⑦ C.①⑥ D.③④
高三化学选择题简单题查看答案及解析
-
以下关于氟、氯、溴、碘的性质叙述错误的是
①HF、HCl、HBr、HI中酸性最强的是HF
②单质F2、Cl2、Br2、I2中,I2沸点最高
③单质F2、Cl2、Br2、I2中,氧化性最强的是F2
④HF、HCl、HBr、HI还原性最强的是HI
⑤单质F2、Cl2、Br2、I2中,与氢化合最容易的是F2
⑥HF、HCl、HBr、HI沸点最高的是HI
⑦HF、HCl、HBr、HI稳定性逐渐减弱
A.只有① B.②⑤⑦ C.①⑥ D.③④
高三化学选择题中等难度题查看答案及解析
-
关于下列各图的叙述不正确的是( )
化学方程式
平衡常数K
F2 + H2 = 2HF
6.5×1095
Cl2 + H2 = 2HCl
2.6×1033
Br2 + H2 = 2HBr
1.9×1019
I2 + H2 = 2HI
8.7×102
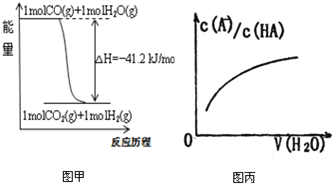
A.已知CO的燃烧热283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.某温度下,pH =11的NH3∙H2O和pH =1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3∙H2O与NH3三种微粒的平衡浓度之和为0.05mol∙L-1
C.在常温下,X2(g) 和 H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
的变化情况
高三化学单选题简单题查看答案及解析
-
关于下列各图的叙述不正确的是( )
化学方程式
平衡常数K
F2 + H2 = 2HF
6.5×1095
Cl2 + H2 = 2HCl
2.6×1033
Br2 + H2 = 2HBr
1.9×1019
I2 + H2 = 2HI
8.7×102
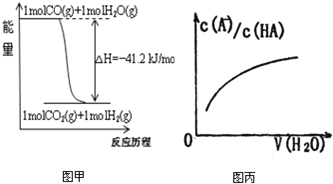
A.已知CO的燃烧热283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.某温度下,pH =11的NH3∙H2O和pH =1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3∙H2O与NH3三种微粒的平衡浓度之和为0.05mol∙L-1
C.在常温下,X2(g) 和 H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
的变化情况
高三化学单选题简单题查看答案及解析
-
下列能说明氯的非金属性强于溴的事实是
A.HClO酸性强于HBrO
B.HBr的分解温度低于HCl
C.Cl2、Br2的熔点的高低
D.BrCl + H2O → HBrO + HCl是非氧化还原反应
高三化学选择题中等难度题查看答案及解析
-
卤族元素的单质能与H2反应
H2+F2=2HF
在暗处能剧烈化合并发生爆炸
H2+Cl2=2HCl
光照或点燃发生反应
H2+Br2=2HBr
加热至一定温度才能反应
H2+I2=2HI
不断加热才能缓慢反应,生成的HI会分解
(1)卤族元素位于周期表中的__________族。
(2)用电子式表示HCl的形成过程__________。
(3)依据上表,可以推测出:随着原子序数的递增,__________(填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式____________。
高三化学填空题简单题查看答案及解析
-
卤族元素的单质能与H2反应
H2+F2=2HF
在暗处能剧烈化合并发生爆炸
H2+Cl2=2HCl
光照或点燃发生反应
H2+Br2=2HBr
加热至一定温度才能反应
H2+I2=2HI
不断加热才能缓慢反应,生成的HI会分解
(1)卤族元素位于周期表中的________族。
(2)用电子式表示HCl的形成过程________。
(3)依据上表,可以推测出:随着原子序数的递增,________(填字母)。
a.单质的熔沸点逐渐升高 b.元素的非金属性逐渐减弱
c.卤化氢的还原性依次减弱 d.卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式________。
高三化学填空题困难题查看答案及解析
-
卤族元素的单质能与H2反应
H2+F2=2HF
在暗处能剧烈化合并发生爆炸
H2+Cl2=2HCl
光照或点燃发生反应
H2+Br2=2HBr
加热至一定温度才能反应
H2+I2=2HI
不断加热才能缓慢反应,生成的HI会分解
(1)卤族元素位于周期表中的______________族。
(2)用电子式表示HCl的形成过程______________。
(3)依据上表,可以推测出:随着原子序数的递增,___________(填字母)。
a. 单质的熔沸点逐渐升高 b. 元素的非金属性逐渐减弱
c. 卤化氢的还原性依次减弱 d. 卤化氢的稳定性依次减弱
(4)不同卤素原子之间可形成卤素互化物,其性质与卤素单质相近。写出BrCl和SO2在水溶液中发生反应的化学方程式___________。
高三化学简答题中等难度题查看答案及解析
-
化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2===2HCl推测:H2+Br2===2HBr。但类比是相对的,如根据2Na2O2+2CO2===2Na2CO3+O2,类推2Na2O2+2SO2===2Na2SO3+O2是错误的,应该是Na2O2+SO2===Na2SO4。下列各组类比中正确的是
A.由溶解性CaCO3<Ca(HCO3)2,推测:Na2CO3<NaHCO3
B.由CO2+Ca(ClO)2+H2O===CaCO3↓+2HClO,推测:SO2+Ca(ClO)2+H2O===CaSO3↓+2HClO
C.由2CO2+Ca(ClO)2+2H2O===Ca(HCO3)2+2HClO,推测:CO2+NaClO+H2O===NaHCO3+HClO
D.由Na2SO3+2HCl===2NaCl+H2O+SO2↑,推测:Na2SO3+2HNO3===2NaNO3+H2O+SO2↑
高三化学选择题中等难度题查看答案及解析