-
常温下 0.1mol/L的H2A溶液中H2A、HA—、A2— 三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是( )
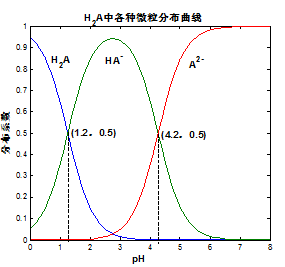
A.H2A 2H+ + A2— K=10—5.4
2H+ + A2— K=10—5.4
B.在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.已知25℃时HF的Ka=10-3.45,将少量H2A的溶液加入足量NaF溶液中,发生的反应为:H2A+F﹣═ HF+HA﹣
D.将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2
-
常温下 0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是( )
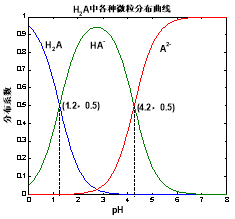
A.H2A 2H+ + A2- K=10-5.4
2H+ + A2- K=10-5.4
B.在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.已知25℃时HF的 Ka=10-3.45,将少量H2A的溶液加入足量NaF溶液中,发生的反应为: H2A+F-═ HF+HA-
D.将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2
-
常温下0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物质的量分数随pH变化的关系如图所示.下列表述正确的是( )

A. 在含H2A、HA-、A2-的溶液中,通入少量HCl,HA-的物质的量分数一定变大
B. 将等物质的量的NaHA、Na2A溶于水中,所得溶液中存在:c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-)
C. 在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D. 将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2
-
常温下,0.1 mol·L−1 H2R溶液中H2R、HR−、R2−三者中所占物质的量分数(分布系数δ)随pH变化的关系如图所示。下列表述正确的是
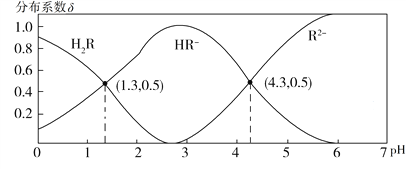
A. Na2R溶液中:c(Na+)=c(HR−)+2c(R2−)
B. H2R H++HR−,Ka1=1.0×10−1.3
H++HR−,Ka1=1.0×10−1.3
C. 等物质的量的NaHR和Na2R溶于水,使得溶液pH恰好为4.3
D. HF的Ka=1.0×10−3.4,在足量NaF溶液中加入少量H2R,发生反应:H2R+2F− 2HF+R2−
2HF+R2−
-
常温下,0.1 mol·L−1 H2R溶液中H2R、HR−、R2−三者中所占物质的量分数(分布系数δ)随pH变化的关系如图所示。下列表述正确的是
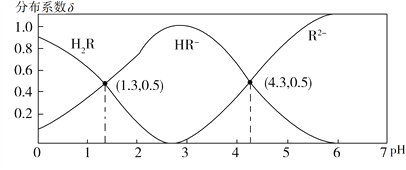
A. Na2R溶液中:c(Na+)=c(HR−)+2c(R2−)
B. H2R H++HR−,Ka1=1.0×10−1.3
H++HR−,Ka1=1.0×10−1.3
C. 等物质的量的NaHR和Na2R溶于水,使得溶液pH恰好为4.3
D. HF的Ka=1.0×10−3.4,在足量NaF溶液中加入少量H2R,发生反应:H2R+2F− 2HF+R2−
2HF+R2−
-
某化学小组设计了如图1所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图2所示,则下列说法中不正确的是
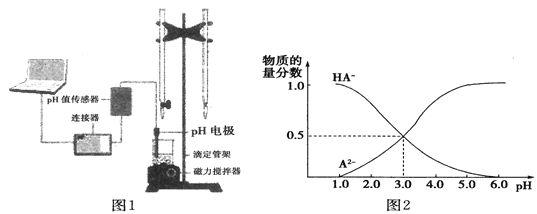
A.pH=4.0时,图中n(HA-)约为0.0091mol
B.该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂
C.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
D.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
-
某化学小组设计了如图1所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图2所示,则下列说法中不正确的是
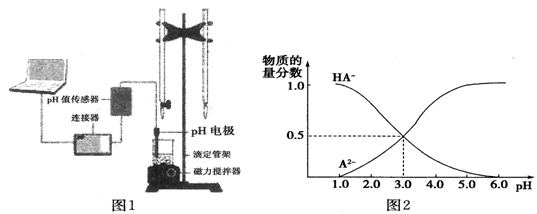
A. pH=4.0时,图中n(HA-)约为0.0091mol
B. 该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂
C. 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
D. 0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
-
某化学小组设计了如图所示的数字化实验装置,研究常温下,向1L0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是( )
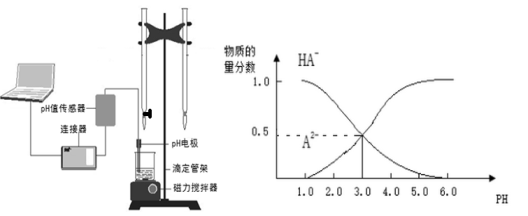
A.pH=4.0时,图中n(HA-)约为0.0091mol
B.该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂
C.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
D.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
-
某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的 物质的量分数与溶液pH的关系如图乙所示,(已知HA=H++HA- HA-  H++A2-)则下列说法中正确的是( )
H++A2-)则下列说法中正确的是( )
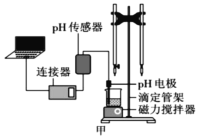
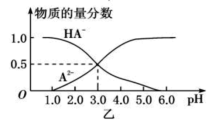
A.pH=3.0时,可以计算出Ka2= 10 -3
B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
C.该实验左边的滴定管为碱式滴定管,用来盛装NaOH溶液,烧杯中并加酚酞作指示剂
D.常温下,将等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
-
某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L 0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的 物质的量分数与溶液pH的关系如图乙所示,(已知HA=H++HA- HA-  H++A2-)则下列说法中正确的是( )
H++A2-)则下列说法中正确的是( )
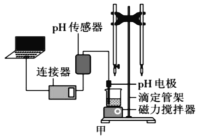
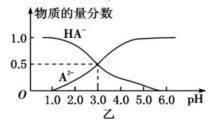
A.pH=3.0时,可以计算出Ka2= 10 -3
B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
C.该实验左边的滴定管为碱式滴定管,用来盛装NaOH溶液,烧杯中并加酚酞作指示剂
D.常温下,将等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0

2H+ + A2— K=10—5.4










