-
下列说法正确的是
A. 元素的电负性越大,其单质越稳定
B. 分子晶体中可能不存在共价键
C. 晶格能越大,形成的离子晶体越稳定
D. 金属晶体和离子晶体均具有延展性
-
Ⅰ.下列说法正确的是__________。
A.元素的电负性越大,其单质越稳定
B.分子晶体中可能不存在共价键
C.晶格能越大,形成的离子晶体越稳定
D.金属晶体和离子晶体均具有延展性
Ⅱ.钢铁中含有C、N、Mn等元素,实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O  2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
(1)Mn原子的价层电子的轨道表达式(电子排布图)为____________________。
(2)已知H2S2O8的结构简式如图所示。
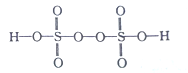
①H2S2O8中S的轨道杂化方式为______________,H、O、S三种元素中,电负性最大的元素是___________(填元素符号)。
②S基态原子中电子的运动状态有_________种。
③上述反应中S2O82-断裂的共价键类型为___________(填“σ键”或“π键”) ,每生成1mol MnO4-,断裂的共价键数目为___________NA。

(3)C和N能形成多种结构的晶体。一种新型的超硬材料类似于金刚石的结构,但硬度比金刚石大,其晶胞如图所示(图示原子都包含在晶胞内),其化学式为______________。已知晶胞参数a=0.64nm,b=0.55nm,c=0.24nm,则该晶体的密度为_______________(列出式子即可,但式子中不包含字母)g/cm3。
-
下列说法正确的是
A.原子晶体中一定含有共价键;离子晶体中一定含有离子键,可能含有共价键;分子晶体中一定存在分子间作用力和共价键
B.晶格能是指离子形成1mol离子晶体释放的能量,通常取正值
C.含有阴离子的晶体中一定有阳离子,含有阳离子的晶体中不一定含有阴离子
D.元素的第一电离能 是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的
是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的 逐渐增大
逐渐增大
-
下列说法不正确的是( )
A.HF的热稳定性很好,是因为HF分子间存在氢键
B.构成单质的分子内不一定存在共价键
C.由非金属元素组成的化合物不一定是共价化合物
D.NaCl晶体熔化,需要破坏离子键
-
下列说法正确的是( )
A.两种元素形成的离子晶体中不可能存在共价键
B.氢键影响物质的物理性质,也决定其稳定性
C.石墨比金刚石稳定的原因是石墨晶体中存在分子间作用力
D.NaCl晶体中,每个Cl-周围同时吸引6个Na+
-
下列说法正确的是
A.分子内共价键越强,分子越稳定,其熔沸点也越高
B.C、H、O、N四种元素组成的化合物一定是离子化合物
C.HF分子间存在着氢键,所以HF比HCl稳定
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
-
下列说法正确的是( )
A.第一电离能越小的元素其单质金属活泼性一定越大
B.电负性越小的元素金属性一定越强
C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键
D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低
-
下列说法正确的是( )
A.第一电离能越小的元素其单质金属活泼性一定越大
B.电负性越小的元素金属性一定越强
C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键
D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低
-
下列说法正确的是( )
A.分子内共价键越强,分子越稳定,其熔沸点也越高
B.C、H、O、N四种元素组成的化合物一定是离子化合物
C.HF分子间存在着氢键,所以HF比HCl稳定
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
-
Ⅰ.下列有关说法正确的是________。
A.相同类型的离子晶体,晶格能越大,形成的晶体越稳定
B.手性催化剂只催化或者主要催化一种手性分子的合成
C.用金属的电子气理论能合理地解释金属易腐蚀的原因
D.H3O+、NH4Cl和[Ag(NH3)2]+中均存在配位键
Ⅱ.碳及其化合物在自然界中广泛存在。
(1)基态碳原子的价电子排布图可表示为________。
(2)第一电离能:碳原子________(填“>”“<”或“=”)氧原子,原因是__________________________。
(3)冰晶胞中水分子的空间排列方式与金刚石晶胞类似。每个冰晶胞平均占有________个水分子,冰晶胞与金刚石晶胞排列方式相同的原因是__________________________。
(4)C60的晶体中,分子为面心立方堆积,已知晶胞中C60分子间的最短距离为d cm,可计算C60晶体的密度为________g/cm3。
(5)请写出一个反应方程式以表达出反应前碳原子的杂化方式为sp2,反应后变为sp3:________________________________。
2MnO4-+10SO42-+16H+

