-
前四周期元素X、Y、Z、M、E的原子序数依次增大,其中元素X的基态原子有3个不同的能级,且3个能级中的电子数均相等。元素Y的核外p电子总数比s电子总数少1。元素Z的核外s电子总数与p电子总数相等,且与Y元素在同一周期。元素M的主族序数与周期数的差为4。元素E位于周期表的第10列。
(1)元素X、Y、Z的第一电离能由小到大的顺序为_____________(用元素符号表示)。
(2)常温下,配合物Fe(XZ)5为黄色液体,易溶于非极性溶剂,熔点为215K,沸点为376K。据此推断Fe(XZ)5 晶体属于_____________晶体。配合物Fe(XZ)5的中心原子的基态核外电子排布式为_____________。
(3)XZM2分子中所有原子最外电子层均形成8电子稳定结构,XZM2分子中σ键和π键的个数比为_____________,中心原子的杂化方式为_____________。
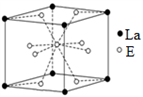
(4)E和La的合金是目前使用广泛的储氢材料,在我国已实现了产业化。该合金的晶胞结构如图所示,则该晶体的化学式为_____________(用元素符号表示)。
-
A、B、C、D、E、F六种元素为前四周期元素,原子序数依次增大。A的最高正价和最低负价的绝对值相等,B的基态原子的电子分布在3个不同的能级且各能级中电子数相等。D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子在同周期元素中未成对电子数最多。请回答下列问题:
(1)F元素在周期表中的位置 ;F元素价电子排布式为 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为 。(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是 。
A.分子中都含有σ键和π键
B.都是含极性键和非极性键的直线型分子
C.B2A2的沸点明显低于A2D2
D.都具有还原性
(4) 由 A、C 两种元素可以形成一种 CA5的既含离子键又含共价键的化合物,其电子式为 ;
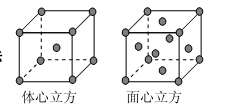
(5) 金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞中实际 含有的Fe原子个数之比为 。
-
(13分)有A、B、C、D、E、F、G、H八种原子序数依次增大的元素(原子序数均小于30)。A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,A、E同主族,F的基态原子s能级的电子总数与p能级的电子数相等,B、G同族,H的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)H元素在周期表中属于 区。G的基态原子电子排布式为 CD2中C的杂化类型是___________
(2)下列说法不正确的是 。
a.B2A2分子中含有σ键和π键
b.B2A2分子的沸点明显低于A2D2分子
c.A2D2分子的空间构型为直线形
d.B、C、D的电负性由大到小的顺序为D>C>B
e.B、C、D的第一电离能由大到小的顺序为D>C>B
f.H2+能与BD分子形成[H(BD)4]2+,其原因是BD分子中含有空轨道
g.B和G的单质能形成相同类型的晶体,其熔点B > G
(3)由B、F、H三种元素形成的一种具有超导性的晶体,B位于F和H原子紧密堆积所形成的空隙当中。晶胞如图所示,该晶体的化学式为___________

(4)CD2、D2和熔融ECD3可制作燃料电池,其原理如下图所示。该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,石墨Ⅰ电极反应式为___________

-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1) 原子基态时外围电子轨道表示式为______;
原子基态时外围电子轨道表示式为______;
(2)由A、B、C形成的离子 与
与 互为等电子体,则
互为等电子体,则 的结构式为______;
的结构式为______;
(3)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”
键” 或大
或大 键
键 。大
。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的电子数和原子个数,如苯分子中大
键的电子数和原子个数,如苯分子中大 键表示为
键表示为
①下列微粒中存在“离域 键”的是______;
键”的是______;


② 分子中大
分子中大 键可以表示为______;
键可以表示为______;
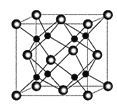
(4) 和D能够形成化合物X,其晶胞结构如图所示,晶胞参数
和D能够形成化合物X,其晶胞结构如图所示,晶胞参数 ,晶胞中C原子的配位数为______;列式计算晶体X的密度______
,晶胞中C原子的配位数为______;列式计算晶体X的密度______ 。
。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1)F原子基态的外围核外电子排布式为______________________________;
(2)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为_______________;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为_______________;
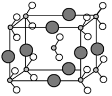
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为_________;
(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2=CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物。
①下列说法正确的是__________________;
A.N2O为直线型分子
B.C、N、O的第一电离能依次增大
C.CH2=CH一CHO分子中碳原子均采用sp2杂化
D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H20)5]S04,该配合物中心离子的配体为_____________,其中提供空轨道的是__________________(填微粒符号)。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F原子基态的核外电子排布式为________。
(2)在A、B、C三种元素中,第一电离能由大到小的顺序是________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是________。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为________。
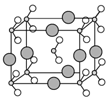
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同:D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为25。
(1)F基态原子的核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由小到大顺序是(用元素符号答) 。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB- 的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的类型为 。
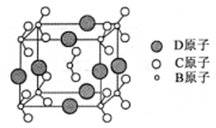
(6)由B、C、D三种元素形成的化合物晶体的晶胞如右图所示,则该化合物的化学式为 。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F原子基态的外围核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是 (用元素符号回答)。
(3)元素B的简单气态氢化物的沸点 (高于,低于)元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。
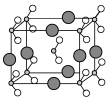
(7)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因 。
-
原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同:D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为25。
(1)F基态原子的核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是(用元素符号回答) 。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB- 的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
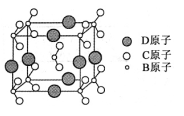
(6)由B、C、D三种元素形成的化合物晶体的晶胞如右图所示,则该化合物的化学式为 。
-
原子序数依次增大的A、B、C、D、E五种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为短周期中原子半径最大的主族元素;E的原子序数为22。
(1)①E被称为“国防金属”和“生物金属”,是重要的结构材料。E原子基态的外围核外电子排布式为 ;
②金红石(EO2)的熔点1825℃,用熔盐法直接电解金红石可获得金属E,金红石所属的晶体类型是 晶体;
③ECl4能与NH4Cl反应生成配合物(NH4)2[ECl6]。此配合物中,形成配位键时提供孤对电子的有 (填元素符号)。与NH4+互为等电子体的一种阴离子为 (填化学式),其中心原子杂化类型为 杂化。
(2)在A、B、C三种元素中,电负性由小到大的顺序是 (用元素符号回答)。
(3)元素A的简单气态氢化物的沸点 (“高于”,“低于”)元素B的简单气态氢化物的沸点,其主要原因是 。
(4)由B形成的离子B3-与AC2互为等电子体,则B3-的
分子构型为 。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。











