-
某体系中存在如下反应:①H2S+4H2O-8e = SO42-+10H+,②2IO3-+12 H++10e = I2+6H2O。
(1)反应①中H2S做_____剂,反应②属于_______ 反应(填“氧化”或“还原”)。
(2)若在反应①中失去0.2 mol 电子,则反应②中可生成______g I2。
(3)写出并配平碘酸钾与硫化氢反应的化学方程式,同时标出电子转移的方向和数目:_____。
(4)由上述反应可推知__________。
a.氧化性:K2SO4> KIO3 b.酸性:HIO3> H2SO4
c.还原性:H2S > I2 d.反应过程中溶液的酸性逐渐减弱
高三化学综合题困难题查看答案及解析
-
某体系中存在如下反应:
①H2S+4H2O-8e → SO42-+10H+
②2IO3-+12 H++10e → I2+6H2O
(1)反应①中H2S做__________剂,反应②属于___________ 反应(填“氧化”或“还原”)。
(2)若在反应①中失去0.2 mol 电子,则反应②中可生成________ g I2。
(3)写出并配平碘酸钾与硫化氢反应的化学方程式,同时标出电子转移的方向和数目:
_______________________________________________________________________。
(4)由上述反应可推知________。
a.氧化性:K2SO4 > KIO3 b.酸性:HIO3 > H2SO4
c.还原性:H2S > I2 d.反应过程中溶液的酸性逐渐减弱
高三化学填空题困难题查看答案及解析
-
在5H2S + 8KIO3 = 4K2SO4 + 4I2 + H2SO4 + 4H2O的反应中 ,下列说法错误的是
A.H2S是还原剂 B还原性:H2S>I2
C.KIO3 被还原 D.转移40mole-
高三化学选择题中等难度题查看答案及解析
-
生物脱H2S的原理为:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4FeSO4+O2+2H2SO4
2Fe2(SO4)3+2H2O
硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,氧化速率随温度和pH变化如下图。下列说法正确的是
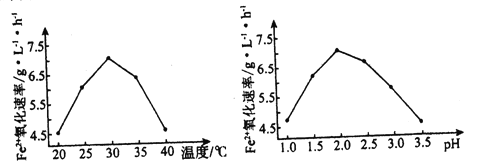
A. 该过程最终将H2S转化为Fe2(SO4)3
B. H+是反应2的反应物,c(H+)越大反应速率越快
C. 反应1消耗11.2LH2S,转移的电子数目约为6.0×1023个
D. 反应温度过高,Fe2+氧化速率下降,其原因可能是硫感菌失去活性
高三化学单选题简单题查看答案及解析
-
生物法(加入脱硫细菌)净化含硫废气时发生如下反应:CH3COOH +SO42-=2HCO3-+H2S。下列有关说法正确的是
A. CH3COOH是氧化剂 B. SO42-被氧化
C. H2S的酸性弱于H2CO3 D. 该反应属于复分解反应
高三化学选择题中等难度题查看答案及解析
-
某体系中存在如下反应:
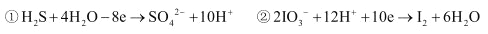
(1)反应①中 H2S 做___________剂,反应②属于___________反应(填“氧化”或“还原”)。
(2)若在反应①中失去 0.2mol 电子,则反应②中可生成___________g 碘。
(3)由上述反应可推知___________。
a.氧化性K2SO4 KIO3 b.酸性: HIO3 H2SO4
c. 还原性 H2S I2 d. 反应过程中溶液的酸性逐渐减弱
高三化学填空题中等难度题查看答案及解析
-
某体系中存在如下反应:
①
②
(1)反应①中H2S作_______剂,反应②属于_______反应。(填“氧化”或“还原”)
(2)若在反应①中失去0.2 mol电子,则反应②中可生成_______g碘。
(3)写出并配平碘酸钾与硫化氢反应的化学方程式,同时标出电子转移的方向和数目:______。
(4)由上述反应可推知_______。
a.氧化性:K2SO4>KIO3 b.酸性:HIO3>H2SO4
c.还原性:H2S>I2 d.反应过程中溶液的酸性逐渐减弱
高三化学填空题中等难度题查看答案及解析
-
常温下,某反应体系中存在六种粒子:ClO4-、SO42-、ClO3-、S2O82-、H+、H2O。在反应过程中,溶液的 pH 与反应进程的关系如图所示。下列说法正确的是
A. ClO4-是氧化剂
B. SO42-是氧化产物
C. 氧化性:S2O82->ClO3-
D. 生成 1 mol 还原产物时转移 2 mol 电子
高三化学单选题中等难度题查看答案及解析
-
某兴趣小组探究以芒硝Na2SO4·10H2O和CaO为原料制备Na2CO3。
(1)将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3。三元体系中反应的离子方程式为: SO42-+ Ca(OH)2(s)+2H2O
CaSO4·2H2O(s)+2 OH-
该反应的平衡常数表达式K=_________________________。
往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3 [即c(OH-)=0.02mol/L],可使反应在常温下容易进行。反应后过滤,再向滤液中通入CO2,进一步处理得到Na2CO3。
(2)在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是_______________________________________________________________。
(3)添加的酸性物质须满足的条件(写出两点)是_____________、______________。
(4)用平衡移动原理解释添加酸性物质的理由:____________________________________;以HA表示所添加的物质,则总反应的离子方程式可写为_______________________。
(5)Na2CO3溶液中存在水解平衡:CO32-+H2O
HCO3-+OH-。下列说法错误的是_________。
a.加水稀释,溶液中所有离子的浓度都减小
b.通入CO2,溶液pH减小
c.加入NaOH固体,
减小
d.稀释溶液,平衡常数增大
高三化学填空题困难题查看答案及解析
-
某兴趣小组探究以芒硝Na2SO4·10H2O和CaO为原料制备Na2CO3。
(1)将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3。三元体系中反应的离子方程式为: SO42-+ Ca(OH)2(s)+2H2O
CaSO4·2H2O(s)+2 OH-
该反应的平衡常数表达式K=_________________________。
往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3 [即c(OH-)=0.02mol/L],可使反应在常温下容易进行。反应后过滤,再向滤液中通入CO2,进一步处理得到Na2CO3。
(2)在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是_______________________________________________________________。
(3)添加的酸性物质须满足的条件(写出两点)是_____________、______________。
(4)用平衡移动原理解释添加酸性物质的理由:____________________________________;以HA表示所添加的物质,则总反应的离子方程式可写为_______________________。
(5)Na2CO3溶液中存在水解平衡:CO32-+H2O
HCO3-+OH-。下列说法错误的是_________。
a.加水稀释,溶液中所有离子的浓度都减小
b.通入CO2,溶液pH减小
c.加入NaOH固体,
减小
d.稀释溶液,平衡常数增大
高三化学填空题困难题查看答案及解析