-
碳酸钾与碳酸氢钾都是重要的化学试剂与工业原料,具有广泛的用途.
(1)将碳酸钾、石灰石和二氧化硅进行高温煅烧,可得到组成为K2O•CaO•6SiO2的钾玻璃,同时排出CO2.若制造5.1kg钾玻璃,排放的CO2在标准状况下的体积是_____L.
(2)已知亚硫酸的酸性强于碳酸.工业上用碳酸钾与碳酸氢钾的混合溶液吸收SO2,充分反应后,所得溶液组成如下表:
物质
K2CO3
KHCO3
K2SO3
质量(kg)
55.2
120.0
63.2
计算原吸收液中碳酸钾与碳酸氢钾的物质的量之比_______________.
(3)根据上表中的数据,计算上表的混合溶液还能吸收SO2的最大质量(不计SO2的溶解)._____________
(4)将热的浓CuSO4溶液与K2CO3溶液混合,析出物中有一种蓝色粒状晶体(不含结晶水),式量为376,其中钾元素的质量分数为0.104.取0.02mol该晶体溶于足量的稀盐酸中,没有气体产生,再加入BaCl2,产生9.32g白色沉淀,通过计算推断晶体的化学式.___
高三化学计算题困难题查看答案及解析
-
碳酸钡是一种重要的无机盐产品,广泛应用于工业陶瓷、光学玻璃、建筑等行业。
生产制备:工业上一般以重晶石
为原料,采用高温煅烧还原法;实验室一般以重晶石
为原料,采用沉淀转化法。
高温煅烧还原法:

煅烧还原的化学方程式为:_____________。
为了提高浸取速率,可采取的措施是__________
任写一种
。
经检验BaS的水溶液呈碱性,原因是
用离子方程式表示
__________。
沉淀转化法:向
沉淀中加入饱和
溶液,充分搅拌,弃去上层清液。如此处理多次,直到
全部转化为
:
平衡常数
现有
,每次用
饱和
溶液处理,假定
能全部转化,至少需要处理_____________次。
从“绿色化学”角度分析,用饱和
溶液沉淀转化法的优点是:__________。
分离提纯
某实验室分离提纯混有少量碳酸钙杂质的碳酸钡样品的步骤如下:
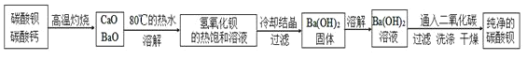
将灼烧后的固体混合物置于
的热水中,制成氢氧化钡的热饱和溶液。为减少
的损失并除去不溶物应进行的操作是_____。
向制得的
溶液中滴加_______
填一种试剂名称
,再通入二氧化碳。当观察到_______时,即可停止通二氧化碳。
环境监测
环境监测某工厂废水中
的浓度。取废水
,控制适当的酸度加入足量的
溶液,得
沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时
全部转化为
,再加入过量KI溶液,反应液中再滴加
溶液,反应完全时,消耗
溶液
。已知有关的离子方程式为:
;
。
该工厂废水中
的物质的量浓度__________
高三化学工业流程困难题查看答案及解析
-
纯碱和硫酸都是重要的化工原料,用途非常广泛。
(1)利用氨碱法得到的碳酸氢钠经煅烧生成纯碱。工艺流程如下图所示:
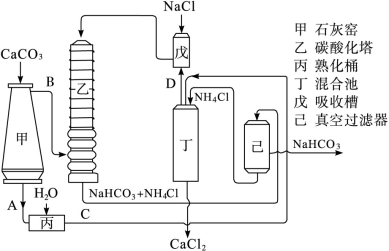
氨碱法示意图
图中的中间产物C是_________,D是________(写化学式);装置乙中发生反应的化学方程式为_________________________________。
(2)火山喷发所产生的硫磺可用于生产重要的化工原料硫酸。甲企业用接触法生产硫酸采用的主要原料是硫磺和空气。工艺流程如下图所示:
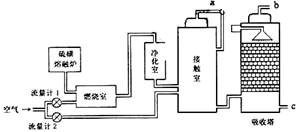
为了充分利用反应放出的热量,接触室中应安装____________(填设备名称)。吸收塔中填充许多瓷管,其作用是____________。为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2的转化率,经流量计2的氧气量为接触室中SO2完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为____________。
高三化学计算题中等难度题查看答案及解析
-
碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:
饱和
.
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③
盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
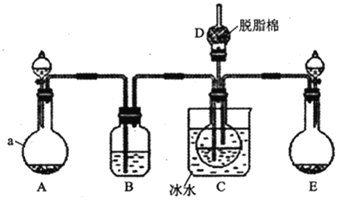
请回答下列问题
(1)仪器a的名称是______.
(2)
中应选用的药品是______
填序号
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)
中脱脂棉应浸润的试剂是______
填写字母编号
浓硫酸
稀硫酸
氢氧化钠溶液
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度
假设晶体中不含碳酸盐杂质
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

操作Ⅲ中的方法是______,______,______
所得晶体中碳酸氢钠的纯度是______
不必化简
高三化学实验题中等难度题查看答案及解析
-
碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:
饱和
.
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去.
可选用的药品有:①石灰石②生石灰③
盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
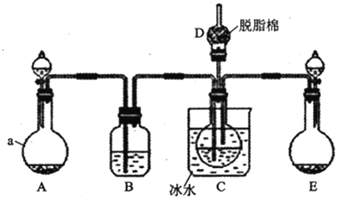
请回答下列问题
(1)仪器a的名称是______.
(2)
中应选用的药品是______
填序号
(3)在实验过程中,应先向C中通入的气体的化学式是______,其原因是______.
(4)
中脱脂棉应浸润的试剂是______
填写字母编号
浓硫酸
稀硫酸
氢氧化钠溶液
浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度
假设晶体中不含碳酸盐杂质
,先将晶体充分干燥后,称量质量为wg,称量质量为wg,然后进行如下图所示实验:

操作Ⅲ中的方法是______,______,______
所得晶体中碳酸氢钠的纯度是______
不必化简
高三化学实验题中等难度题查看答案及解析
-
碳酸氢钠是一种重要的化工原料,在日常生活中也有广泛的用途,侯德榜先生发明了连续生产纯碱与氯化铵的联合制碱工艺,成为近代化学工业的奠基人之一,该反应原理为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl △H<0。
现用如图所示装置和上述原理制取碳酸氢钠晶体,图中夹持装置已略去。
可选用的药品有:①石灰石②生石灰③6mol/L盐酸④稀硫酸⑤浓氨水⑥饱和氯化钠溶液⑦饱和碳酸氢钠溶液
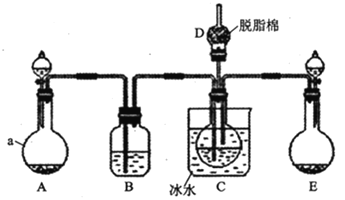
请回答下列问题:
(1)仪器a的名称是___。
(2)B中应选用的药品是___(填序号)
(3)在实验过程中,应先向C中通入的气体的化学式是___,其原因是___。
(4)D中脱脂棉应浸润的试剂是___(填写字母编号)。
a.浓硫酸 b.稀硫酸 c.氢氧化钠溶液 d.浓硝酸
(5)该小组同学为了测定C中所得晶体中碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),先将晶体充分干燥后,称量质量为wg,然后进行如图所示实验:

①操作Ⅲ中的方法是___,___,___。
②所得晶体中碳酸氢钠的纯度是___(不必化简)。
高三化学实验题中等难度题查看答案及解析
-
钠及其化合物具有广泛的用途。
(1)工业上制备碳酸氢钠的化学方程式为____________。
(2)用Na2CO3熔融作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示,正极的电极反应式为__________。
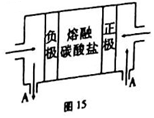
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质
CH3COONa
Na2CO3
NaClO
NaCN
pH
8.8
11.6
10.3
11.1
上述盐溶液的阴离子中,结合H+能力最强的是_______,根据表中数据,浓度均为0.01 mol·L-1下列四种酸的溶液分别稀释100倍,pH变化最大的是_______(填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当100 mL 2mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH<7,则溶液中各离子浓度由大到小的顺序为_______。
②常温下,已知Ksp[Cu(OH)2]=2×10-20, Ksp[CuS]=1.3×10-36。向浓度为0.1mol/L,体积为10mL的氢氧化钠溶液中,逐滴加入浓度为0.1mol/L 硫酸铜溶液至pH=6时Cu2+的浓度为______。向该溶液中滴入一滴0.1mol/L的硫化钠溶液,_______(填“有”或“没有”)CuS沉淀析出。(一滴约为0.05mL)
高三化学简答题困难题查看答案及解析
-
铁及其化合物在生产、生活中具有广泛的用途。请回答下列问题:
(1)氰化物极毒,
可以消除含氰废液中的
,其中
的电子式为________。
(2)碳酸亚铁
是一种重要的工业盐,外观为白色固体,潮湿空气中易被氧化。用硫铁矿烧渣
主要含
、
、少量
制备
的工艺流程如下:
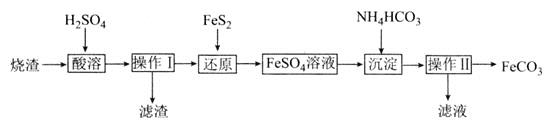
“还原”时,发生反应的离子方程式为________。
的溶解度曲线如图所示,欲获得
,采用的实验操作是________。
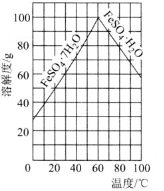
在空气中煅烧可制备铁红,反应的化学方程式为________。
“沉淀”步骤中
达到沉淀溶解平衡时,若
,欲使所得的
中不含有
,应调节溶液的pH不超过________
已知:
,
,
。
(3)铁
镍电池结构、强度极好,循环寿命和工作寿命长。电池总反应为
。写出放电时的负极反应式:________。
(4)化合物
为
价
为亮绿色晶体,可用于晒制蓝图。其组成测定实验如下:
步骤Ⅰ:称取0.491g
置于锥形瓶中,加足量蒸馏水和稀
;
步骤Ⅱ:用
溶液进行滴定,恰好反应时消耗
溶液
;
步骤Ⅲ:再加入适当的还原剂,将
完全转化为
,用
溶液继续滴定,当
完全氧化时,消耗溶液
溶液2.00mL。
步骤Ⅰ中加足量稀
的目的是________。
该化合物的化学式为________。
高三化学综合题困难题查看答案及解析
-
[化学—选修2:化学与技术] 工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为: ;
②硫酸钠和焦炭、石灰石反应的化学方程式为: (已知硫酸钠做氧化剂,生成物中气体只有一种)。
(2)氨碱法的工艺如图所示,得到的碳酸氢钠经煅烧生成纯碱。

①图中的中间产物C是_______,(填化学式,下同)D是_______;
②装置乙中发生反应的化学方程式为 。
(3)联合制碱法是对氨碱法的改进,其优点是除了副产物氯化铵可用作化肥外还有______________。
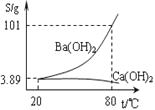
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?__________。
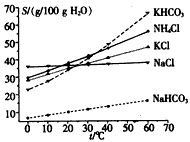
高三化学实验题中等难度题查看答案及解析
-
工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为 _;
②硫酸钠和焦炭、石灰石反应的化学方程式为_ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
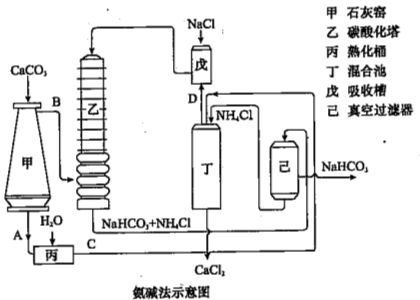
①图中的中间产物C是_______,D_______。(写化学式);
②装置乙中发生反应的化学方程式为 ;
(3)联合制碱法对氨碱法的改进,其优点是 ;
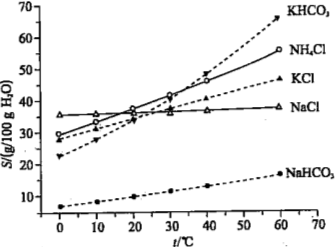
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?
高三化学填空题困难题查看答案及解析