-
铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是 用化学用语及相关文字说明表达式为______
用化学用语及相关文字说明表达式为______
(2)下列实验能比较镁和铝的金属性强弱的是______ 填字母序号
填字母序号
 测定镁和铝的导电性强弱
测定镁和铝的导电性强弱
 测定等物质的量浓度的
测定等物质的量浓度的 和
和 溶液的pH
溶液的pH
 向
向 和
和
 中加过量NaOH溶液
中加过量NaOH溶液
(3)冶炼金属铝时,用石墨做电极电解熔融______ 填化学式
填化学式 ,液态铝在______
,液态铝在______ 填“阴”或“阳”
填“阴”或“阳” 极得到
极得到
(4) 与
与 在高温下反应可制得高温结构陶瓷氮化铝
在高温下反应可制得高温结构陶瓷氮化铝 ,且生成
,且生成 。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为______
。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为______
(5)聚合铝 是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铝灰、铝土矿、铝渣等为原料
是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铝灰、铝土矿、铝渣等为原料 主要成分为Al、
主要成分为Al、 可制取聚合铝.实验步骤如下:
可制取聚合铝.实验步骤如下:
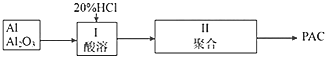
①写出酸溶过程中发生的非氧化还原反应的离子方程式:______
②聚合铝 的分子式为
的分子式为 ,聚合铝中
,聚合铝中 与
与 的比值对净水效果有很大影响,定义盐基度
的比值对净水效果有很大影响,定义盐基度 :
: ,当
,当 时,
时, ______
______ 填入合适数字
填入合适数字
③制取聚合铝的方法有多种,若将步骤I后的溶液pH直接调制 时,将在过程④发生聚合而得到某种聚合铝
时,将在过程④发生聚合而得到某种聚合铝 ,写出生成该聚合铝的离子反应方程式是______
,写出生成该聚合铝的离子反应方程式是______
-
铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___________
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝-空气电池以其环保、安全而受到越来越多的关注,其原理如下图所示。

该电池的正极反应方程式为 _____;电池中NaCl溶液的作用是 ______;以该电池为电源,用惰性电极电解Na2SO4溶液,当Al电极质量减少1.8g时,电解池阴极生成的气体在标准状况下的体积为_______L。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为___________
(4)同主族的元素应用广泛。2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
①基态Ga原子价电子排布式____,核外电子占据最高能级的电子云形状为____;基态As原子最高能层上有____个电子。
②镓失去电子的逐级电离能(单位:kJ/mol)的数值依次为577、1985、2962、6192,-1由此可推知镓的主要化合价为_____和+3,砷的第一电离能比镓_____填“大”或“小”)。
③第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为____。
④砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中C原子的杂化方式为 ______,AsH3分子的空间构型为______。
⑤相同压强下,AsH3的沸点_______NH3(填“大于”或“小于”),原因为________。
-
铝是最重要的金属之一,铝及其化合物在生活中有广泛的用途。
(1)纳米铝粉可以作高效催化剂、导电膜层、高档金属颜料等。普通铝在空气中能稳定存在,而纳米铝粉在空气中能自燃,从影响反应速率的角度分析其原因是________。
(2)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①该反应的化学方程式为_________________。
②MnO2加入酸化后的H2O2溶液中,MnO2溶解,同时产生无色无味的气体。该反应的离子方程式是_____________,该反应中还原剂是___________。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O将产生的气体通过下图所示装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O将产生的气体通过下图所示装置。
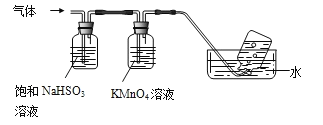
①集气瓶中收集到的气体是_________(填化学式)。
②B中酸性KMnO4溶液褪色(MnO4—还原为Mn2+),发生反应的离子方程式为__________。
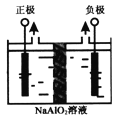
(4)Al(OH)3是重要化工原料。电解法制备高品质Al(OH)3的装置如图(中间用离子交换膜隔开),电解总反应方程式为4NaAlO2+10H2O 4Al(OH)3↓+4NaOH+O2↑+2H2↑,阳极的电极反应式为____________。
4Al(OH)3↓+4NaOH+O2↑+2H2↑,阳极的电极反应式为____________。
-
铝(熔点660℃)是一种应用广泛的金属,工业上用 (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石( )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,其原因是__________,冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,请写出铝与V2O5在高温下反应的化学方程式:___________。
(2)将 液和
液和 溶液混合制取
溶液混合制取 。该实验用于盛装NaF溶液的试剂瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
。该实验用于盛装NaF溶液的试剂瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
(3)下列关于铝元素的叙述不正确的是__________(填序号)。
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________,水源中的
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________,水源中的 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,此时铝主要以
还原为N2,此时铝主要以 的形式存在于溶液中,请写出该反应的离子方程式:__________,当该反应转移5mol电子时,产生的
的形式存在于溶液中,请写出该反应的离子方程式:__________,当该反应转移5mol电子时,产生的 在标况下的体积约为_______L。
在标况下的体积约为_______L。
-
铝(熔点660℃)是一种应用广泛的金属,工业上用A12O3(熔点2045℃)和冰晶石(Na2AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)____________ .
(2)将0.1 mol/L AlCl3溶液和10%NH4F溶液混合制取Na2AlF6。该实验所用试管及盛装NaF 溶液的试剂瓶均为塑料材质,原因是____________ 。
(3)下列关于氧化铝的叙述正确的是
A.氧化铝可以治疗胃酸过多。
B.氧化铝因为熔点高,可以作耐火材料.
C.氧化铝是铝热剂的成分之一。
D.氧化铝是两性氧化物,所以既能浴于盐酸又能溶于氨水。
(4)某工厂排放出有毒物质NOCl , 它遇水就会生成NO3―。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为____________。水源中的NO3―对人类健康会产生危害。为了降低水源中NO3―的浓度,有研究人员建议在碱性条件下用铝粉将NO3―还原为N2,该反应的离子方程式为____________,此方法的缺点是处理后的水中生成了AlO2―,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理。已知25℃时,Ksp[Al(OH)3] = l.3×l0-33 Al(OH)3 AlO2-+H++H2O K=1.0×10-13,25℃时,若欲使上述处理后的水中AlO2―浓度降到1.0×10-6mol/L,则应调节至pH= ____________。此时水中c(A13+)= ____________
AlO2-+H++H2O K=1.0×10-13,25℃时,若欲使上述处理后的水中AlO2―浓度降到1.0×10-6mol/L,则应调节至pH= ____________。此时水中c(A13+)= ____________
-
铝(熔点660℃)是一种应用广泛的金属,工业上用A12O3(熔点2045℃)和冰晶石(Na2AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)____________ .
(2)将0.1 mol/L AlCl3溶液和10%NH4F溶液混合制取Na2AlF6。该实验所用试管及盛装NaF 溶液的试剂瓶均为塑料材质,原因是____________ 。
(3)下列关于氧化铝的叙述正确的是
A.氧化铝可以治疗胃酸过多。
B.氧化铝因为熔点高,可以作耐火材料.
C.氧化铝是铝热剂的成分之一。
D.氧化铝是两性氧化物,所以既能浴于盐酸又能溶于氨水。
(4)某工厂排放出有毒物质NOCl , 它遇水就会生成NO3―。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为____________。水源中的NO3―对人类健康会产生危害。为了降低水源中NO3―的浓度,有研究人员建议在碱性条件下用铝粉将NO3―还原为N2,该反应的离子方程式为____________,此方法的缺点是处理后的水中生成了AlO2―,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理。已知25℃时,Ksp[Al(OH)3] = l.3×l0-33 Al(OH)3 AlO2-+H++H2O K=1.0×10-13,25℃时,若欲使上述处理后的水中AlO2―浓度降到1.0×10-6mol/L,则应调节至pH= ____________。此时水中c(A13+)= ____________
AlO2-+H++H2O K=1.0×10-13,25℃时,若欲使上述处理后的水中AlO2―浓度降到1.0×10-6mol/L,则应调节至pH= ____________。此时水中c(A13+)= ____________
-
铝(熔点660℃)是一种应用广泛的金属,工业上用A12O3(熔点2045℃)和冰晶石(Na2AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(l)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)_______.
(2)将0.1 mol/L AlCl3溶液和10%NH4F溶液混合制取Na2AlF6。该实验所用试管及盛装NaF 溶液的试剂瓶均为塑料材质,原因是____________。
(3)下列关于氧化铝的叙述正确的是_______
A.氧化铝可以治疗胃酸过多。
B.氧化铝因为熔点高,可以作耐火材料.
C.氧化铝是铝热剂的成分之一。
D.氧化铝是两性氧化物,所以既能溶于盐酸又能溶于氨水。
(4)某工厂排放出有毒物质NOCl , 它遇水就会生成NO3-。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为_________,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理。
已知25℃时,Ksp[Al(OH)3] = l.3×l0-33 Al(OH)3 AlO2-+H++H2O K=1.0×10-13
AlO2-+H++H2O K=1.0×10-13
25℃时,若欲使上述处理后的水中A1O2-浓度降到1.0×10-6mol/L,则应调节至pH=_______。
此时水中c(A13+)=__________
-
铝(熔点660℃)是一种应用广泛的金属,工业上用Al2O3(熔点2045℃)和冰晶石(Na3AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,原因是____(用化学用语及相关文字说明)。
(2)将0.1mo/LAlCl3溶液和10%NH4F溶液混合制取Na3AlF6。该实验所用试管及盛装NaF溶液的试剂瓶均为塑料材质,原因是____(用离子方程式表示)。
(3)下列关于氧化铝的叙述正确的是_____。
A.氧化铝可以治疗胃酸过多 B.氧化铝因为熔点高,可以作耐火材料
C.氧化铝是铝热剂的成分之一 D.氧化铝是天然蓝宝石的主要成分
(4)以Al 和NiO(OH)为电极,NaOH 溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)某工厂排放出有毒物质NOC1,它遇水就会生成NO3-。NOCl 分子中各原子均满足8电子稳定结构,则NOCl的电子式为____。水源中的NO3-对人类健康会产生危害,为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为____。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是________(填编号)。
a.NH3比PH3稳定性强
b.常温下,氮气是气体,磷单质是固体
c.氮气与氢气化合比磷与氮气化合更容易
d.硝酸显强氧化性,磷酸不显强氧化性
(2)某温度下氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
i. 2NO(g)+Cl2(g) 2ClNO(g) △H1< 0
2ClNO(g) △H1< 0
ii. 2NO2(g)+ NaCl(s) NaNO3(s)+ClNO(g) △H2< 0
NaNO3(s)+ClNO(g) △H2< 0
现有反应4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) ,则反应热△H3=_____(用△H1、△H2表示)。
2NaNO3(s)+2NO(g)+Cl2(g) ,则反应热△H3=_____(用△H1、△H2表示)。
(3)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下发生反应:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
2NH3(g) △H=-92.4kJ/mol。达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
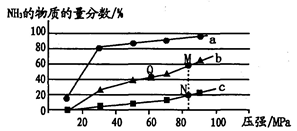
① 曲线a 对应的温度是_______________。
② 上图中M、N、Q点平衡常数K的大小关系是_________。
③ M点对应的H2转化率是_____________。
(4)亚硝酸盐是食品添加剂中毒性较强的物质之一。在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO。写出Cu+和亚硝酸根(NO2-)离子在酸性水溶液中反应的离子方程式__________。
(5)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。用氨水SO2,当吸收液显中性时,溶液中离子浓度关系正确的是_______(填字母)。(已知:NH4HSO3溶液显酸性。)
a.c(NH4+)=2c(SO32-)+c(HSO3-)
b.c(NH4+)>c(SO32-)>c(H+)=c(OH-)
c.c(NH4+)=c(SO32-)+c(HSO3-)+c(H2SO3)
-
含磷化合物在生产生活中有着重要的应用。
(1)磷与氨是同主族元素,下列能说明者非金属性强弱的是_______(填字母)。
a.NH3比PH3稳定性强
b.常温下,氮气为气体,磷单质为固体
c.氮气与氢气化合比磷与氢气化合更困难
d.HNO3的酸性比HPO3酸性强
(2)工业常用磷精矿[Ca5(PO4)3F]和硫酸反应制各磷酸。己知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+ H2O(l) △H=-271kJ/mol
5CaO(s)+3H3PO4(l)+HF(g)=Ca5(PO4)F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)F和硫酸反应制备磷酸的热化学方程式为________________。
(3)已知PCl5(g) PCl3(g)+Cl2(g) △H>0。温度为T时,把一定量的PCl5气体引入一真空瓶内,反应达平衡后PCl5与PCl3的分压之比为1:3(分压一总压×物质的量分数)。
PCl3(g)+Cl2(g) △H>0。温度为T时,把一定量的PCl5气体引入一真空瓶内,反应达平衡后PCl5与PCl3的分压之比为1:3(分压一总压×物质的量分数)。
①PCl5的分解率a1=_____%。若达到兴衡后体系总压为1.4MPa,用平衡分压代替平衡浓度表示反应的平衡常数Kp=_________。
②温度为T2时,新的平衡体系中PCl5与Cl2分压相同,则PCl5的分解率a1________a2,温度T1___ T2(填“>”“<”或“=”)。
③达到平衡后,下列情况使PCl5分解率增大的是___________(填字母)。
a.温度、体积不变,充入氩气 b.体积不变,对体系加热
C.温度、体积不变,充入氯气 d.温度不变,增大容器体积
(4)氧化水解法产三氯氧磷的废水中主要含有H3PO4、H3PO3等,可先加入适量漂白粉,再加入生石灰调节pH 将磷元素转化为磷酸的钙盐沉淀并回收。
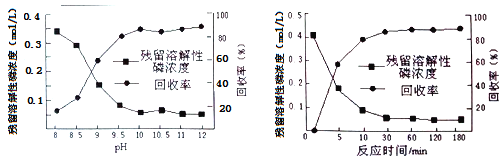
①在沉淀前先加入适量漂白粉的作用是__________________。
②下图是不同条件对磷的沉淀回收率的影响图像。处理该厂废水需控制的工艺条件为______。