-
A、B、C、D、E、R六种元素位于周期表的前四周期,其原子序数依次增大。已知A原子核外有三个未成对电子;B的最外层电子数是内层电子数的3倍;化合物C2E的晶体为离子晶体;D单质的熔点在同周期单质中最高;E原子核外的M层中只有两对成对电子;R原子核外最外层电子数与C相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D四种原子的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)C的氯化物的熔点比D的氯化物的熔点高,理由是 。
(3)基态R+离子的核外电子排布式是 。
(4)Q分子是A2B的等电子体,Q的结构式为 。
(5)图一是R单质的晶胞结构,配位数为 ;图二是B、R两元素组成的一种化合物的晶胞,其化学式为 。
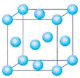
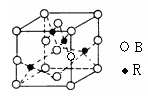
图一 图二
-
A、B、C、D、E五种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E位于同一主族,D的最外层电子数比B最外层电子数多2,C的最外层电子数是次外层的2.5倍.请回答下列问题:
(1)C、D氢化物中较稳定的是 ______ ;(填化学式)
(2)A、E可形成1:1型的化合物,两微粒间的化学键是 ______ ;写出C的气态氢化物的电子式 ______ ;
(3)写出D的一种同素异形体是 ______ .(写化学式)
(4)与B同族的单质在同周期元素中熔点最高、硬度最大,这种单质是 ______ ,熔点高、硬度大的原因是 _______________________ 。
-
已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大,X、W同主族,Y、Z为同周期的相邻元素,W原子的质子数等于Y、Z原子最外层电子数之和,Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)写出X、Y的元素符号:X______、Y______.
(2)W+和Z2-的核外电子排布相同,两种微粒半径大小关系为______.
(3)由X、Y、Z所形成的离子化合物的化学式是______,它与W的最高价氧化物的水化物的溶液反应时的离子方程式是______.
(4)已知拆开1mol X-X键、1mol Y≡Y、1mol Y-X键分别需要吸收的能量为436kJ、946kJ、391kJ.则由X2和Y2反应生成1mol YX3,需要______(填“放出”或“吸收”)的热量是______kJ.
-
中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
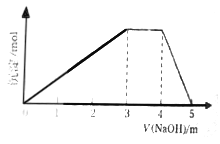
A. 简单的离子半径:M>Y>Z
B. 气态氢化物的热稳定性:Y>X
C. 由R、X、Y、M四种元素只组成一种盐
D. 最高价氧化物对应水化物的酸性:M>Z
-
中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生的沉淀质量与滴加氢氧化钠溶液体积的变化情况如图所示。下列说法不正确的是( )
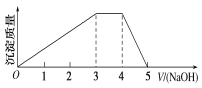
A.简单离子半径:M>Y>Z
B.气态氢化物的热稳定性:Y>X
C.最高价氧化物对应水化物的酸性:M>Z
D.由R、X、Y、M四种元素只能组成二种盐
-
已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z 原子的最外层电子数之和。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为 ,含有离子键和非极性 共价键的化合物的电子式为 ;含有极性共价键和非极性共价键的化合物的电子式为 。
共价键的化合物的电子式为 ;含有极性共价键和非极性共价键的化合物的电子式为 。
(2)由X、Y、Z所形成的常见离子化合物是 (写化学式),该化合物与[W的最高价氧化物对应水化物的浓溶液加热时反应的离子方程式为 。
-
已知 X、Y、Z、W 四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X 和 W 同主族,Y、Z 为同周期的相邻元素。W 原子的质子数等 于 Y、Z 原子最外层电子数之和。Y 的气态氢化物分子中有 3 个共价键。Z 原子 最外层电子数是次外层电子数的 3 倍。试推断:
(1)X、Y、Z、W 四种元素的符号:
X:____________;Y: ____________; Z:____________;W:_____________。
(2)由以上元素中的两种元素组成的共价化合物有_____,离子化合物有____________。(以上均任写两种)
(3)由 X、Y、Z 三种元素所形成的只含共价键的化合物是_____,既含共价键, 又含离子键的化合物是__。
-
已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)X、Y、Z、W四种元素的符号:X___、Y__、Z___、W_____
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为_____,_____.
(3)由X、Y、Z所形成的离子化合物是_____,它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是_____.
-
(14分)已知X、Y、Z、W四种元素是元素周期表中三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。试推断:
(1)X、Y、Z、W四种元素的符号:X________、Y________、Z 、W________。元素Z在周期表中的位置是______________________。
(2)由以上元素中的两种元素组成的化合物,溶于水后水溶液显碱性,该化合物的电子式分别为 、 ________ (任写2种)。
(3)由X、Y、Z所形成的共价化合物(Y呈最高价)是________,离子化合物是________。(均写化学式)
(4)由X和Y两种元素组成的18电子的分子为__________(写分子式),该分子中所有原子都已达到类似于稀有气体原子的稳定结构,则其结构式为__________。
-
已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)写出X、Y的元素符号:X________、Y________;
(2)W在元素周期表中的位置是________;Z的原子结构示意图________
(3)由X、Y、Z所形成的离子化合物的化学式是________,它与W的最高价氧化物的水化物的溶液反应时的离子方程式是________;
(4)用电子式表示Y的氢化物的形成过程________.



