-
下表是有关物质的 Ksp:
物质
CaCO3
MgCO3
Ca(OH)2
Mg(OH)2
Ksp(单位省略)
2.8×10-9
6.8×10-6
4.7×10-6
5.6×10-12
回答下列问题:
(1)某同学在实验室条件下模拟从海水中提取镁的生产过程。在加试剂时,误将纯碱溶液加入海水中;他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他_______(填“能” 或“不能”)将Mg2+转化为Mg(OH)2 沉淀,理由是_______。
(2)要制得无水 MgCl2,过滤出 Mg(OH)2 沉淀后,用试剂_________(填化学式)将其溶解。
(3)将得到的氯化镁溶液在浓缩池中制得 MgCl2·6H2O。然后将 MgCl2·6H2O 转移到干燥塔中,在干燥的 HCl 气流中加热 MgCl2·6H2O,才能得到无水 MgCl2,原因是:_________。
高二化学综合题中等难度题查看答案及解析
-
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ、25℃时有关物质的溶度积如下:
物质
CaCO3
MgCO3
Ca(OH)2
Mg(OH)2
Fe (OH)3
Ksp
4.96×10-9
6.82×10-6
4.68×10-6
5.61×10-12
2.64×10-39
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
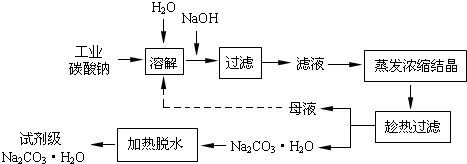
(1)加入NaOH溶液时,反应的离子方程式为__________________;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= ___________;
(3)“母液”中除了含有Na+、CO32-外,还含有_________等离子。
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行_________(填“可行”或“不可行”),并说明理由__________________;
(5)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g) △H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式__________________;
高二化学填空题困难题查看答案及解析
-
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
物质
CaCO3
MgCO3
Ca(OH)2
Mg(OH)2
溶度积
2.8×10-9
6.8×10-6
5.5×10-6
1.8×10-11
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为____(填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是____;如果不能直接投入,应将贝壳作何处理____,试写出化学方程式_______。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为_______(填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他___(填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是________。(用离子方程式表示)
(3)已知海水中镁离子浓度为1.8×10-3mol/L,则要使镁离子产生沉淀,溶液的pH最低应为___。
高二化学填空题中等难度题查看答案及解析
-
常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:
CaSO4
CaCO3
MgCO3
Mg(OH)2
CuS
BaSO4
H2S
H2CO3[]
KSP或Ka
9.1х10-6
2.8х10-9
6.8х10-6
1.8х10-11
6.3х10-36
1.1х10-10
Ka1=1.3х10-7
Ka2=7.1х10-15
Ka1=4.4х10-7
Ka2=4.7х10-11
则下列说法不正确的是
A.相同温度、相同浓度的钠盐溶液的pH:Na2S>Na2CO3>NaHS>NaCl>NaHSO4
B.在NaHS溶液中滴加硫酸铜溶液,生成黑色沉淀:HS-+Cu2+===CuS↓+H+
C.除去锅炉中的水垢时,通常先加入足量硫酸钠溶液,将碳酸钙转化成硫酸钙,然后再用酸液处理
D.在Mg(HCO3)2溶液中滴加澄清石灰水发生反应的离子方程式为Mg2++2HCO+2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O
高二化学选择题困难题查看答案及解析
-
下列对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的原因解释中正确的有
①Mg(OH)2的Ksp大于MgCO3的Ksp,且在水中发生了沉淀转化
②Mg(OH)2的Ksp小于MgCO3的Ksp,且在水中发生了沉淀转化
③MgCO3电离出的CO32-发生水解,使水中c(OH-)减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀
④MgCO3电离出的CO32-发生水解,使水中c(OH-)增大,对Mg(OH)2的沉淀溶解平衡而言,Qc>Ksp,生成Mg(OH)2沉淀
A.①② B.②④ C.③④ D.②③
高二化学选择题简单题查看答案及解析
-
目前世界各国获得镁的主要来源从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:
物质
CaCO3
MgCO3
Ca(OH)2
Mg(OH)2
溶度积
2.8×10-9
6.8×10-6
5.5×10-6
1.8×10-11
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为________(填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是________。如果不能直接投入,应将贝壳作何处理,试写出化学方程式:________。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为________。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ="=2" Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于________(选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为________。
③该氯化钙样品中钙元素的质量百分数为________。
高二化学填空题极难题查看答案及解析
-
下列化学方程式错误的是 ( )。
A.Ca(HCO3)2
CaCO3↓+CO2↑+H2O
B.Mg(HCO3)2
MgCO3↓+CO2↑+H2O
C.MgCO3+H2O
Mg(OH)2↓+CO2↑
D.CaCO3+H2O=Ca(OH)2+CO2↑
高二化学选择题中等难度题查看答案及解析
-
下列离子反应方程式正确的是
A. 在碳酸氢镁溶液中加入足量Ca(OH)2溶液: Mg2++HCO3-+Ca2++2OH–== MgCO3↓+CaCO3↓+2H2O
B. 将氯化亚铁溶液和稀硝酸混合:3Fe2++ 4H++NO3-= 3Fe3++2H2O+NO↑
C. 向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
D. 向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全: Al3+ +SO42—+Ba2+ +3OH—==BaSO4↓+Al(OH)3↓
高二化学选择题中等难度题查看答案及解析
-
煮沸暂时硬水时,不可能发生的反应是( )
A.Ca(HCO3)2CaCO3↓+H2O+CO2↑
B.Mg(HCO3)2MgCO3↓+H2O+CO2↑
C.MgCO3+H2OMg(OH)2+CO2↑
D.Mg(OH)2MgO+H2O
高二化学选择题中等难度题查看答案及解析
-
已知:某温度下,Ksp[Ca(OH)2]=5.5×10-6、Ksp[Mg(OH)2]=1.8×10-11、Ksp(AgCl)=1.8×10-10。相同条件下,在这三种物质的饱和溶液中,有关金属离子浓度的说法正确的是( )
A. Mg2+的浓度最小
B. Ca2+的浓度最小
C. Ag+的浓度最小
D. 同一温度下,难溶电解质的Ksp越大,溶液中的金属离子的浓度也越大
高二化学单选题中等难度题查看答案及解析