把0.1 molMnO2粉末加入50 mL过氧化氢的溶液里(密度为1.1 g·mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示。
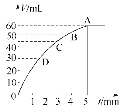
(1)实验时放出气体的体积为__________。
(2)放出一半气体所需的时间约为____________。
(3)根据曲线形状解释反应速率变化的原因________________________。
高一化学填空题简单题
把0.1 molMnO2粉末加入50 mL过氧化氢的溶液里(密度为1.1 g·mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示。

(1)实验时放出气体的体积为__________。
(2)放出一半气体所需的时间约为____________。
(3)根据曲线形状解释反应速率变化的原因________________________。
高一化学填空题简单题
把0.1 molMnO2粉末加入50 mL过氧化氢的溶液里(密度为1.1 g·mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示。

(1)实验时放出气体的体积为__________。
(2)放出一半气体所需的时间约为____________。
(3)根据曲线形状解释反应速率变化的原因________________________。
高一化学填空题简单题查看答案及解析
(10分)把0.1molMnO2粉末加入50ml过氧化氢的溶液里(密度为1.1g·mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示。
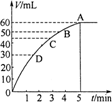
(1)实验时放出气体的体积为________。
(2)放出一半气体所需的时间约为________。
(3)A、B、C、D各点反应速率由快到慢的顺序是________。
(4)根据曲线形状解释反应速率变化的原因________。
(5)计算反应前过氧化氢的物质的量浓度________
高一化学填空题简单题查看答案及解析
将0.1mol MnO2粉末加入到50mL过氧化氢溶液(H2O2,ρ=1.1g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示.
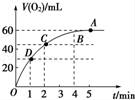
(1)实验时放出气体的总体积是 .
(2)放出一半气体所需的时间为 .
(3)反应放出体积气体所需的时间约为 .
(4)A,B,C,D各点反应速率的快慢顺序为
(5)解释反应速率变化的原因:
(6)计算H2O2初始状态的浓度 .
高一化学填空题中等难度题查看答案及解析
加入0.1 mol MnO2粉末于50 mL过氧化氢溶液(ρ=1.1 g·mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示。
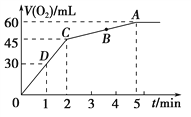
(1)实验时放出气体的总体积是_______________________________________。
(2)放出一半气体所需的时间为_________________________________________。
(3)反应放出3/4气体所需时间为_________________________________________________。
(4)A、B、C、D各点反应速率快慢的顺序为________________________________________。
(5)解释反应速率变化的原因是_______________________________________________。
(6)计算H2O2的初始物质的量的浓度________________________________________。
(7)求反应到2 min时,H2O2的质量分数_______________________________________。
高一化学综合题中等难度题查看答案及解析
加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g·mL-1),在标准状况下放出气体的体积和时间的关系如图所示,回答下列问题。
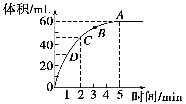
(1)A、B、C、D四点化学反应速率快慢的顺序为____________________。
(2)解释反应速率变化的原因__________________________________。
(3)计算过氧化氢的初始物质的量浓度________。
(4)求反应进行到2分钟时过氧化氢的质量分数。
高一化学填空题中等难度题查看答案及解析
(8分)为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2 粉末于 50 mL密度为1.1g∙cm-3 的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如右图所示。请依图回答下列问题:

(1)实验时放出气体的总体积为___________;
(2)放出一半气体所需要的时间为______________;
(3)ABCD四点化学反应速率的由快到慢顺序为 ___________ ;
(4)在5min后,收集到的气体体积不再增加,原因是________。
高一化学填空题简单题查看答案及解析
I:为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50 mL密度为 1.1 g/cm3的双氧水溶液中, 通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示。
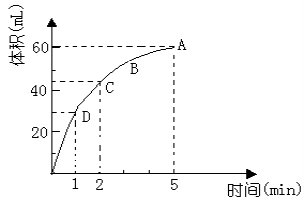
请依图回答下列问题:
(1)放出一半气体所需要的时间为________________________;
(2)A、B、C、D各点反应速率快慢的顺序是__________________;
(3)在5min后,收集到的气体体积不再增加,原因是________________________;
(4)过氧化氢溶液的初始物质的量浓度为_______________________(保留两位有效数字)
II: 在2L的密闭容器中充入一定量的SO3 气体,在一定温度和催化剂作用下,发生反应:2SO3
2SO2+O2,4min测得n(O2)=0.8mol,n(SO3)=6.4mol。
求: n(SO2) =___________;氧气的生成速率v (O2)__________; SO3的转化率_________________。
高一化学填空题中等难度题查看答案及解析
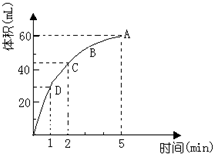
高一化学解答题中等难度题查看答案及解析

高一化学填空题中等难度题查看答案及解析
标准状况下,1体积水中能溶解500体积的HCl气体。若向水中通入标准状况下的44.8 L HCl气体配成1L溶液,假设气体完全溶解,得溶液中含HCl的物质的量浓度为;若得溶液密度为1.1g/cm3,则溶液中含HCl质量分数为________;从该溶液中取出10 mL浓盐酸溶解于水配制成250 mL溶液,配制后的稀溶液中含HCl物质的量浓度为________。在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有________;配制过程中,造成浓度偏低的操作可能有________(选填下列操作的序号)。
A、容量瓶蒸馏水洗后未加干燥
B、量筒用蒸馏水洗后未干燥
C、将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量中加水到刻度
D、用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线
E、定容时,俯视液面加水至刻度线
高一化学实验题简单题查看答案及解析